فهرست عناوین
- مقدمه
- تعریف اسید هیدروکلریک (HCl)
- درک قطبیت مولکولی
- قطبیت مولکول HCl
- قطبیت آب به عنوان حلال
- شبیه در شبیه حل می شود: حلال های قطبی و مواد قطبی
- مقایسه حلالیت مواد قطبی و غیرقطبی
- برهم کنش مولکولی بین HCl و آب
- تفکیک (یونش) HCl در آب
- آبپوشی یون ها توسط آب قطبی
- انحلال گرماده HCl
- حلالیت بسیار بالای HCl : نگاهی کمی
- نامحلول بودن HCl در حلال های غیرقطبی
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 08-10-1404
تاریخ بروزرسانی مقاله : 08-10-1404
تعداد کلمات : 3600
آدرس مقاله : لینک مقاله
قابلیت حل شدن اسید کلریدریک در آب ناشی از قطبیت آن

مقدمه
هیدروژن کلرید در شرایط معمول به شکل یک گاز شناخته می شود، اما نکته مهم اینجاست که وقتی با آب تماس پیدا می کند، خیلی سریع در آن حل می شود. حاصل این فرایند، مایعی با خاصیت اسیدی بالا است که آن را با نام اسید هیدروکلریک می شناسند و در حوزه های مختلف کاربرد دارد.
این رفتار خاص به ساختار مولکولی آن برمی گردد. در ترکیب هیدروژن کلرید، توزیع بار الکتریکی یکنواخت نیست و همین نابرابری باعث می شود مولکول تمایل زیادی به برقراری ارتباط با آب داشته باشد. این ویژگی، نقش اصلی را در حل شدن سریع آن ایفا می کند.
آب هم از نظر ساختاری رفتاری مشابه دارد و به همین دلیل می تواند چنین موادی را به راحتی در خود نگه دارد. وقتی این دو ماده با هم ترکیب می شوند، واکنشی سریع رخ می دهد که همراه با آزاد شدن گرماست و در مدت کوتاهی یک محلول پایدار شکل می گیرد.
در چنین شرایطی به ویژه در محیط های صنعتی و آزمایشگاهی، انتخاب ماده اولیه با کیفیت اهمیت بالایی دارد. به همین دلیل بسیاری از مصرف کنندگان به دنبال خرید اسید کلریدریک کیمیا کلر کبودان ارومیه گالن 20 لیتری هستند تا از یکنواختی، قدرت مناسب و عملکرد قابل اعتماد محلول نهایی اطمینان داشته باشند.
در نهایت، همین ویژگی ساده اما مهم توضیح می دهد چرا هیدروژن کلرید به راحتی در آب حل می شود و یکی از قوی ترین محلول های اسیدی پرکاربرد را به وجود می آورد؛ محلولی که اگر درست انتخاب و استفاده شود، می تواند پاسخگوی نیازهای متنوع و حساس باشد.
تعریف اسید هیدروکلریک (HCl)
اسید هیدروکلریک زمانی به وجود می آید که یک گاز خاص در آب حل شود. این گاز به تنهایی دیده نمی شود اما بوی تند و تیزی دارد که به راحتی قابل تشخیص است. وقتی با آب ترکیب می شود، مایعی به دست می آید که اثرگذاری بالایی دارد و نمی توان آن را یک ماده معمولی دانست.
این مایع قدرت زیادی در واکنش با مواد مختلف دارد و به همین دلیل در بسیاری از کارها مورد استفاده قرار می گیرد. تماس آن با بعضی سطوح می تواند باعث تغییر یا حتی از بین رفتن آنها شود، به همین خاطر همیشه باید با دقت و رعایت نکات ایمنی از آن استفاده کرد.
جالب است بدانیم که این ماده فقط مخصوص کارخانه ها یا محیط های فنی نیست. مقدار کمی از آن به طور طبیعی در بدن انسان وجود دارد و نقش مهمی در شکستن غذا و آماده سازی آن برای جذب بهتر ایفا می کند. بدون حضور این ماده، فرایند گوارش به درستی انجام نمی شود.
در محیط های کاری، از اسید هیدروکلریک برای تمیز کردن، آماده سازی سطوح و کنترل شرایط استفاده می شود. حتی در بعضی مصارف خانگی و ساختمانی هم نمونه های رقیق شده آن در دسترس است و افراد برای کارهای مشخص از آن بهره می برند.
با این حال، نباید فراموش کرد که این ماده هرچه غلیظ تر باشد، خطر بیشتری دارد. بخارهای تند آن می تواند در هوا پخش شود و ایجاد سوزش کند. به همین دلیل نگهداری و استفاده درست از آن اهمیت زیادی دارد و بی احتیاطی در کار با آن می تواند دردسرساز شود.
درک قطبیت مولکولی
وقتی دو اتم به هم وصل می شوند، همیشه الکترون ها را به یک اندازه با هم شریک نمی شوند. بعضی اتم ها تمایل بیشتری دارند الکترون ها را به سمت خود بکشند و همین موضوع باعث می شود توزیع بار در مولکول یکنواخت نباشد. نتیجه این نابرابری، به وجود آمدن دو ناحیه متفاوت در یک مولکول است.
در چنین حالتی، یک سمت مولکول کمی منفی تر و سمت دیگر کمی مثبت تر می شود. به این وضعیت می گویند مولکول دو قطبی. آب نمونه شناخته شده ای از این نوع رفتار است و به همین دلیل ویژگی های خاصی مثل حل کردن مواد مختلف را دارد. در بررسی لحظه دوقطبی مولکول اسید کلریدریک (قطبیت مولکولی) نیز دقیقا همین پدیده دیده می شود، جایی که کشش قوی تر الکترون ها توسط یکی از اتم ها باعث ایجاد این دوگانگی بار می شود.
در مقابل، بعضی مولکول ها چنین تفاوتی را تجربه نمی کنند. وقتی اتم ها از یک نوع باشند یا قدرت کشش آنها شبیه هم باشد، الکترون ها به شکل متعادل پخش می شوند. در این حالت مولکول نه سمت مثبت مشخصی دارد و نه سمت منفی، و به همین دلیل غیرقطبی به حساب می آید.
نکته جالب اینجاست که شکل قرار گرفتن اتم ها هم اهمیت دارد. گاهی با وجود اینکه پیوندها نابرابر هستند، چینش مولکول طوری است که اثرها یکدیگر را خنثی می کنند. در نتیجه، کل مولکول رفتاری خنثی از خود نشان می دهد.
همین تفاوت ساده توضیح می دهد چرا بعضی مواد به راحتی در هم حل می شوند و بعضی دیگر اصلا با هم کنار نمی آیند. به طور کلی، شباهت در این ویژگی باعث جذب می شود و تفاوت زیاد، مانع مخلوط شدن مواد با یکدیگر خواهد شد.
قطبیت مولکول HCl
مولکول HCl از دو جزء ساده ساخته شده است: یک اتم هیدروژن و یک اتم کلر. با این حال، همین ترکیب ساده رفتاری متفاوت از آنچه در ظاهر دیده می شود دارد. دلیل اصلی این تفاوت، تمایل بیشتر کلر به جذب الکترون ها نسبت به هیدروژن است؛ موضوعی که باعث می شود پیوند بین این دو کاملا متعادل نباشد.
در این پیوند، الکترون ها بیشتر به سمت کلر کشیده می شوند. به همین خاطر، کلر کمی بار منفی و هیدروژن اندکی بار مثبت پیدا می کند. این نابرابری باعث می شود مولکول HCl حالتی دو قطبی داشته باشد؛ یعنی دو سر آن رفتار یکسانی نداشته باشند و هر کدام واکنش متفاوتی نشان دهند.
اگرچه در حالت گازی نمی توان HCl را یک ماده کاملا یونی دانست، اما توزیع نامتقارن بار الکتریکی باعث می شود رفتاری نزدیک به ترکیبات یونی از خود نشان دهد. همین ویژگی سبب می شود مولکول های HCl بتوانند یکدیگر را جذب کنند و کنار هم قرار بگیرند، حتی بدون آن که پیوند واقعی یونی تشکیل شود.
نکته مهم تر، ارتباط این ویژگی با آب است. آب هم ساختاری قطبی دارد و به همین دلیل با موادی که رفتار مشابهی دارند، سازگارتر است. بخش مثبت HCl به سمت ناحیه های منفی آب کشیده می شود و بخش منفی آن با قسمت های مثبت مولکول های آب تعامل برقرار می کند.
در نتیجه این برهم کنش ها، هیدروژن کلرید خیلی راحت در آب حل می شود و محلولی قوی به وجود می آورد. هرچند شدت این خاصیت از آب کمتر است، اما به اندازه ای هست که توضیح دهد چرا HCl یکی از گازهایی است که به سرعت و بدون مقاومت وارد آب می شود و محلولی پایدار و پرکاربرد تشکیل می دهد.
قطبیت آب به عنوان حلال
آب از نظر شیمیایی رفتاری ویژه دارد و به همین دلیل یکی از مهم ترین حلال ها در طبیعت به شمار می رود. این ماده به شدت قطبی است و می تواند بسیاری از مواد یونی و قطبی را به خوبی در خود حل کند. ساختار مولکول آب خمیده است و دو اتم هیدروژن به یک اتم اکسیژن متصل شده اند؛ همین شکل خاص، پایه بسیاری از ویژگی های آن را تشکیل می دهد.
اکسیژن نسبت به هیدروژن الکترون ها را قوی تر جذب می کند، در نتیجه پیوندهای میان آن ها یکنواخت نیستند. به همین علت، سمت اکسیژن مولکول کمی بار منفی و ناحیه هیدروژن ها کمی بار مثبت پیدا می کند. چون مولکول آب صاف و خطی نیست، این بارهای جزئی یکدیگر را خنثی نمی کنند و آب به صورت یک مولکول با دوقطبی قوی باقی می ماند.
یکی از پیامدهای مهم این قطبیت، ایجاد پیوند هیدروژنی بین مولکول های آب است. در این نوع برهم کنش، هیدروژن یک مولکول به اکسیژن مولکول دیگر جذب می شود و شبکه ای از ارتباطات ضعیف اما مؤثر شکل می گیرد. همین پیوندها دلیل نقطه جوش بالا، کشش سطحی زیاد و پایداری غیرعادی آب در مقایسه با مولکول های مشابه هستند.
وقتی ماده ای در آب حل می شود، مولکول های آب اطراف ذرات آن قرار می گیرند و آن ها را پایدار می کنند. بخش منفی آب به سمت یون های مثبت و ناحیه مثبت آن به سوی یون های منفی یا قسمت های الکترون دار می چرخد. این توانایی در جدا کردن و احاطه ذرات، باعث شده آب بتواند طیف گسترده ای از ترکیبات را در خود حل کند و به همین دلیل به آن لقب حلال همگانی داده اند.
شبیه در شبیه حل می شود: حلال های قطبی و مواد قطبی
در شیمی یک جمله معروف وجود دارد که می گوید «شبیه در شبیه حل می شود». این عبارت ساده توضیح می دهد چرا بعضی مواد به راحتی با هم مخلوط می شوند و بعضی دیگر نه. اگر دو ماده از نظر قطبیت به هم نزدیک باشند، معمولاً تمایل دارند در یکدیگر حل شوند، اما وقتی تفاوت زیادی بین آن ها باشد، این اتفاق به سختی رخ می دهد.
حلال های قطبی مثل آب، برای حل کردن مواد قطبی یا یونی بسیار مناسب هستند. علت این موضوع، وجود نیروهای جاذبه قوی بین ذرات هم جنس است. به همین دلیل آب می تواند موادی مانند نمک خوراکی یا شکر را بدون مشکل در خود حل کند، چون از نظر رفتاری با آن ها سازگاری دارد.
در مقابل، مواد قطبی با ترکیبات غیرقطبی رابطه خوبی ندارند. مثال شناخته شده آن آب و روغن است که حتی با هم زدن هم به صورت یکنواخت مخلوط نمی شوند. روغن غیرقطبی است و نمی تواند وارد ساختار منظم و پیوندهای بین مولکولی آب شود، بنابراین جدا باقی می ماند و یک لایه مستقل تشکیل می دهد.
از سوی دیگر، حلال های غیرقطبی مانند هگزان برای حل کردن روغن ها و چربی ها بسیار کارآمد هستند، اما در برابر مواد قطبی یا یونی عملکرد ضعیفی دارند. این قاعده کلی نشان می دهد هر ماده ای در محیطی بهتر حل می شود که نیروهای بین مولکولی آن با حلال هماهنگ باشد. به همین دلیل هیدروژن کلرید که ماهیتی قطبی دارد، در آب به خوبی حل می شود ولی در حلال های غیرقطبی تقریباً نامحلول باقی می ماند.
مقایسه حلالیت مواد قطبی و غیرقطبی
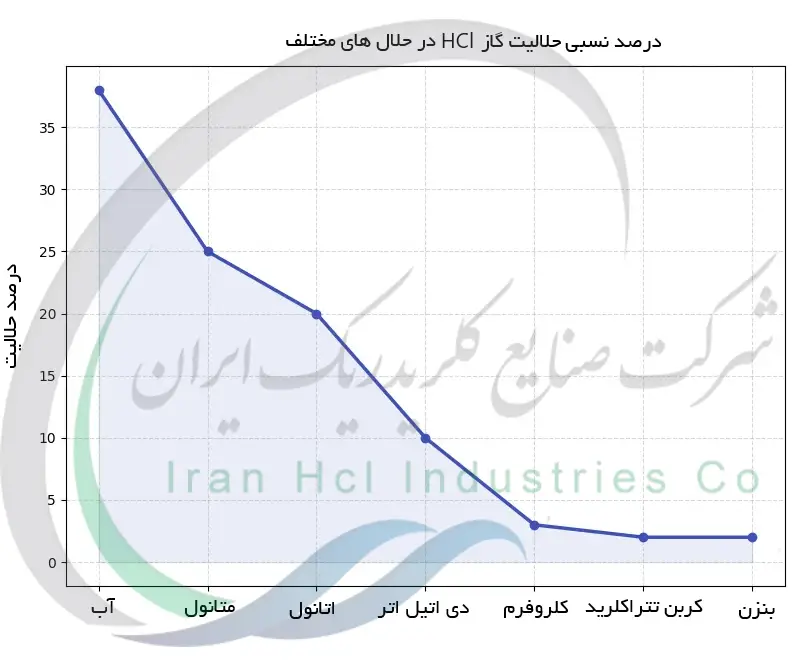
برای درک بهتر این که چرا «شبیه در شبیه حل می شود»، می توان رفتار مواد مختلف را هنگام تماس با آب بررسی کرد. آب به بعضی ترکیبات اجازه می دهد به راحتی در آن پخش شوند، اما در برابر برخی دیگر تقریباً بی تفاوت است. این تفاوت بیشتر به قطبی یا غیرقطبی بودن ماده برمی گردد.
مواد قطبی یا یونی معمولاً رابطه خوبی با آب دارند. برای نمونه، هیدروژن کلرید که ماهیتی قطبی دارد، به سرعت در آب حل می شود. در مقابل، اکسیژن که یک مولکول غیرقطبی است، فقط مقدار بسیار کمی در آب حل می گردد و بیشتر به صورت گاز باقی می ماند.
در میان مایعات هم همین الگو دیده می شود. اتانول به دلیل ساختار قطبی خود، کاملاً با آب مخلوط می شود و مرزی بین آن ها باقی نمی ماند. اما هگزان که غیرقطبی است، حتی پس از هم زدن نیز از آب جدا می ماند و یک لایه مستقل تشکیل می دهد.
اگر نمونه های مختلف را کنار هم قرار دهیم، نتیجه روشن تر می شود. موادی که می توانند با آب برهم کنش قوی برقرار کنند یا در آن یونیزه شوند، به سادگی حل می شوند. در مقابل، ترکیبات غیرقطبی تعامل مؤثری با آب ندارند و یا اصلاً حل نمی شوند یا فقط مقدار بسیار ناچیزی از آن ها وارد محلول می شود.
این رفتار محدود به یک حالت خاص نیست و در گازها، مایعات و جامدات به شکل مشابهی دیده می شود. از گازهایی مثل HCl و NH₃ گرفته تا مایعاتی مانند الکل ها و حتی جامداتی مثل نمک و شکر، همگی نشان می دهند که قطبیت مولکولی نقش تعیین کننده ای در میزان حلالیت در آب دارد.
| ماده | قطبیت/نوع | حلالیت در آب | نوع برهم کنش | توضیح |
|---|---|---|---|---|
| هیدروژن کلرید (HCl) | کووالانسی قطبی | بسیار زیاد (~720 g/L در 20°C) | یون-دوقطبی (تشکیل H₃O⁺ و Cl⁻) | قطبی؛ در آب به طور کامل یونیزه میشود. |
| آمونیاک (NH₃) | کووالانسی قطبی | زیاد (~480 g/L در 20°C) | پیوند هیدروژنی | قطبی؛ پیوند هیدروژنی تشکیل میدهد (هیدروکسید آمونیوم در آب). |
| اتانول (C₂H₅OH) | قطبی (پروتیک) | قابل امتزاج (کاملاً محلول) | پیوند هیدروژنی | قطبی پروتیک؛ از طریق پیوند هیدروژنی با آب کاملاً مخلوط میشود. |
| سدیم کلرید (NaCl) | یونی | زیاد (~360 g/L در 25°C) | یون-دوقطبی | جامد یونی؛ قطبیت آب یونهای Na⁺ و Cl⁻ را پایدار میکند. |
| سوکروز (شکر) | کووالانسی قطبی | زیاد (~2000 g/L در 20°C) | پیوند هیدروژنی | بسیار قطبی؛ پیوند هیدروژنی گستردهای با آب تشکیل میدهد. |
| روغن (هگزان) | کووالانسی غیرقطبی | ناچیز (غیرمحلول) | ندارد (فقط واندروالسی) | غیرقطبی؛ نمیتواند وارد شبکه پیوند هیدروژنی آب شود. |
| اکسیژن (O₂) | دواتمی غیرقطبی | کم (~0.009 g/L در 20°C) | پراکندگی ضعیف | غیرقطبی؛ جاذبه بسیار اندکی با آب دارد (حلالیت بسیار کم). |
برهم کنش مولکولی بین HCl و آب
وقتی گاز HCl وارد آب می شود، خیلی زود میان مولکول های آن و مولکول های آب نیروهای جاذبه شکل می گیرد. هیدروژن که در ساختار HCl بار جزئی مثبت دارد، به سمت اکسیژن آب که اندکی بار منفی دارد کشیده می شود. هم زمان، اتم کلر با بار جزئی منفی به سوی هیدروژن های اطراف در مولکول های آب جذب می گردد.
در این وضعیت، چند مولکول آب می توانند پیرامون یک مولکول HCl قرار بگیرند و طوری جهت گیری کنند که بخش های با بار مخالف رو به آن باشند. این آرایش باعث می شود نیروهایی از جهات مختلف به پیوند H–Cl وارد شود و استحکام آن به تدریج کاهش یابد.
در عمل، همین نیروهای ضعیف اما متعدد باعث شکسته شدن پیوند بین هیدروژن و کلر می شوند. در نتیجه، مولکول HCl به یون های H⁺ و Cl⁻ تفکیک می گردد. البته یون هیدروژن به صورت آزاد باقی نمی ماند و خیلی سریع با آب ترکیب شده و یون H₃O⁺ را به وجود می آورد.
این فرایند هنگام حل شدن گاز HCl در آب با سرعت بالا و همراه با آزاد شدن گرما انجام می شود. نقش اصلی را قطبیت آب ایفا می کند؛ مولکول های آب با احاطه کردن اجزای HCl، نیروی جاذبه میان آن ها را تضعیف می کنند. به این ترتیب، آب محیطی پایدار فراهم می آورد که در آن تجزیه HCl به یون ها به سادگی امکان پذیر می شود.
تفکیک (یونش) HCl در آب
وقتی هیدروژن کلرید وارد آب می شود، دیگر به شکل یک مولکول مستقل باقی نمی ماند و به طور کامل به اجزای باردار تبدیل می شود. در واقع HCl در محیط آبی پایدار نیست و بلافاصله با آب وارد واکنش می گردد.
این واکنش را می توان به صورت ساده چنین نوشت:
HCl + H₂O → H₃O⁺ + Cl⁻
در این فرایند، یون هیدرونیوم همان مولکول آب است که یک پروتون اضافی دریافت کرده و یون کلرید نیز بخش منفی باقی مانده از HCl محسوب می شود. به بیان دیگر، پروتون از هیدروژن کلرید جدا شده و به آب منتقل می گردد.
همین رفتار باعث می شود HCl در دسته اسیدهای قوی قرار بگیرد. چون تقریباً تمام مولکول های حل شده آن یونیزه می شوند، می توان گفت این ماده در آب به طور کامل تفکیک می شود. به همین دلیل در محلول آبی، مولکول خنثی HCl عملاً وجود ندارد و همه آن به یون های آبپوشیده تبدیل شده است.
اهمیت تشکیل یون هیدرونیوم در این جا روشن می شود، زیرا همین یون ها عامل اصلی خاصیت اسیدی محلول هستند. کاهش pH و واکنش سریع با بازها مستقیماً به حضور این یون ها در آب وابسته است.
آبپوشی یون ها توسط آب قطبی
بعد از آن که HCl در آب به یون های H₃O⁺ و Cl⁻ جدا می شود، مولکول های آب بلافاصله اطراف این ذرات باردار را می گیرند و آن ها را پایدار می کنند. به این فرایند آبپوشی یا هیدراتاسیون گفته می شود و نقش مهمی در رفتار محلول دارد. قطبی بودن آب باعث می شود بتواند یون ها را به شکل مؤثری در محیط نگه دارد.
یون هیدرونیوم که بار مثبت دارد، به گونه ای احاطه می شود که بخش اکسیژن مولکول های آب رو به آن قرار می گیرد. این یون می تواند هم زمان با چند مولکول آب پیوند هیدروژنی برقرار کند و به این ترتیب، بار مثبت خود را در میان یک مجموعه از مولکول ها پخش نماید.
در مقابل، یون کلرید با بار منفی توسط آب به شکلی متفاوت احاطه می شود. در این حالت، سمت هیدروژن مولکول های آب که بار جزئی مثبت دارد، به سوی کلرید جهت گیری می کند. لایه ای از آب که هر یون را در بر می گیرد، پوسته آبپوشی نام دارد.
برهم کنش میان یون ها و دوقطبی های آب با آزاد شدن انرژی همراه است که به آن حرارت آبپوشی می گویند. این انرژی باعث می شود حل شدن از نظر ترمودینامیکی مطلوب باشد. آبپوشی همچنین مانع می شود یون های با بار مخالف دوباره به سادگی به هم متصل شوند. هر یون به طور جداگانه در محلول باقی می ماند و کاملاً توسط آب محافظت می شود. این پوسته های پایدار نشان می دهند چرا آب یکی از قدرتمندترین حلال ها برای گونه های باردار به شمار می رود.
انحلال گرماده HCl
حل شدن HCl در آب با آزاد شدن مقدار زیادی گرما همراه است و به همین دلیل آن را یک فرایند گرماده می دانند. افرادی که تجربه تهیه محلول اسید هیدروکلریک غلیظ یا رقیق کردن آن را دارند، معمولاً متوجه می شوند که ظرف به طور محسوس داغ می شود. اگر گاز HCl بدون دقت در آب حل شود، گرمای آزاد شده می تواند آن قدر زیاد باشد که محلول به جوش بیاید یا حتی به اطراف پاشیده شود.
دلیل این رفتار به تغییرات انرژی در حین واکنش برمی گردد. در مراحل اولیه، برای شکستن پیوند H–Cl و جدا کردن مولکول ها، مقداری انرژی مصرف می شود. همچنین بخشی از نیروهای جاذبه بین مولکول های آب نیز باید تضعیف گردد تا فرایند پیش برود.
در ادامه، زمانی که یون های H₃O⁺ و Cl⁻ تشکیل می شوند و مولکول های آب اطراف آن ها را می گیرند، شرایط کاملاً تغییر می کند. آبپوشی این یون ها با ایجاد جاذبه های قوی یون-دوقطبی همراه است و در این مرحله انرژی قابل توجهی آزاد می شود. این انرژی آزاد شده از مقدار انرژی مصرف شده در ابتدا بیشتر است و در نهایت باعث گرم شدن محلول می گردد.
به همین علت، هنگام افزودن HCl به آب باید نهایت دقت را به خرج داد. آزاد شدن سریع گرما می تواند خطرناک باشد و اگر اسید به آرامی و با رقیق سازی مناسب اضافه نشود، امکان جوشیدن یا پاشش محلول وجود دارد.
حلالیت بسیار بالای HCl : نگاهی کمی
گاز هیدروژن کلرید توانایی بسیار زیادی برای حل شدن در آب دارد و این ویژگی آن را از بسیاری گازها متمایز می کند. به صورت عددی، در دمای حدود ۲۰ درجه سانتی گراد هر لیتر آب می تواند نزدیک به ۷۲۰ گرم HCl را در خود نگه دارد که معادل محلولی با غلظت تقریبی ۳۷ درصد وزنی است.
با تغییر دما، این مقدار کمی دستخوش تغییر می شود. در دمای صفر درجه، میزان انحلال حتی بالاتر می رود و به حدود ۸۲۳ گرم در هر لیتر می رسد. در مقابل، با افزایش دما تا حدود ۶۰ درجه سانتی گراد، حلالیت کاهش پیدا می کند و به حدود ۵۶۱ گرم در لیتر می رسد. این رفتار نشان می دهد که در این سیستم، بالا رفتن دما باعث افت نسبی توان حل کنندگی آب می شود.
به همین دلیل، اسید هیدروکلریک غلیظی که به صورت تجاری عرضه می شود معمولاً غلظتی در بازه ۳۲ تا ۳۶ درصد دارد. این محدوده تقریباً بیشترین مقداری است که آب در دمای معمول می تواند به شکل پایدار نگه دارد. از دید مولی نیز، یک لیتر آب در شرایط عادی قادر است حدود ۲۰ مول HCl را جذب کند که برابر با حجم بسیار زیادی از گاز HCl در شرایط استاندارد است.
چنین ظرفیت بالایی نشان دهنده سازگاری قوی میان آب و HCl است. اگر غلظت از حدود ۳۷ درصد فراتر رود، محلول به حالت اشباع می رسد و HCl اضافی دیگر حل نمی شود. در این حالت، گاز آزاد شده و پدیده دود کردن اسید هیدروکلریک مشاهده می گردد. این حلالیت چشمگیر، مستقیماً به قطبیت HCl و توانایی آن در تشکیل یون های آبپوشی شده مربوط است؛ آب تا رسیدن به مرز اشباع، HCl را با تمایل زیاد در خود جذب می کند.
نامحلول بودن HCl در حلال های غیرقطبی
با وجود این که HCl در آب به آسانی حل می شود، در حلال های غیرقطبی رفتاری کاملاً متفاوت نشان می دهد. در چنین محیط هایی، مانند هیدروکربن هایی نظیر هگزان یا تولوئن، شرایط لازم برای برقراری برهم کنش های قوی با یک مولکول قطبی وجود ندارد.
در این حلال ها، مولکول های HCl فقط می توانند نیروهای بسیار ضعیف واندروالسی با مولکول های غیرقطبی برقرار کنند. این نیروها آن قدر کم هستند که نه می توانند پیوندهای میان مولکول های HCl را بشکنند و نه انرژی لازم برای جدا شدن آن از فاز خودش را فراهم نمایند. به همین دلیل، هیدروژن کلرید در مایعات کاملاً غیرقطبی تقریباً حل نمی شود و معمولاً به صورت گاز جدا باقی می ماند یا تنها مقدار بسیار کمی از آن وارد محلول می شود.
نکته مهم تر این است که حتی در صورت حل شدن جزئی HCl در یک حلال غیرقطبی، فرآیند یونیزه شدن تقریباً رخ نمی دهد. علت این موضوع آن است که چنین حلال هایی توانایی پایدار کردن یون های H⁺ و Cl⁻ را ندارند. در نتیجه، HCl در این محیط ها رفتار یک اسید قوی را نشان نمی دهد.
این تفاوت آشکار میان رفتار HCl در آب و در حلال های غیرقطبی، نقش تعیین کننده قطبیت را به خوبی نشان می دهد. حلال های قطبی مانند آب می توانند HCl را هم حل کنند و هم به یون تبدیل نمایند، اما حلال های غیرقطبی از انجام این کار ناتوان اند و در عمل HCl را تقریباً حل نشده باقی می گذارند.




