فهرست عناوین
- مقدمه
- درک قطبیت مولکولی
- نقش الکترونگاتیویته در پیوندهای شیمیایی
- الکترونگاتیویته هیدروژن و کلر
- چرا مولکول HCl قطبی است
- قطبیت HCl در برابر مولکول های غیرقطبی
- پیوند کووالانسی قطبی در برابر ویژگی یونی در HCl
- گشتاور دوقطبی مولکول HCl
- تأثیر قطبیت مولکولی بر ویژگی های HCl
- مقایسه قطبیت: هیدروژن هالیدها و مولکول های دیگر
- مقیاس ها و مقادیر الکترونگاتیویته
- اختلاف الکترونگاتیویته و مرزهای نوع پیوند
- قطبیت HCl در محلول آبی
- روندهای الکترونگاتیویته در جدول تناوبی
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 22-08-1404
تاریخ بروزرسانی مقاله : 22-08-1404
تعداد کلمات : 3300
آدرس مقاله : لینک مقاله
قطبیت مولکول اسید کلریدریک و الکترونگاتیوی

مقدمه
اسید هیدروکلریک (HCl) یک ماده شیمیایی شناخته شده است که نمونه ای کلاسیک از ظهور قطبیت مولکولی محسوب می شود. این مولکول ساده ی دواتمی از هیدروژن و کلر تشکیل شده و اختلافی که در میزان کشش هر اتم بر الکترون های مشترک وجود دارد باعث توزیع نابرابر بار الکتریکی در آن می شود. مفهوم قطبیت همین جدایش بار الکتریکی در سراسر یک مولکول را توصیف می کند و مستقیماً ناشی از اختلاف الکترونگاتیویته بین اتم های پیوندی است.
در مولکول HCl، کلر الکترون ها را بسیار قوی تر از هیدروژن به سوی خود می کشد و در نتیجه این مولکول قطبی شده و انتهای کلر آن دارای بار جزئی منفی و انتهای هیدروژن دارای بار جزئی مثبت می شود. قطبیت و الکترونگاتیویته از مفاهیم بنیادی در شیمی است که بر ویژگی هایی مانند حلالیت، نقطه ی جوش و قدرت اسیدی مواد تأثیر می گذارد. در بسیاری از صنایع شیمیایی و آزمایشگاهی، شناخت دقیق رفتار قطبی مولکول ها به ویژه در مورد اسید هیدروکلریک برای انتخاب نوع ماده، غلظت مناسب و روش استفاده اهمیت زیادی دارد.
همین موضوع سبب می شود تصمیم گیری درباره تأمین این ماده در بخش هایی مانند خرید اسید کلریدریک ارومیه بر پایه ی آگاهی علمی از ساختار و قطبیت این مولکول انجام شود تا کیفیت، خلوص و عملکرد مطلوب آن در فرایندهای صنعتی یا آزمایشگاهی تضمین گردد. این مقاله به بررسی قطبیت مولکول اسید هیدروکلریک و نقش الکترونگاتیویته می پردازد و با دیدی جامع توضیح می دهد که چرا مولکول HCl قطبی است و چگونه تفاوت الکترونگاتیویته به طور کلی بر پیوندهای شیمیایی اثر دارد.
درک قطبیت مولکولی
قطبیت مولکولی به توزیع نابرابر بار الکتریکی در یک مولکول گفته می شود. زمانی که اتم های یک مولکول به دلیل اختلاف در تمایلشان به الکترون ها (الکترونگاتیویته)، الکترون های مشترک را به طور نامساوی به اشتراک می گذارند، پیوند قطبی شکل می گیرد و روی هر سر پیوند بارهای جزئی ایجاد می شود. اتمی که الکترون ها را قوی تر جذب می کند دارای بار منفی جزئی (δ⁻) می گردد، در حالی که اتم دیگر اندکی مثبت (δ⁺) می شود. اگر یک مولکول دست کم یک پیوند قطبی داشته باشد و هندسه ی مولکولی آن طوری نباشد که قطبیت پیوند را خنثی کند، کل آن مولکول قطبی به حساب می آید.
چنین مولکول های قطبی دارای گشتاور دوقطبی قابل اندازه گیری هستند که کمیتی برداری است و بزرگی و جهت جدایش بار را نشان می دهد. در مقابل اگر الکترون ها به طور برابر به اشتراک گذاشته شوند یا اگر پیوندهای قطبی به صورت متقارن در ساختار مولکول قرار گرفته باشند، ممکن است مولکول در مجموع غیرقطبی باشد. درک قطبیت مولکولی مهم است زیرا قطبیت یک مولکول بر نحوه ی تعامل آن با میدان های الکتریکی، جهت گیری در کنار مولکول های دیگر و چگونگی حل شدن آن در حلال ها تأثیر می گذارد.
در زمینه ی تحلیل دقیق مولکول های دوقطبی، بررسی ساختار پیوندی و شکل مولکولی اسید کلریدریک نمونه ای روشن از این مفهوم است؛ زیرا اختلاف الکترونگاتیویته ی زیاد بین هیدروژن و کلر موجب ایجاد پیوندی قویاً قطبی می شود و این مولکول را به یکی از مثال های کلاسیک قطبیت تبدیل می کند. قطبیت نقش کلیدی در تعیین خواص فیزیکی و فعالیت شیمیایی مواد دارد و مطالعه آن در مورد HCl، درک عمیق تری از رفتار مولکول های قطبی ارائه می دهد..
نقش الکترونگاتیویته در پیوندهای شیمیایی
مفهوم الکترونگاتیویته توضیح می دهد چرا برخی اتم ها الکترون های مشترک در یک پیوند شیمیایی را قوی تر به سمت خود جذب می کنند. الکترونگاتیویته در واقع میزان تمایل یک اتم برای کشیدن الکترون های پیوندی به سوی خود هنگام اتصال به اتم دیگر است. برای هر عنصر عددی به عنوان الکترونگاتیویته، معمولا بر پایه مقیاس پاولینگ، تعیین شده تا بتوان قدرت جذب الکترون عناصر مختلف را با هم مقایسه کرد.
در این مقیاس، فلوئور با مقدار تقریبی 4.0 بالاترین الکترونگاتیویته را دارد، در حالی که عناصری مانند سزیم یا فرانسیوم با مقادیری نزدیک به 0.7 در پایین ترین سطح قرار می گیرند. به طور کلی، نافلزها نسبت به فلزها الکترونگاتیویته بیشتری دارند و تمایل بالاتری به جذب الکترون نشان می دهند.
وقتی دو اتم با الکترونگاتیویته متفاوت پیوند تشکیل می دهند، الکترون های مشترک به طور مساوی بین آن ها تقسیم نمی شوند. اتم الکترونگاتیوتر بار منفی جزئی می گیرد و اتم دیگر بار مثبت جزئی پیدا می کند. هرچه اختلاف الکترونگاتیویته بیشتر باشد، پیوند قطبی تر خواهد بود.
اگر این اختلاف بسیار بزرگ شود، الکترون تقریبا به طور کامل به یک اتم منتقل می شود و پیوند یونی شکل می گیرد. بنابراین الکترونگاتیویته یک طیف پیوسته از پیوند کووالانسی غیرقطبی تا پیوند یونی را توضیح می دهد.
الکترونگاتیویته هیدروژن و کلر
هیدروژن و کلر از نظر الکترونگاتیویته اختلاف قابل توجهی دارند و همین تفاوت، علت اصلی قطبی بودن پیوند H–Cl به شمار می رود. بر اساس مقیاس پاولینگ، الکترونگاتیویته هیدروژن حدود 2.2 و الکترونگاتیویته کلر نزدیک به 3.2 است. این اختلاف نشان می دهد که کلر توان بسیار بیشتری برای جذب الکترون ها نسبت به هیدروژن دارد.
در پیوند H–Cl، اتم کلر الکترون های مشترک را بیشتر به سمت خود می کشد و در نتیجه بار منفی جزئی می گیرد. در مقابل، اتم هیدروژن که الکترون کمتری در اطراف خود دارد، دارای بار مثبت جزئی می شود. اختلاف الکترونگاتیویته میان این دو عنصر حدود 0.9 تا 1.0 برآورد می شود.
این مقدار اختلاف آن قدر زیاد نیست که پیوند را کاملا یونی کند، اما برای ایجاد یک پیوند کووالانسی قطبی کاملا کافی است. به همین دلیل پیوند H–Cl در مقایسه با بسیاری از پیوندهای هیدروژن، قطبیت بالایی دارد، هرچند شدت آن به اندازه پیوند H–F نیست. از آنجا که کلر پس از فلوئور دومین هالوژن با الکترونگاتیویته بالا محسوب می شود، اتصال آن به هیدروژن همواره پیوندی با قطبیت مشخص ایجاد می کند.
چرا مولکول HCl قطبی است
مولکول HCl دارای قطبیت قابل توجهی است، زیرا از دو اتم متفاوت با الکترونگاتیویته نابرابر تشکیل شده است. کشش قوی تر کلر نسبت به الکترون ها باعث می شود این اتم بار منفی جزئی بگیرد، در حالی که هیدروژن اندکی بار مثبت پیدا می کند. همین تفاوت، پایه شکل گیری یک پیوند قطبی در این مولکول است.
از آنجا که HCl تنها شامل یک پیوند قطبی است، کل مولکول ماهیتی قطبی دارد. برخلاف مولکول های چندپیوندی، در HCl هیچ آرایش فضایی وجود ندارد که بتواند این قطبیت را خنثی کند. به همین دلیل، اثر قطبی پیوند به طور کامل در کل مولکول دیده می شود.
در نمایش های ساختاری، این قطبیت معمولا با پیکانی از سمت هیدروژن به سوی کلر یا با نوشتن H⁺–Cl⁻ نشان داده می شود. این دوقطبی دائمی باعث می شود HCl در میدان های الکتریکی جهت گیری کند و با مولکول های قطبی مانند آب برهمکنش شدیدی داشته باشد.
قطبیت HCl در برابر مولکول های غیرقطبی
در مقابل مولکول های قطبی مانند HCl، مولکول های غیرقطبی فاقد جدایش دائمی بار در ساختار خود هستند. برای نمونه، گاز هیدروژن (H₂) و گاز کلر (Cl₂) از دو اتم کاملاً یکسان تشکیل شده اند. در مولکول H₂، هر دو اتم هیدروژن الکترونگاتیویته برابری دارند و الکترون های پیوندی را به صورت مساوی میان خود تقسیم می کنند، بنابراین هیچ بار جزئی در هیچ بخشی از مولکول ایجاد نمی شود.
در مورد Cl₂ نیز وضعیت مشابهی برقرار است. دو اتم کلر با توان یکسان الکترون ها را جذب می کنند و توزیع الکترونی کاملاً یکنواخت باقی می ماند، به طوری که گشتاور دوقطبی شکل نمی گیرد. این مولکول های دو اتمی غیرقطبی محسوب می شوند، زیرا اختلاف الکترونگاتیویته میان اتم های پیوندی آن ها صفر است.
در نتیجه، مولکول هایی مانند H₂ یا Cl₂ نه دارای قطب مثبت هستند و نه قطب منفی. این ترکیبات در میدان الکتریکی جهت گیری مشخصی نشان نمی دهند و تمایل اندکی برای برهمکنش با مولکول های قطبی دارند.
مولکول های غیرقطبی تنها از طریق نیروهای ضعیف لاندن، یعنی دوقطبی های لحظه ای القایی، با یکدیگر برهمکنش می کنند. در مقابل، مولکول های قطبی مانند HCl می توانند جاذبه های دوقطبی–دوقطبی قوی تری برقرار سازند. همین تفاوت در نیروهای بین مولکولی توضیح می دهد که چرا گازهایی مانند کلر و هیدروژن در آب حل پذیری بسیار کمی دارند، اما هیدروژن کلرید به دلیل قطبیت بالا به راحتی در آب حل می شود.
پیوند کووالانسی قطبی در برابر ویژگی یونی در HCl
HCl یک ترکیب کووالانسی قطبی به شمار می آید و نباید آن را کاملاً یونی دانست، با این حال اختلاف الکترونگاتیویته میان هیدروژن و کلر آن قدر قابل توجه است که بخشی از ویژگی های یونی را در پیوند ایجاد می کند. در پیوندهای کاملاً یونی، مانند سدیم کلرید، یک اتم عملاً الکترون ها را به طور کامل در اختیار می گیرد و یون های جداگانه شکل می گیرند.
در مولکول HCl چنین انتقال کاملی رخ نمی دهد. الکترون ها همچنان مشترک هستند، اما این اشتراک به صورت نابرابر انجام می شود و چگالی الکترونی بیشتر به سمت کلر متمایل است. به همین دلیل می توان گفت پیوند H–Cl ترکیبی از خصلت کووالانسی و یونی دارد، هرچند ماهیت کووالانسی آن غالب باقی می ماند.
شیمیدانان برای بیان این موضوع گاهی درصد خصلت یونی پیوند را محاسبه می کنند. برای HCl این مقدار حدود 15 تا 20 درصد برآورد شده است، یعنی بخشی از پیوند به جدایش بار شباهت دارد. با وجود این، HCl در حالت خالص، به ویژه در فاز گاز، به صورت مولکول های مستقل باقی می ماند و ساختار بلوری یونی تشکیل نمی دهد.
گشتاور دوقطبی مولکول HCl
یافته های آزمایشگاهی قطبی بودن مولکول HCl را با اندازه گیری گشتاور دوقطبی آن به خوبی تأیید می کنند. در فاز گاز، مولکول HCl گشتاور دوقطبی حدود 1.08 دبی نشان می دهد. دبی واحد اندازه گیری گشتاور دوقطبی است و هر یک دبی تقریبا برابر با 3.34×10⁻³⁰ کولن متر می باشد. این مقدار بیانگر آن است که الکترون ها بین هیدروژن و کلر به شکل کاملا مساوی تقسیم نشده اند.
اگر پیوند HCl کاملا یونی بود و یک الکترون به طور کامل بین دو اتم جدا می شد، مقدار گشتاور دوقطبی باید بسیار بزرگ تر می بود و به حدود 6 تا 7 دبی می رسید. اختلاف چشمگیر میان مقدار واقعی و مقدار نظری نشان می دهد که پیوند H–Cl عمدتا کووالانسی است و تنها بارهای جزئی در دو سر مولکول وجود دارد.
در مقایسه با سایر هیدروژن هالیدها، گشتاور دوقطبی HCl در محدوده میانی قرار دارد؛ بزرگ تر از HBr و HI، اما کوچک تر از HF. این اندازه گیری ها ثابت می کنند که HCl مولکولی قطبی است، اما پیوند آن یونی خالص محسوب نمی شود.
تأثیر قطبیت مولکولی بر ویژگی های HCl
قطبیت مولکولی به طور مستقیم بر ویژگی های فیزیکی و شیمیایی مواد اثر می گذارد و HCl نیز از این قاعده جدا نیست. چون HCl یک مولکول قطبی است، میان مولکول های آن نیروهای بین مولکولی دوقطبی–دوقطبی برقرار می شود. این نیروها در مقایسه با نیروهای پخش لاندن میان مولکول های غیرقطبی هم جرم، قدرت بیشتری دارند.
به همین دلیل، هیدروژن کلرید نقطه جوش بالاتری نسبت به مولکول های غیرقطبی با جرم مولی مشابه نشان می دهد. برای نمونه، HCl با جرم مولی حدود 36.5 در نزدیکی دمای 85- درجه سانتی گراد می جوشد، در حالی که مولکول غیرقطبی F₂ با جرم مولی نزدیک به 38 در دمای حدود 188- درجه سانتی گراد به جوش می رسد.
قطبیت HCl همچنین باعث می شود این ماده در حلال های قطبی مانند آب به خوبی حل شود. تماس گاز HCl با آب موجب ایجاد جاذبه های قوی میان دوقطبی ها شده و حل شدن سریع را رقم می زند. به همین علت، هیدروژن کلرید در هوای مرطوب دود می کند. در مقابل، گازهای غیرقطبی مانند O₂ یا N₂ در آب حل پذیری کمی دارند. این قطبیت بر واکنش پذیری HCl نیز اثر می گذارد و بسیاری از خواص آن را توضیح می دهد.
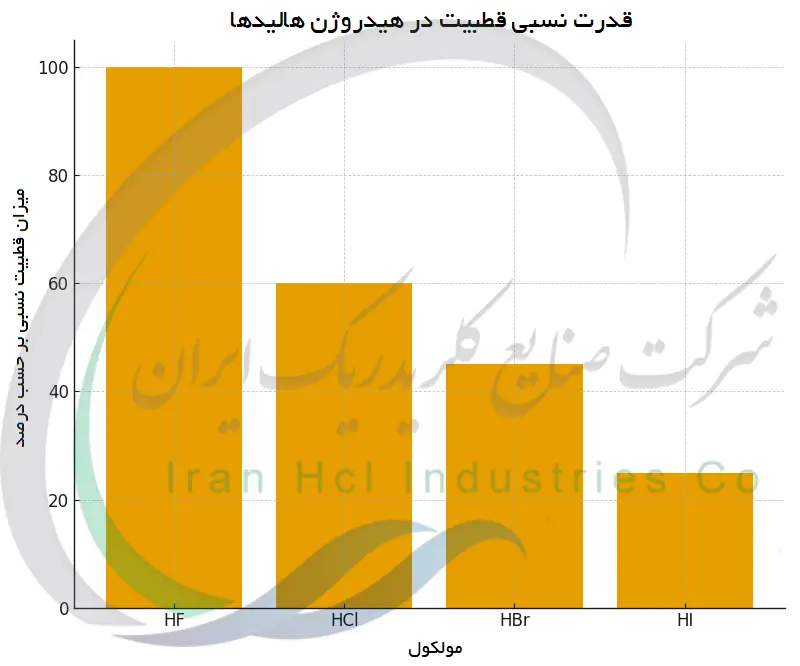
مقایسه قطبیت: هیدروژن هالیدها و مولکول های دیگر
هالیدهای هیدروژن شامل HF، HCl، HBr و HI نمونه های مناسبی برای بررسی و مقایسه قطبیت مولکولی هستند. همه این مواد مولکول های دو اتمی خطی به شمار می آیند که در آن ها یک اتم هیدروژن به یک هالوژن متصل شده است، اما شدت قطبیت پیوند در هرکدام با توجه به الکترونگاتیویته هالوژن تفاوت دارد. فلوئور بالاترین الکترونگاتیویته را دارد، بنابراین پیوند H–F با اختلاف حدود 1.78 بیشترین قطبیت را نشان می دهد.
کلر نسبت به فلوئور الکترونگاتیویته کمتری دارد و در نتیجه در HCl اختلافی در حدود 0.96 ایجاد می شود که پیوندی قطبی اما ضعیف تر از HF به وجود می آورد. در ادامه این روند، برم و ید الکترونگاتیویته پایین تری دارند و به همین دلیل پیوندهای HBr و HI قطبیت کمتری نشان می دهند.
این تغییرات در مقدار گشتاور دوقطبی نیز دیده می شود؛ HF بیشترین مقدار را دارد، HCl در حد میانی قرار می گیرد و HBr و HI مقادیر کمتری نشان می دهند. درصد خصلت یونی نیز از HF به سمت HI کاهش می یابد.
در مقابل، مولکول هایی مانند H₂ یا Cl₂ که از اتم های یکسان ساخته شده اند، کاملا غیرقطبی هستند. همچنین برخی مولکول ها با وجود پیوندهای قطبی، به دلیل تقارن هندسی در مجموع غیرقطبی می شوند؛ CO₂ نمونه ای از این حالت است. در حالی که آب به علت شکل خمیده خود قطبیت بالایی دارد.
| مولکول | الکترونگاتیویته (اتم 1) | الکترونگاتیویته (اتم 2) | اختلاف الکترونگاتیویته | گشتاور دوقطبی (D) |
|---|---|---|---|---|
| H₂ | 2.2 (H) | 2.2 (H) | 0.0 | 0.0 |
| Cl₂ | 3.2 (Cl) | 3.2 (Cl) | 0.0 | 0.0 |
| HF | 2.2 (H) | 4.0 (F) | 1.8 | ~1.8 |
| HCl | 2.2 (H) | 3.2 (Cl) | 0.9 | ~1.1 |
| HBr | 2.2 (H) | 3.0 (Br) | 0.8 | ~0.8 |
| HI | 2.2 (H) | 2.7 (I) | 0.5 | ~0.4 |
| H₂O | 2.2 (H) | 3.4 (O) | 1.2 | ~1.9 |
| CO₂ | 2.6 (C) | 3.4 (O) | 0.9 | 0.0 |
مقیاس ها و مقادیر الکترونگاتیویته
الکترونگاتیویته بر پایه یک مقیاس نسبی سنجیده می شود و در گذر زمان، شیمیدانان روش های گوناگونی برای بیان آن پیشنهاد کرده اند. شناخته شده ترین این روش ها مقیاس پاولینگ است که لینوس پاولینگ آن را در سال 1932 معرفی کرد. در این دیدگاه، الکترونگاتیویته با انرژی پیوند ارتباط دارد و نشان می دهد یک پیوند میان دو اتم متفاوت، مانند H–Cl، تا چه اندازه پایدارتر از میانگین پیوندهای هم نوع آن ها است.
بر اساس این روش، پاولینگ مقدار تقریبی 2.1 را برای هیدروژن و حدود 3.0 را برای کلر در نظر گرفت و فلوئور را با بیشترین مقدار یعنی 4.0 در بالاترین جایگاه قرار داد. در منابع جدیدتر، این اعداد با دقت بیشتری گزارش می شوند؛ برای نمونه، مقدار هیدروژن نزدیک به 2.20 و کلر حدود 3.16 ذکر می شود، هرچند چارچوب کلی مقیاس تغییر نکرده است.
علاوه بر مقیاس پاولینگ، معیارهای دیگری نیز وجود دارد. در مقیاس مولیکن، الکترونگاتیویته از میانگین انرژی یونش و الکترون خواهی محاسبه می شود. مقیاس آلرد–روخو نیز این ویژگی را به بار مؤثر هسته و اندازه اتم پیوند می دهد.
با وجود تفاوت های عددی جزئی، همه این مقیاس ها عناصر را تقریبا به یک ترتیب رتبه بندی می کنند. فلوئور همواره در صدر قرار دارد، اکسیژن، کلر و نیتروژن مقادیر بالایی دارند و فلزاتی مانند سزیم یا فرانسیوم در پایین ترین حد هستند. این مقیاس ها ابزار مناسبی برای مقایسه توان جذب الکترون و پیش بینی قطبیت پیوندها فراهم می کنند.
اختلاف الکترونگاتیویته و مرزهای نوع پیوند
در کتاب های آموزشی شیمی معمولا برای تشخیص نوع پیوند از حدود تقریبی بر پایه اختلاف الکترونگاتیویته استفاده می شود. زمانی که اختلاف الکترونگاتیویته میان دو اتم بسیار کم باشد، که اغلب کمتر از حدود 0.4 در مقیاس پاولینگ در نظر گرفته می شود، پیوند حاصل کووالانسی غیرقطبی محسوب می گردد و الکترون های پیوندی تقریبا به طور مساوی میان دو اتم پخش می شوند. نمونه های رایج این حالت پیوند H–H با اختلاف صفر و پیوند C–H با اختلاف نزدیک به 0.35 هستند که عملا غیرقطبی به حساب می آیند.
اگر اختلاف الکترونگاتیویته در بازه ای میانی قرار گیرد، یعنی حدود 0.4 تا 1.7، پیوند به صورت کووالانسی قطبی توصیف می شود. در این شرایط یک اتم الکترون ها را قوی تر جذب می کند، اما نه به اندازه ای که آن ها را کاملا در اختیار بگیرد، بنابراین بارهای جزئی مثبت و منفی شکل می گیرند. پیوند H–Cl با اختلاف تقریبی 0.96 و پیوندهای O–H در آب با اختلاف حدود 1.24 در این گروه قرار دارند.
وقتی اختلاف الکترونگاتیویته از حدود 1.7 تا 2.0 فراتر می رود، پیوند ماهیتی عمدتا یونی پیدا می کند. در چنین حالتی یک اتم آن قدر الکترونگاتیوتر است که عملا الکترون را از اتم مقابل می گیرد و یون های با بار مخالف تشکیل می شوند، مانند NaCl با اختلاف نزدیک به 2.1.
باید توجه داشت این مرزها قطعی نیستند و گذار از پیوند کووالانسی به یونی به شکل تدریجی رخ می دهد. برخی پیوندها مانند HCl یا HF در ناحیه میانی قرار می گیرند؛ آن ها کووالانسی هستند اما قطبیت قابل توجهی دارند که گاهی به صورت درصدی از خصلت یونی بیان می شود. با این حال، اختلاف الکترونگاتیویته راهنمای مناسبی برای تشخیص کلی نوع پیوند به شمار می آید.
قطبیت HCl در محلول آبی
وقتی هیدروژن کلرید وارد آب می شود، قطبیت بالای آن روند جدا شدن مولکول به یون ها را بسیار آسان می کند. در محیط آبی، HCl مانند یک اسید قوی عمل می کند؛ پیوند H–Cl از هم گسسته می شود، هیدروژن به مولکول آب منتقل شده و یون هیدرونیوم تشکیل می گردد، در حالی که کلر به صورت یون کلرید باقی می ماند.
عامل اصلی این رفتار، قطبیت ذاتی مولکول HCl است. از آنجا که این مولکول از پیش دارای دوقطبی مشخص Hδ⁺–Clδ⁻ می باشد، مولکول های قطبی آب می توانند هر دو سر آن را پایدار کنند. هیدروژن با بار مثبت جزئی به اکسیژن آب که بار منفی نسبی دارد جذب می شود و کلر نیز توسط هیدروژن های آب با قطب مثبت احاطه می گردد.
در عمل، برهمکنش هم زمان تعداد زیادی مولکول آب با HCl باعث می شود مولکول اولیه به اجزای باردار خود تجزیه شود. به همین دلیل اسید هیدروکلریک در آب تقریبا به طور کامل به یون های H₃O⁺ و Cl⁻ تبدیل می گردد.
در مقابل، ترکیباتی با قطبیت کمتر چنین تفکیکی را تجربه نمی کنند. حتی HF با وجود پیوند بسیار قطبی، به دلیل استحکام زیاد پیوند و تشکیل پیوند هیدروژنی قوی، به طور کامل یونیزه نمی شود. در HCl، ترکیب قطبیت مناسب و پیوند نه چندان محکم سبب می شود آب بتواند آن را به راحتی بشکند و رفتار اسیدی قوی ایجاد شود.
روندهای الکترونگاتیویته در جدول تناوبی
الکترونگاتیویته در جدول تناوبی الگوهای مشخص و قابل پیش بینی دارد که به درک رفتار شیمیایی عناصر کمک می کند. در طول هر دوره، یعنی حرکت از چپ به راست جدول، مقدار الکترونگاتیویته معمولا افزایش پیدا می کند. علت این موضوع افزایش بار هسته ای اتم هاست، زیرا با اضافه شدن پروتون ها و بدون افزایش چشمگیر لایه های الکترونی، هسته توان بیشتری برای جذب الکترون های پیوندی خواهد داشت.
به همین دلیل، عناصر واقع در سمت راست هر دوره مانند اکسیژن، کلر یا فلوئور الکترونگاتیویته بالاتری نسبت به فلزاتی مانند سدیم و منیزیم دارند. این تفاوت باعث می شود نافلزها در پیوندهای شیمیایی تمایل بیشتری به کشیدن الکترون ها از خود نشان دهند.
در مقابل، با حرکت از بالا به پایین یک گروه، الکترونگاتیویته کاهش می یابد. بزرگ تر شدن اندازه اتم و افزایش تعداد لایه های الکترونی سبب می شود الکترون های ظرفیت دورتر از هسته قرار بگیرند و اثر پوششی افزایش یابد، در نتیجه قدرت جذب کاهش پیدا می کند.
در گروه هالوژن ها، فلوئور بیشترین مقدار را دارد و پس از آن کلر، برم و ید قرار می گیرند. هیدروژن اگرچه در گروه یک است، اما نافلز محسوب می شود و الکترونگاتیویته آن از فلزات قلیایی بیشتر است. شناخت این روندها امکان پیش بینی قطبیت پیوندها را فراهم می کند و نشان می دهد هرچه فاصله عناصر در جدول بیشتر باشد، پیوند قطبی تر خواهد بود.





بررسی اختلاف الکترونگاتیوی بین اتم های هیدروژن و کلر در اسید کلریدریک و تعریف الکترونگاتیوی در شیمی
بررسی لحظه دوقطبی مولکول اسید کلریدریک (قطبیت مولکولی) و مقایسه با مولکول های دیگر
آشنایی با قابلیت حل شدن اسید کلریدریک در آب ناشی از قطبیت آن و بررسی تولید صنعتی و کاربردهای این ماده
مقایسه قطبیت مولکول اسید کلریدریک با هیدروژن فلوئورید و بررسی نکات ایمنی و خطرهای جدی