فهرست عناوین
- ساختار پیوندی و شکل مولکولی اسید هیدروکلریک
- ترکیب و فرمول مولکولی HCl
- شکل گیری پیوند کووالانسی در اسید هیدروکلریک
- ساختار لوییس و آرایش الکترونی HCl
- قاعده اوکتت و آرایش الکترونی در HCl
- اختلاف الکترونگاتیوی و قطبیت پیوند
- بارهای جزئی و گشتاور دوقطبی HCl
- شکل هندسی مولکول و زاویه پیوند در HCl
- نظریه VSEPR و شکل مولکولی HCl
- طول پیوند و انرژی پیوند H–Cl
- نیروهای بین مولکولی در مولکول های HCl فاقد پیوند هیدروژنی
- در آب: تفکیک و یونش
- هیبریداسیون (همپوشانی اوربیتال های اتمی) در HCl
- مقایسه HCl با سایر هالیدهای هیدروژن
- ارتباط استحکام پیوند با قدرت اسیدی در HCl
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 21-08-1404
تاریخ بروزرسانی مقاله : 21-08-1404
تعداد کلمات : 3500
آدرس مقاله : لینک مقاله
ساختار پیوندی و شکل مولکولی اسید کلریدریک
ساختار پیوندی و شکل مولکولی اسید هیدروکلریک
اسید هیدروکلریک با فرمول HCl یک ماده شیمیایی شناخته شده است که ساختار مولکولی ساده اما مهمی دارد. در حالت خالص به صورت گاز هیدروژن کلرید وجود دارد و هر مولکول آن از یک اتم هیدروژن و یک اتم کلر تشکیل شده است. این اتم ها با تشکیل یک پیوند کووالانسی منفرد یک مولکول دو اتمی را به وجود می آورند.
ساختار پیوندی HCl بسیار قطبی است زیرا اتم کلر الکترون های مشترک را بسیار قوی تر از اتم هیدروژن به سوی خود می کشد. در نتیجه، پیوند H–Cl دارای خصلت نسبتا یونی شده و به مولکول یک گشتاور دوقطبی قابل توجه می دهد. در محلول آبی، همین قطبیت پایه ی رفتار اسید قوی HCl را تشکیل می دهد و سبب می شود این ماده در واکنش های صنعتی و آزمایشگاهی به عنوان یکی از مهم ترین اسیدهای معدنی مورد استفاده قرار گیرد.
استفاده از این ماده در صنایع مختلف شیمیایی و فلزی، اهمیت تأمین آن را دوچندان کرده است. به همین دلیل، خرید اسید کلریدریک تبریز برای واحدهای صنعتی، آزمایشگاه ها و تصفیه خانه ها گزینه ای مطمئن جهت دسترسی به محصولی با خلوص بالا و عملکرد پایدار محسوب می شود. درک ساختار پیوندی و شکل مولکولی اسید هیدروکلریک برای توضیح واکنش پذیری، ویژگی های فیزیکی و نقش آن در فرآیندهای شیمیایی ضروری است.
ترکیب و فرمول مولکولی HCl
در ساده ترین نگاه، اسید هیدروکلریک از پیوند میان یک اتم هیدروژن و یک اتم کلر تشکیل می شود. فرمول مولکولی و جرم مولکولی اسید کلریدریک به شکل HCl و در حدود 36.5 گرم بر مول بیان می شود که نسبت یک به یک هیدروژن و کلر را مشخص می کند. هیدروژن سبک ترین عنصر شناخته شده است (عدد اتمی 1) و کلر در گروه هالوژن ها قرار دارد (عدد اتمی 17). این دو عنصر در کنار هم یک مولکول دو اتمی می سازند، یعنی مولکولی که تنها از دو اتم تشکیل شده است.
این ماده در حالت خالص به صورت گاز هیدروژن کلرید دیده می شود؛ گازی بی رنگ با بویی تند و زننده. اما زمانی که گاز هیدروژن کلرید در آب حل می گردد، اسید هیدروکلریک به وجود می آید که به عنوان یک محلول اسیدی قوی شناخته می شود. مولکول HCl به خودی خود بسیار کوچک و ساده است، اما نوع پیوند و ترکیب آن اساس رفتار شیمیایی این اسید را شکل می دهد. HCl در گروه هالیدهای هیدروژن، یعنی ترکیبات H–X که X یک هالوژن است، قرار می گیرد و همه آن ها ساختار دو اتمی خطی مشابهی دارند.
هر مولکول HCl جرم مولکولی نزدیک به 36.5 گرم بر مول دارد و به دلیل ویژگی خاص پیوندی خود، در فاز گاز به صورت واحدهای جداگانه و نه یک شبکه گسترده حضور دارد. چنین ساختار مولکولی ای باعث فراریت بالای HCl و واکنش پذیری شدید آن در هنگام تماس با هوا یا آب می شود.
شکل گیری پیوند کووالانسی در اسید هیدروکلریک
پیوند موجود در اسید هیدروکلریک از طریق به اشتراک گذاشتن الکترون میان هیدروژن و کلر شکل می گیرد و به همین دلیل در دسته پیوندهای کووالانسی قرار می گیرد. اتم هیدروژن در لایه بیرونی خود تنها یک الکترون والانس دارد، در حالی که اتم کلر دارای هفت الکترون والانس در پوسته ظرفیت خود است. با سهیم شدن یک جفت الکترون، هر دو اتم به وضعیت الکترونی پایدارتر می رسند؛ هیدروژن به حالت پر شدن لایه اول خود با دو الکترون می رسد و کلر نیز لایه ظرفیتش را با هشت الکترون کامل می کند.
این جفت الکترون مشترک، پیوند کووالانسی یگانه H–Cl را به وجود می آورد. شکل گیری چنین پیوندی در HCl نتیجه تمایل اتم ها برای رسیدن به آرایش الکترونی مشابه گازهای نجیب است؛ به گونه ای که برای کلر قانون اوکتت و برای هیدروژن قانون دوگانه برقرار می شود.
برخلاف پیوند یونی که در آن یک اتم ممکن است الکترون خود را به طور کامل به اتم دیگر منتقل کند، در مولکول HCl الکترون ها به صورت مشترک میان دو اتم باقی می مانند و آن ها را به هم متصل نگه می دارند. همین موضوع باعث می شود مولکول HCl به صورت یک واحد مستقل وجود داشته باشد و در شرایط معمول به یون های جداگانه تفکیک نشود.
به علت تفاوت در توان جذب الکترون میان دو اتم، این پیوند به طور مشخص ماهیتی کووالانسی قطبی دارد، اما همچنان در گروه پیوندهای اشتراکی یا کووالانسی قرار می گیرد و نه در دسته پیوندهای یونی.
ساختار لوییس و آرایش الکترونی HCl
ساختار لوییس HCl به صورت تصویری نشان می دهد که الکترون های والانس در این مولکول چگونه کنار هم قرار گرفته اند. در این نمایش، هیدروژن که دارای 1 الکترون والانس است با یک نقطه و کلر که 7 الکترون والانس دارد با هفت نقطه پیرامون آن نمایش داده می شود. زمانی که این دو اتم پیوند برقرار می کنند، یک الکترون از هیدروژن و یک الکترون از کلر با هم جفت شده و یک زوج الکترون مشترک میان H و Cl ایجاد می کنند.
این زوج الکترون پیوندی معمولا در رسم لوییس به شکل یک خط بین دو اتم (H—Cl) نشان داده می شود که بیانگر یک پیوند کووالانسی یگانه است. پس از شکل گیری پیوند، اتم کلر دارای سه جفت الکترون ناپیوندی در اطراف خود باقی می ماند، یعنی شش الکترونی که در پیوند شرکت ندارند، در حالی که هیدروژن هیچ جفت الکترون آزادی ندارد.
در مجموع، هشت الکترون در این ساختار در نظر گرفته شده است که برابر با مجموع الکترون های والانس مولکول HCl می باشد؛ یک الکترون از هیدروژن و هفت الکترون از کلر. در ساختار لوییس، هر دو اتم لایه بیرونی خود را کامل کرده اند: زوج الکترون پیوندی، ظرفیت لایه اول هیدروژن را پر می کند و آرایش اوکتت کلر نیز با یک زوج پیوندی و سه جفت الکترون آزاد تکمیل می شود.
نمایش نقطه ای لوییس نشان می دهد که HCl دارای آرایش پیوندی پایدار است و هیچ بار رسمی روی هیچ یک از اتم ها وجود ندارد؛ موضوعی که بیانگر یک مولکول خنثی و متعادل می باشد.
قاعده اوکتت و آرایش الکترونی در HCl
پایداری مولکول HCl را می توان با توجه به قاعده اوکتت و آرایش های الکترونی ایجاد شده توضیح داد. با شکل گیری پیوند H–Cl، هر یک از اتم ها به آرایش الکترونی شبیه گازهای نجیب می رسند. هیدروژن که در حالت عادی پیکربندی الکترونی 1s¹ دارد، از راه پیوند به الکترون دوم دست پیدا می کند و در عمل به آرایش هلیوم یعنی 1s² می رسد. کلر نیز که در وضعیت پایه دارای پیکربندی [Ne]3s²3p⁵ است، از طریق پیوند اشتراکی یک الکترون اضافه به دست می آورد و زیرلایه 3p خود را به صورت [Ne]3s²3p⁶ کامل می کند که همان آرایش الکترونی آرگون محسوب می شود.
تحقق قاعده اوکتت برای کلر، یعنی داشتن هشت الکترون در لایه ظرفیت، و قاعده دوگانه برای هیدروژن، یعنی وجود دو الکترون در لایه بیرونی، مولکول HCl را به شکل قابل توجهی پایدار می کند. هر اتم با تکمیل لایه ظرفیت خود به سطح انرژی پایین تری می رسد و همین موضوع نیروی محرک اصلی تشکیل پیوند به شمار می آید.
نتیجه این فرایند آن است که هیچ یک از اتم ها دارای بار رسمی نیستند و مولکول کمترین فشار الکترونی درونی را تجربه می کند. از آنجا که هر دو اتم به تعداد الکترون مطلوب خود رسیده اند، جفت الکترون پیوندی تمایل اندکی به جدا شدن در شرایط معمول دارد و این مسئله به پایداری HCl کمک می کند. مولکول HCl نمونه ای کلاسیک است که نشان می دهد اتم ها چگونه با به اشتراک گذاشتن الکترون ها قاعده اوکتت را برآورده کرده و در نهایت ترکیبی خنثی و پایدار ایجاد می کنند.
اختلاف الکترونگاتیوی و قطبیت پیوند
تفاوت الکترونگاتیوی میان هیدروژن و کلر به طور مستقیم باعث ایجاد قطبیت در پیوند H–Cl می شود. الکترونگاتیوی معیاری برای توان هر اتم در جذب الکترون های پیوندی است و کلر در این مقیاس مقدار بالاتری نسبت به هیدروژن دارد. به همین دلیل، در مولکول HCl الکترون های مشترک تمایل بیشتری به سمت اتم کلر پیدا می کنند.
در نتیجه این جابه جایی، چگالی الکترونی اطراف هیدروژن کاهش می یابد و الکترون ها به طور مساوی میان دو اتم تقسیم نمی شوند. به همین علت، پیوند ایجاد شده از نوع کووالانسی قطبی است و نه یک پیوند کاملا غیرقطبی. این عدم تعادل، ماهیت پیوند را مشخص می کند.
بخش مربوط به کلر در این پیوند دارای بار جزئی منفی و ناحیه هیدروژن دارای بار جزئی مثبت است. اختلاف الکترونگاتیوی حدود 0.9 در مقیاس پاولینگ برای ایجاد چنین قطبیتی کافی است، اما به اندازه ای نیست که پیوند یونی شکل بگیرد. به همین دلیل مولکول HCl ساختاری قطبی دارد که بر خواص آن تاثیر می گذارد.
بارهای جزئی و گشتاور دوقطبی HCl
به علت جدا شدن بارهای الکتریکی در پیوند H–Cl، مولکول اسید هیدروکلریک دارای گشتاور دوقطبی مشخص و قابل اندازه گیری است. گشتاور دوقطبی یک کمیت برداری به شمار می رود که میزان جدایی بارهای مثبت و منفی در یک مولکول و فاصله آن ها از یکدیگر را نشان می دهد. در مورد HCl، مقدار این گشتاور نسبتا زیاد است و حدود 1.08 دبی اندازه گیری می شود که واحد رایج برای بیان دوقطبی الکتریکی است.
این مقدار بیانگر آن است که بخش مربوط به اتم کلر دارای بار جزئی منفی بوده و در مقابل، سمت مربوط به هیدروژن بار جزئی مثبت دارد. هرچند گشتاور دوقطبی HCl کمی کمتر از مولکول هایی مانند آب یا HF است، اما برای یک مولکول دو اتمی همچنان عدد بزرگی محسوب می شود و ماهیت قطبی HCl را به خوبی نشان می دهد.
وجود این دوقطبی قوی سبب می شود مولکول های HCl در میدان های الکتریکی جهت گیری پیدا کنند و با مولکول های قطبی دیگر برهم کنش شدیدی داشته باشند. برای نمونه، گشتاور دوقطبی بالای HCl نقش مهمی در انحلال پذیری بالای آن در آب دارد، زیرا بخش های با بار مخالف مولکول HCl به مولکول های قطبی آب جذب می شوند.
در مجموع، جدایی واضح بار در ساختار مولکولی HCl یکی از ویژگی های اساسی پیوند آن است و رفتار این ماده را در بسیاری از فرآیندهای شیمیایی تحت تاثیر قرار می دهد.
شکل هندسی مولکول و زاویه پیوند در HCl
با توجه به اینکه مولکول HCl تنها از دو اتم تشکیل شده که با یک پیوند یگانه به یکدیگر متصل هستند، هندسه مولکولی آن ساده ترین حالت ممکن را دارد و به صورت خطی تعریف می شود. در یک مولکول دو اتمی مانند HCl، عملا زاویه پیوندی برای بررسی وجود ندارد و فقط یک خط مستقیم مطرح است که اتم های هیدروژن و کلر را به هم وصل می کند.
در واقع، مولکول HCl شکلی خطی ایجاد می کند که پیوند H–Cl همان خط اصلی آن است. زاویه پیوند در این مولکول برابر با 180 درجه در نظر گرفته می شود که صرفا بیانگر قرار گرفتن دو اتم دقیقا روبه روی یکدیگر و حضور پیوند میان آن هاست.
برخلاف مولکول های پیچیده تر که می توانند ساختارهایی مانند خمیده، مثلثی یا چهاروجهی داشته باشند، مولکولی که فقط شامل دو اتم است امکان انتخاب شکل دیگری ندارد و طبق تعریف باید خطی باشد. در HCl هیچ اتم مرکزی وجود ندارد که چند پیوند پیرامون آن آرایش یابد، بلکه هیدروژن و کلر تنها همسایه یکدیگر محسوب می شوند.
این ساختار ساده به این معناست که آرایش فضایی HCl تنها یک محور مستقیم دارد و هر مولکول HCl در فضا در اصل یک زنجیره خطی متشکل از دو اتم است. شکل خطی این مولکول مستقل از حالت فیزیکی آن، چه گاز، چه مایع یا محلول، ثابت باقی می ماند، زیرا این ویژگی ذاتی مولکول های دو اتمی است.
نظریه VSEPR و شکل مولکولی HCl
با اینکه خطی بودن مولکول HCl به دلیل داشتن تنها دو اتم کاملا بدیهی به نظر می رسد، بررسی آن با استفاده از نظریه VSEPR یا همان نظریه دافعه زوج الکترون های لایه ظرفیت نیز نکات آموزشی مهمی دارد. طبق این نظریه، می توان اتم کلر را به عنوان اتم مرکزی در نظر گرفت که زوج های الکترونی اطراف آن قرار گرفته اند.
در مولکول HCl، اتم کلر چهار ناحیه چگالی الکترونی پیرامون خود دارد؛ یک جفت الکترون پیوندی که با اتم هیدروژن مشترک است و سه جفت الکترون غیر پیوندی یا تنها. بر اساس نظریه VSEPR، این چهار ناحیه الکترونی تلاش می کنند تا بیشترین فاصله ممکن را از یکدیگر داشته باشند و در نتیجه آرایشی چهاروجهی با زاویه تقریبی 109.5 درجه بین زوج ها شکل می گیرد.
این وضعیت را می توان به صورت AX₁E₃ نمایش داد، به طوری که A نشان دهنده اتم مرکزی کلر، X₁ بیانگر یک اتم هیدروژن متصل و E₃ معرف سه جفت الکترون غیر پیوندی روی کلر است. نظریه VSEPR چنین آرایش چهاروجهی را برای کل مجموعه زوج های الکترونی پیش بینی می کند.
اما هنگام تعیین شکل واقعی مولکول، تنها موقعیت اتم ها در نظر گرفته می شود و جفت های الکترونی غیر اتمی نقشی در شکل هندسی مولکول ندارند. از آنجا که فقط یک اتم به اتم مرکزی متصل است، شکل مولکولی در نهایت خطی خواهد بود.
به بیان ساده تر، پیوند H–Cl یکی از بازوهای آرایش چهاروجهی زوج های الکترونی محسوب می شود و چون اتم دیگری برای ایجاد پیوند یا زاویه اضافی وجود ندارد، مولکول HCl به صورت خطی دیده می شود.
طول پیوند و انرژی پیوند H–Cl
پیوند یگانه میان هیدروژن و کلر در مولکول HCl دارای طول و استحکام مشخصی است که به ویژگی های این دو اتم مربوط می شود. طول پیوند H–Cl که فاصله میان هسته های هیدروژن و کلر را نشان می دهد، حدود 1.27 آنگستروم یا 1.27×10⁻¹⁰ متر اندازه گیری شده است. این مقدار از طول پیوند H–F بیشتر است، زیرا اتم کلر از فلوئور بزرگ تر می باشد، اما از پیوندهای H–Br و H–I کوتاه تر است و این روند نشان می دهد با افزایش اندازه اتم هالوژن، طول پیوند نیز افزایش پیدا می کند.
از نظر قدرت پیوند، H–Cl در رده پیوندهای کووالانسی منفرد نسبتا قوی قرار دارد. انرژی لازم برای گسستن این پیوند حدود 430 کیلوژول بر مول است که بیانگر اتصال محکم میان دو اتم می باشد. برای مقایسه، پیوند H–F انرژی بالاتری در حدود 565 کیلوژول بر مول دارد، در حالی که پیوندهای H–Br و H–I ضعیف تر هستند و به ترتیب انرژی هایی نزدیک به 360 و 300 کیلوژول بر مول دارند.
انرژی پیوند نسبتا بالای HCl نشان می دهد که شکستن این مولکول نیازمند صرف انرژی قابل توجهی است، هرچند به دلیل قطبی بودن پیوند، در شرایط مناسب می تواند گسسته شود. طول و استحکام پیوند HCl از عوامل مهمی به شمار می آیند که بر فرکانس ارتعاشی، میزان واکنش پذیری و تغییرات انرژی در واکنش های مرتبط با HCl اثر می گذارند.
نیروهای بین مولکولی در مولکول های HCl فاقد پیوند هیدروژنی
در حالت های مایع یا جامد و همچنین هنگام حل شدن در حلال ها، مولکول های HCl از راه نیروهای بین مولکولی با یکدیگر برهم کنش پیدا می کنند. نیروی اصلی میان آن ها جاذبه دوقطبی–دوقطبی است، زیرا HCl یک مولکول قطبی به شمار می رود که در آن اتم هیدروژن دارای بار جزئی مثبت و اتم کلر دارای بار جزئی منفی می باشد. به همین دلیل، بخش مثبت هر مولکول به بخش منفی مولکول دیگر جذب می شود.
علاوه بر این، نیروهای لاندن یا نیروهای پراکندگی نیز میان مولکول ها حضور دارند، چرا که ابر الکترونی بزرگ اتم کلر می تواند دچار نوسان شود و دوقطبی های موقتی ایجاد کند. با این حال، اسید هیدروکلریک پیوند هیدروژنی تشکیل نمی دهد، زیرا کلر در مقایسه با فلوئور، اکسیژن یا نیتروژن اندازه بزرگ تری دارد و پیوند H–Cl از قطبیت کافی برای ایجاد چنین پیوندی برخوردار نیست.
در نتیجه، نقطه جوش HCl که حدود ° C – 85 است، به مراتب پایین تر از HF می باشد و این ماده در دمای اتاق به شکل گاز دیده می شود. ضعیف بودن نیروهای دوقطبی و پراکندگی باعث می شود مولکول های HCl به راحتی از یکدیگر جدا شوند و هنگام تماس با آب به سرعت در آن حل گردند.
در آب: تفکیک و یونش
زمانی که گاز هیدروژن کلرید وارد آب می شود، به طور کامل به یون ها تجزیه شده و محلولی را به وجود می آورد که با نام اسید هیدروکلریک شناخته می شود. HCl یک اسید قوی به حساب می آید؛ یعنی تقریبا به صورت کامل و نزدیک به صد درصد در آب یونیزه می گردد.
در عمل، هر مولکول HCl که با آب تماس پیدا می کند، به یک یون هیدروژن و یک یون کلرید تبدیل می شود. یون هیدروژن بلافاصله به مولکول آب متصل شده و یون هیدرونیوم را تشکیل می دهد، بنابراین واکنش کلی را می توان به صورت HCl + H₂O → H₃O⁺ + Cl⁻ نمایش داد.
در محلول آبی، عملا مولکول سالمی از HCl باقی نمی ماند و محیط شامل یون های هیدرونیوم و کلرید است که آزادانه میان مولکول های آب حرکت می کنند. این تفکیک کامل به دلیل قطبیت بالای پیوند H–Cl و پایداری یون های آب پوشیده رخ می دهد.
مولکول های قطبی آب اطراف یون ها جمع شده و آن ها را پایدار می سازند و مولکول اولیه را از هم جدا می کنند. چون پیوند H–Cl از پیش قطبی و چندان قوی نیست، آب می تواند بر آن غلبه کرده و اتم ها را به یون تبدیل کند.
نتیجه این فرایند آن است که اسید هیدروکلریک رفتار اسیدی بسیار شدیدی نشان می دهد و به آسانی پروتون خود را به مواد دیگر می بخشد.
هیبریداسیون (همپوشانی اوربیتال های اتمی) در HCl
در مولکول HCl، هیبریداسیون اوربیتال ها نقش تعیین کننده ای در ایجاد پیوند ندارد. پیوند H–Cl از طریق همپوشانی مستقیم اوربیتال 1s هیدروژن با یکی از اوربیتال های اتمی کلر شکل می گیرد. در لایه ظرفیت کلر با آرایش 3s²3p⁵، یک الکترون جفت نشده در یکی از اوربیتال های 3p وجود دارد که با الکترون اوربیتال 1s هیدروژن همپوشانی کرده و یک پیوند سیگما ایجاد می کند.
سایر الکترون های والانس کلر به صورت سه جفت الکترون تنها در اوربیتال های 3s و 3p باقی می مانند. از آنجایی که کلر در مولکول HCl تنها یک پیوند تشکیل می دهد، نیازی به مخلوط شدن اوربیتال ها مانند شرایطی که چند پیوند در جهات مختلف وجود دارد، احساس نمی شود.
در واقع، پیوند در HCl بدون استفاده از اوربیتال های هیبرید sp³ نیز به خوبی قابل توضیح است. همپوشانی یک اوربیتال 3p هیبرید نشده کلر با اوربیتال 1s هیدروژن برای تشکیل پیوند سیگما کافی است. برخی منابع آموزشی به صورت رسمی از هیبریداسیون sp³ برای کلر یاد می کنند، اما این بیشتر یک بیان نظری است. نتیجه نهایی، یک پیوند کووالانسی و سه جفت الکترون تنها روی کلر خواهد بود.
مقایسه HCl با سایر هالیدهای هیدروژن
اسید هیدروکلریک یکی از اعضای شناخته شده خانواده هالیدهای هیدروژن است و در کنار HF، HBr و HI قرار می گیرد که از نظر نوع پیوند و ویژگی های فیزیکی و شیمیایی با یکدیگر مقایسه می شوند. با حرکت در گروه هالوژن ها از بالا به پایین، طول پیوند H–X افزایش پیدا می کند؛ به طوری که این مقدار از حدود 0.92 آنگستروم در HF آغاز شده و تا حدود 1.61 آنگستروم در HI می رسد.
هم زمان با افزایش طول پیوند، انرژی پیوند کاهش می یابد. برای مثال، انرژی پیوند در HF حدود 565 کیلوژول بر مول است، در حالی که در HI به حدود 299 کیلوژول بر مول می رسد، یعنی شکستن پیوند در ترکیبات سنگین تر ساده تر انجام می شود.
از نظر قطبیت، HF بیشترین گشتاور دوقطبی را دارد، HCl در حد میانی قرار می گیرد و HI کمترین مقدار را نشان می دهد. تنها HF قادر به تشکیل پیوند هیدروژنی قوی است و به همین دلیل نقطه جوش بالاتری دارد. از دید اسیدیته نیز، HF اسیدی ضعیف محسوب می شود، اما HCl، HBr و HI همگی اسیدهای قوی هستند و در آب تقریبا به طور کامل یونیزه می شوند.
| خاصیت | HF | HCl | HBr | HI |
|---|---|---|---|---|
| جرم مولی (g/mol) | 20.0 | 36.5 | 80.9 | 127.9 |
| الکترونگاتیوی (پاولینگ) | 4.0 | 3.0 | 2.8 | 2.5 |
| طول پیوند (Å) | 0.92 | 1.27 | 1.41 | 1.61 |
| انرژی پیوند (kJ/mol) | 565 | 431 | 366 | 299 |
| گشتاور دوقطبی (D) | 1.8 | 1.1 | 0.8 | 0.4 |
| نقطه جوش (°C) | 19.5 | –85 | –66 | –35 |
| قدرت اسیدی (pKa) | 3.2 | –7 | –9 | –10 |
ارتباط استحکام پیوند با قدرت اسیدی در HCl
میان استحکام پیوند H–Cl در اسید هیدروکلریک و رفتار آن به عنوان یک اسید قوی ارتباط روشنی وجود دارد. به طور کلی، زمانی یک ماده خاصیت اسیدی بالایی دارد که پیوند آن با هیدروژن به راحتی شکسته شود و امکان آزاد شدن یون H⁺ فراهم گردد. در مولکول HCl، پیوند نه آن قدر ضعیف است که مولکول ناپایدار باشد و نه آن قدر محکم که در آب مقاومت کند.
انرژی لازم برای گسستن پیوند H–Cl حدود 430 کیلوژول بر مول است که در مقایسه با HF با انرژی حدود 565 کیلوژول بر مول کمتر می باشد. این تفاوت نشان می دهد آب ساده تر می تواند بر پیوند H–Cl غلبه کرده و آن را بشکند.
وقتی HCl در آب حل می شود، مولکول های قطبی آب یون های H⁺ و Cl⁻ را پایدار می کنند و جدایی کامل رخ می دهد. در مقابل، پیوند بسیار قوی H–F و پایداری کمتر یون فلوئورید باعث می شود HF به سختی تفکیک شود. همچنین یون کلرید به دلیل اندازه بزرگ تر، پایدارتر است. در نتیجه، پیوند ضعیف تر و آنیون پایدارتر، HCl را به نمونه ای روشن از یک اسید قوی تبدیل کرده است.
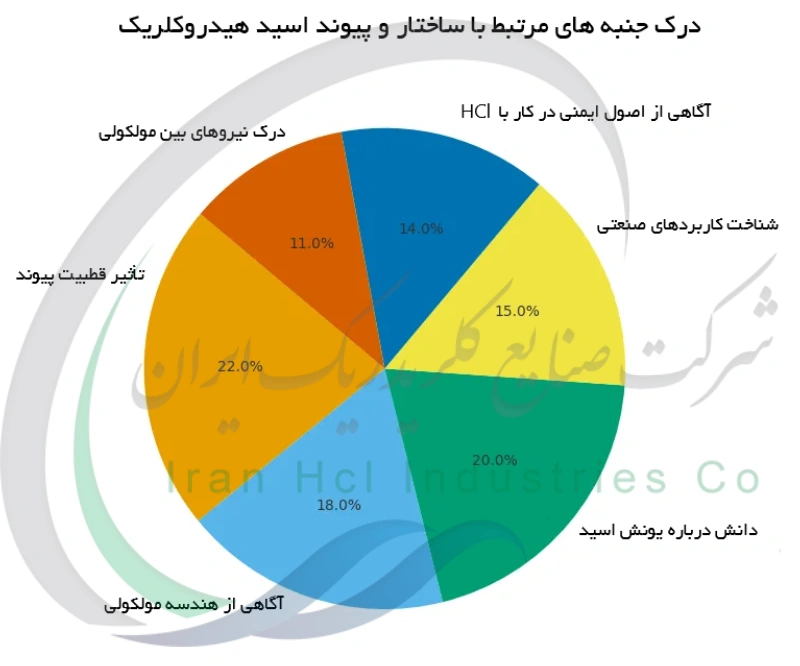





نوع پیوند (کووالانسی قطبی) در مولکول اسید کلریدریک و مقایسه آن با ترکیبات غیرقطبی و یونی
بررسی شکل هندسی مولکول اسید کلریدریک و زاویه پیوند ، با توجه به ماهیت دو اتمی آن
بررسی درک مفهوم طول پیوند در اسید کلریدریک و نحوه اندازه گیری آن
درک قطبیت پیوند و مقایسه قطبیت پیوند اسید کلریدریک با مولکول های مشابه