فهرست عناوین
- مقدمه
- درک مفهوم طول پیوند در مولکول ها
- پیوند H–Cl: یک پیوند کووالانسی قطبی
- تفاوت الکترونگاتیوی و طول پیوند در HCl
- تاثیر اندازه اتم بر طول پیوند HCl
- طول پیوند تعادلی HCl مقدار و واحدها
- مقایسه طول پیوند HCl با سایر مولکول های دو اتمی
- روش های اندازه گیری طول پیوند مولکولی
- طیف سنجی چرخشی و تعیین طول پیوند
- طیف سنجی ارتعاشی و تحلیل طول پیوند
- روش های پراش برای اندازه گیری طول پیوند
- تاثیر حرکت ارتعاشی بر طول پیوند
- تاثیر جایگزینی ایزوتوپی DCl در مقابل HCl بر طول پیوند
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 26-09-1404
تاریخ بروزرسانی مقاله : 26-09-1404
تعداد کلمات : 3000
آدرس مقاله : لینک مقاله
طول پیوند در اسید کلریدریک و نحوه اندازه گیری آن

مقدمه
هیدروژن کلرید (HCl) یک مولکول دو اتمی با یک پیوند H–Cl هستند. در مورد اسید هیدروکلریک محلول آبی HCl، منظور از طول پیوند فاصله بین اتم های هیدروژن و کلر در مولکول HCl است. طول پیوند یک مفهوم بنیادی در شیمی است که نشان دهنده فاصله تعادلی است که در آن نیروهای جاذبه و دافعه بین اتم ها با هم به تعادل می رسند. درک طول پیوند در اسید هیدروکلریک مهم است زیرا با پایداری، واکنش پذیری و بسیاری از خواص فیزیکی مولکول ارتباط دارد.
این ویژگی های ساختاری در مشخصات فنی و کیفی محصولاتی مانند خرید اسید کلریدریک کلران سمنان بشکه 220 لیتری نیز اهمیت بالایی دارند، زیرا رفتار شیمیایی اسید مستقیما به ساختار مولکولی آن وابسته است. در این مقاله بررسی می کنیم که طول پیوند H–Cl چقدر است، چه عواملی بر آن تاثیر می گذارند و روش های اندازه گیری دقیق آن کدامند. با بررسی طول پیوند اسید هیدروکلریک از دیدگاه های گوناگون، درک عمیق تری از پیوند های شیمیایی و ساختار مولکولی به دست می آوریم.
درک مفهوم طول پیوند در مولکول ها
در هر مولکول، طول پیوند به عنوان فاصله بین هسته های دو اتم متصل در حالت تعادلی تعریف می شود. در این فاصله نیروهای جاذبه (مانند کشش بین هسته هر اتم و الکترون های مشترک) دقیقاً با نیروهای دافعه (مانند رانش بین دو هسته مثبت) موازنه می شوند. نتیجه یک پیوند پایدار با طول مشخص است. طول پیوند معمولاً با واحد آنگستروم (Å) یا پیکومتر (pm) بیان می شود (۱ آنگستروم = ۱۰۰ پیکومتر = ۱×۱۰^–۱۰ متر).
به طور کلی عوامل متعددی می توانند بر طول پیوند تاثیر بگذارند: برای مثال، پیوند های قوی تر (با مرتبه پیوند بالاتر، مانند پیوند دوگانه) معمولاً کوتاه تر از پیوند های یگانه هستند و اتم های کوچکتر پیوندهای کوتاه تری نسبت به اتم های بزرگ تر ایجاد می کنند. این مفاهیم مستقیما با شکل هندسی مولکول اسید کلریدریک و زاویه پیوند در آن ارتباط دارند و در توصیف ساختار فضایی مولکول HCl نقش تعیین کننده ای ایفا می کنند. بنابراین طول پیوند یک توصیف مهم از شکل هندسی مولکول و استحکام پیوند شیمیایی در مولکول ها است.
پیوند H–Cl: یک پیوند کووالانسی قطبی
هیدروژن و کلر در مولکول HCl با یک پیوند یگانه کووالانسی به یکدیگر وصل شده اند؛ پیوندی که به شکل محسوسی خاصیت قطبی دارد. علت این موضوع به تفاوت توانایی این دو اتم در جذب الکترون برمی گردد، به طوری که کلر نسبت به هیدروژن قدرت بیشتری در کشیدن الکترون های مشترک پیوند به سمت خود دارد.
در نتیجه این نابرابری، الکترون ها بیشتر در اطراف اتم کلر متمرکز می شوند و همین موضوع باعث می شود کلر دارای بار جزئی منفی (δ-) و هیدروژن دارای بار جزئی مثبت (δ+) باشد. به همین دلیل، مولکول HCl به عنوان یک مولکول قطبی شناخته می شود و رفتار آن با مولکول های غیرقطبی تفاوت دارد.
این قطبیت نقش مهمی در ویژگی های فیزیکی و شیمیایی HCl ایفا می کند. برای مثال، گشتاور دوقطبی آن که حدود ۱٫۱ دبی است و همچنین واکنش آن در میدان های الکتریکی، مستقیماً تحت تاثیر همین توزیع نامتقارن بار قرار دارند.
از طرف دیگر، ماهیت قطبی پیوند H–Cl به استحکام آن نیز کمک می کند. نیروی جاذبه الکترواستاتیکی بین هیدروژن با بار جزئی مثبت و کلر با بار جزئی منفی، در کنار پیوند کووالانسی عمل کرده و باعث افزایش قدرت پیوند و تاثیر نسبی بر طول آن می شود. به همین دلیل، پیوند H–Cl هرچند کووالانسی است، اما به واسطه این قطبیت، ویژگی های یونی جزئی هم دارد و برای یک پیوند یگانه بین این دو اتم، پیوندی نسبتاً قوی و پایدار به شمار می آید.
تفاوت الکترونگاتیوی و طول پیوند در HCl
اختلاف الکترونگاتیوی میان هیدروژن و کلر نقش مهمی در نوع پیوند HCl دارد. در مقیاس پاولینگ، کلر عدد بالاتری نسبت به هیدروژن دارد و همین تفاوت باعث می شود الکترون های پیوندی بیشتر به سمت کلر کشیده شوند. این وضعیت باعث می شود پیوند H–Cl کاملاً خنثی نباشد و بخشی از ویژگی های پیوند یونی را نیز در خود داشته باشد.
این حالت یونی جزئی به این معناست که نیروی جاذبه میان دو اتم قوی تر از یک پیوند کاملاً کووالانسی ساده است. در نتیجه، اتصال میان هیدروژن و کلر استحکام بیشتری پیدا می کند و پایداری پیوند افزایش می یابد. همین عامل سبب می شود رفتار این مولکول با بسیاری از ترکیبات مشابه تفاوت داشته باشد.
در نگاه اول ممکن است تصور شود اختلاف بیشتر الکترونگاتیوی همیشه باعث نزدیک تر شدن اتم ها می شود. بررسی هیدروژن هالیدها نشان می دهد که پیوند H–F به دلیل اختلاف بیشتر، کوتاه تر و قوی تر است. در HCl نیز این اختلاف قابل توجه باعث می شود طول پیوند کمی کوتاه تر از مقدار پیش بینی شده صرفاً بر اساس اندازه اتم ها باشد. این موضوع نشان می دهد توزیع بار و قطبیت چگونه می توانند شکل و هندسه پیوند را تغییر دهند.
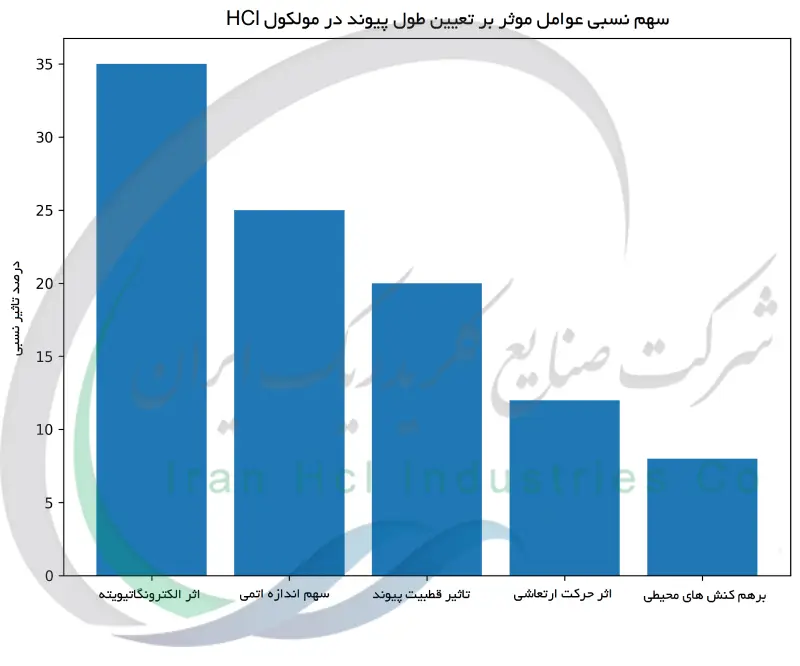
تاثیر اندازه اتم بر طول پیوند HCl
علاوه بر قطبیت، اندازه اتم ها نیز نقش مهمی در تعیین طول پیوند دارند. هیدروژن اتمی بسیار کوچک است، در حالی که کلر در مقایسه با آن اندازه بزرگ تری دارد. شعاع کووالانسی هیدروژن حدود سی تا سی و هفت پیکومتر برآورد می شود و برای کلر عددی نزدیک به نود و نه پیکومتر گزارش شده است. اگر تنها این اعداد کنار هم قرار گیرند، طول پیوند H–Cl چیزی حدود صد و سی تا صد و سی و شش پیکومتر پیش بینی می شود.
اما اندازه گیری های واقعی عددی کمی کمتر، نزدیک به صد و بیست و هفت پیکومتر را نشان می دهند. این اختلاف کوچک بیانگر آن است که نیروی پیوند باعث می شود دو اتم کمی بیش از انتظار ساده به هم نزدیک شوند. بنابراین فقط اندازه اتم ها تعیین کننده فاصله نهایی نیست و عوامل دیگری دخالت دارند.
به طور کلی هرچه اتم بزرگ تر باشد، ابر الکترونی آن گسترده تر است و پیوندی بلندتر شکل می گیرد، زیرا الکترون ها فاصله بیشتری از هسته دارند. در هیدروژن هالیدها، با حرکت از کلر به برم و ید، طول پیوند در HBr و HI افزایش می کند.
طول پیوند تعادلی HCl مقدار و واحدها
طول پیوند در مولکول گازی اسید هیدروکلریک، یا همان HCl، حدود ۱٫۲۷ آنگستروم است که معادل ۱۲۷ پیکومتر به حساب می آید. این عدد فاصله تعادلی میان هسته های هیدروژن و کلر را نشان می دهد؛ فاصله ای که معمولاً با نماد rₑ شناخته می شود و بیانگر حالت پایدار مولکول است. چنین فاصله کوتاهی نشان می دهد که اتم ها در یک پیوند شیمیایی تا چه حد به هم نزدیک می شوند.
اگر این مقدار را به واحد متر تبدیل کنیم، به عددی در حدود ۱٫۲۷×۱۰⁻¹⁰ متر می رسیم. این مقیاس بسیار کوچک کمک می کند درک کنیم چرا برای توصیف ساختارهای اتمی از واحدهای خاصی استفاده می شود. اندازه گیری این فاصله زمانی انجام می گیرد که مولکول در کمترین سطح انرژی ارتعاشی خود قرار دارد.
البته اتم ها کاملاً ثابت نیستند و همواره در حال لرزش اند، به همین دلیل فاصله پیوندی در هر لحظه کمی تغییر می کند. با این حال، مقدار ۱٫۲۷ آنگستروم به عنوان میانگین پایدار و مرجع پذیرفته می شود و در بیشتر منابع علمی به آن اشاره شده است.
روش های پیشرفته طیف سنجی توانسته اند این فاصله را با دقت بسیار بالا، حتی در حد چند صدهزارم آنگستروم، تعیین کنند. به همین دلیل شیمیدان ها معمولاً از آنگستروم یا پیکومتر برای بیان چنین فاصله هایی استفاده می کنند. در نهایت، طول پیوند H–Cl یک عدد کلیدی است که اندازه و ساختار این مولکول ساده را توصیف می کند.
مقایسه طول پیوند HCl با سایر مولکول های دو اتمی
اگر طول پیوند حدود ۱۲۷ پیکومتر برای HCl را مبنا قرار دهیم، مقایسه آن با پیوندهای مشابه در مولکول های دو اتمی کمک می کند جایگاه این عدد بهتر درک شود. در خانواده هیدروژن هالیدها یعنی HF، HCl، HBr و HI، پیوند HCl نه خیلی کوتاه است و نه خیلی بلند، بلکه در حد میانی قرار می گیرد.
برای مثال، در هیدروژن فلوئورید پیوند بسیار کوتاه تر است و حدود ۹۲ پیکومتر اندازه دارد. دلیل آن کوچک بودن اتم فلوئور و قدرت بالای پیوند میان هیدروژن و فلوئور است. هرچه در این گروه به سمت اتم های بزرگ تر حرکت می کنیم، طول پیوند افزایش پیدا می کند.
در هیدروژن برمید، فاصله پیوندی به حدود ۱۴۱ پیکومتر می رسد و در هیدروژن یدید این عدد حتی به حدود ۱۶۱ پیکومتر افزایش می یابد. این تغییرات نشان می دهد که با بزرگ تر شدن اتم هالوژن، پیوند ضعیف تر و بلندتر می شود.
در سوی دیگر، مولکولی مثل H₂ پیوندی بسیار کوتاه دارد، چون از دو اتم کوچک یکسان تشکیل شده است. همچنین Cl₂ با وجود پیوند یگانه، فاصله بلندی دارد زیرا هر دو اتم بزرگ اند و قطبیتی میان آنها وجود ندارد. این مقایسه ها نشان می دهد اندازه اتم ها، قدرت پیوند و قطبیت، همگی در تعیین طول پیوند نقش دارند.
| مولکول | طول پیوند (pm) | انرژی پیوند (کیلوژول بر مول) | گشتاور دوقطبی (D) | درصد یونی بودن |
|---|---|---|---|---|
| H2 | 74 | 432 | 0 | 0 |
| HF | 92 | 565 | 1.82 | ~41 |
| HCl | 127 | 428 | 1.08 | ~17 |
| HBr | 141 | 362 | 0.78 | ~12 |
| HI | 161 | 295 | 0.38 | ~5 |
| HAt* | ~172 (تخمین) | ~250 (تخمین) | ~0 | ~0 |
| Cl2 | 199 | 240 | 0 | 0 |
روش های اندازه گیری طول پیوند مولکولی
اندازه گیری طول پیوند در مولکولی مثل HCl به صورت مستقیم امکان پذیر نیست، چون این فاصله در مقیاسی بسیار کوچک قرار دارد. به همین دلیل، دانشمندان از روش های غیرمستقیم آزمایشگاهی استفاده می کنند تا بتوانند فاصله بین اتم ها را با دقت بالا محاسبه کنند. در طول سال ها، تکنیک های مختلفی برای این کار توسعه یافته که نتایج قابل اعتمادی به دست می دهند.
به طور کلی، این روش ها در دو گروه اصلی قرار می گیرند: روش های طیف سنجی و روش های پراش. در طیف سنجی، رفتار مولکول ها هنگام جذب یا آزاد کردن انرژی بررسی می شود. الگوهای دقیق به دست آمده از این فرآیند، اطلاعات مهمی درباره ساختار مولکول و فاصله اتم ها ارائه می دهند. برای نمونه، تغییرات خطوط طیف چرخشی یا ارتعاشی به طور مستقیم با فاصله بین هسته ها ارتباط دارد.
در روش های پراش، پرتوهایی مانند اشعه ایکس یا الکترون به نمونه تابانده می شود و الگوی حاصل از پراکندگی آنها تحلیل می گردد. این الگوها می توانند جایگاه نسبی اتم ها را نشان دهند. هر کدام از این روش ها کاربرد خاص خود را دارند و در کنار هم، امکان تعیین دقیق طول پیوند H–Cl را فراهم کرده اند.
طیف سنجی چرخشی و تعیین طول پیوند
یکی از دقیق ترین راه ها برای به دست آوردن طول پیوند در مولکول HCl، استفاده از طیف سنجی چرخشی است که معمولاً در ناحیه مایکروویو انجام می شود. در حالت گازی، مولکول های HCl آزادانه می چرخند و این چرخش ها فقط در ترازهای انرژی مشخصی امکان پذیر است. هر بار که مولکول از یک تراز به تراز دیگر می رود، انرژی را به صورت موج مایکروویو جذب یا آزاد می کند.
الگوی این جذب و گسیل به ویژگی فیزیکی مهمی به نام گشتاور لختی بستگی دارد. در مولکول های دو اتمی، این کمیت به جرم اتم ها و فاصله میان آن ها مرتبط است. بنابراین با بررسی دقیق خطوط طیفی، می توان اطلاعات مستقیمی از فاصله بین هسته ها به دست آورد.
دانشمندان از ثابت چرخشی مولکول استفاده می کنند که به طور ریاضی به گشتاور لختی وابسته است. وقتی این مقدار با دقت اندازه گیری شود، طول پیوند نیز قابل محاسبه خواهد بود. برای HCl، اندازه گیری های بسیار دقیق عددی نزدیک به ۱٫۲۷۴ آنگستروم را نشان داده اند.
جالب است که ایزوتوپ های مختلف کلر، مانند ^35Cl و ^37Cl، اگرچه طیف های کمی متفاوت دارند، اما طول پیوند به دست آمده برای هر دو تقریباً یکسان است. این موضوع نشان می دهد طیف سنجی چرخشی روشی قابل اعتماد و بسیار دقیق برای تعیین فاصله اتم ها در مولکول هیدروژن کلرید است.
طیف سنجی ارتعاشی و تحلیل طول پیوند
طیف سنجی ارتعاشی، به ویژه روش فروسرخ، یکی دیگر از راه های مهم برای بررسی طول پیوند به شمار می رود، هرچند این کار به شکل مستقیم انجام نمی شود. در این روش، پیوند H–Cl مانند یک فنر در نظر گرفته می شود که می تواند کشیده و رها شود. این حرکت رفت و برگشتی با فرکانس مشخصی رخ می دهد که در ناحیه فروسرخ قابل شناسایی است.
وقتی طیف جذب فروسرخ HCl در حالت گازی بررسی می شود، به جای یک خط ساده، مجموعه ای از خطوط منظم دیده می شود. علت این موضوع آن است که ارتعاش پیوند همزمان با تغییرات چرخشی مولکول همراه می شود. این ترکیب باعث ایجاد الگویی می گردد که به آن طیف ارتعاشی–چرخشی گفته می شود و شامل شاخه های مختلفی است.
با بررسی دقیق این الگو، می توان اطلاعات ارزشمندی درباره وضعیت مولکول در حالت عادی و حالت برانگیخته به دست آورد. از همین داده ها، طول پیوند در هر حالت محاسبه می شود. معمولاً در حالت برانگیخته، فاصله میان اتم ها کمی بیشتر است، چون پیوند هنگام ارتعاش اندکی کش می آید.
نتایج به دست آمده از طیف فروسرخ با اندازه گیری های طیف سنجی چرخشی همخوانی دارد و آن ها را تایید می کند. افزون بر این، فرکانس ارتعاشی خود نشانه ای از قدرت پیوند است؛ هرچه پیوند محکم تر باشد، ارتعاش سریع تری دارد. جایگاه HCl در میان HF، HBr و HI نیز همین روند را نشان می دهد و تصویری کامل از طول و استحکام پیوند ارائه می کند.
روش های پراش برای اندازه گیری طول پیوند
روش های پراش یا پراکندگی نیز راه دیگری برای بررسی طول پیوند در مواد شیمیایی به شمار می روند. در مورد هیدروژن کلرید، استفاده مستقیم از پراش پرتو ایکس چندان ساده نیست، چون این ماده در دمای معمولی به صورت گاز وجود دارد و به راحتی ساختار جامد پایداری ندارد. در حالت جامد هم، مولکول های آن معمولاً با برهم کنش های بین مولکولی کنار هم قرار می گیرند و همین موضوع تحلیل دقیق پیوند را دشوارتر می کند.
اگر HCl در شرایط خاصی مانند دماهای بسیار پایین متبلور شود، می توان با پراش پرتو ایکس جایگاه اتم های کلر را در شبکه بلوری شناسایی کرد. از آنجا که هیدروژن پرتو ایکس را به سختی پراکنده می کند، دیده شدن مستقیم آن آسان نیست، اما موقعیت کلر و شکل کلی ساختار می تواند فاصله تقریبی بین دو اتم را نشان دهد.
برای حالت گازی، پراش الکترونی کاربرد عملی تری دارد. در این روش، پرتو الکترون از میان گاز HCl عبور می کند و الگوی حاصل از پراکندگی اطلاعاتی درباره فاصله اتم ها ارائه می دهد. آزمایش های انجام شده با این شیوه توانسته اند طول پیوند را با دقت قابل توجهی اندازه گیری کنند.
در برخی موارد خاص، از پراش نوترونی نیز استفاده می شود، زیرا نوترون ها توانایی بهتری در آشکارسازی هیدروژن دارند. هرچند این روش ها معمولاً به دقت طیف سنجی نمی رسند، اما نقش مهمی در تایید داده ها و تکمیل تصویر ساختاری پیوند H–Cl داشته اند.
تاثیر حرکت ارتعاشی بر طول پیوند
حتی اگر دما به صفر مطلق برسد، اتم های موجود در مولکول HCl کاملاً بی حرکت نمی شوند. این اتم ها همچنان یک لرزش پایه دارند و به همین دلیل فاصله میان هیدروژن و کلر همیشه دقیقاً ثابت نیست. وقتی از طول پیوندی مثل ۱۲۷ پیکومتر صحبت می شود، معمولاً منظور همان فاصله تعادلی است؛ یعنی حالتی که مولکول در پایدارترین وضعیت خود قرار دارد.
در عمل، پیوند H–Cl دائماً در حال نوسان است و فاصله بین دو اتم لحظه به لحظه کمی تغییر می کند. این رفتار را می توان شبیه یک فنر تصور کرد که گاهی کش می آید و گاهی جمع می شود. در نتیجه، طول پیوند در بعضی لحظات کمی بیشتر و در برخی زمان ها کمی کمتر از مقدار تعادلی خواهد بود.
به همین دلیل، فاصله متوسطی که در حالت ارتعاشی پایه اندازه گیری می شود معمولاً اندکی بزرگ تر از فاصله تعادلی واقعی است. این مقدار متوسط را اغلب با نمادی متفاوت نشان می دهند تا از مقدار ایده آل تعادلی متمایز شود.
اگر مولکول انرژی بیشتری دریافت کند، مثلاً با گرم شدن یا جذب نور فروسرخ، دامنه این نوسان افزایش می یابد. در چنین شرایطی، پیوند به طور میانگین کشیده تر می شود. این تغییر هرچند کوچک است، اما با ابزارهای دقیق طیف سنجی قابل تشخیص است.
شناخت این رفتار ارتعاشی برای تحلیل داده های آزمایشگاهی اهمیت زیادی دارد، زیرا طول پیوند گزارش شده در منابع علمی در واقع یک مقدار مرجع متوسط است، نه عددی کاملاً ثابت در تمام لحظات.
تاثیر جایگزینی ایزوتوپی DCl در مقابل HCl بر طول پیوند
اگر اتم هیدروژن در مولکول HCl با دوتریوم جایگزین شود، مولکولی به نام DCl به وجود می آید. این تغییر ایزوتوپی در نگاه اول شاید ساده به نظر برسد، اما اطلاعات جالبی درباره رفتار پیوند در اختیار ما می گذارد. از نظر شیمیایی، DCl و HCl تفاوت خاصی ندارند، زیرا نوع پیوند و برهم کنش الکترونی میان اتم ها در هر دو یکسان است.
طول پیوند تعادلی در این دو مولکول تقریباً برابر است، چون فاصله اصلی بین اتم ها به توزیع الکترون ها بستگی دارد، نه به جرم هیدروژن یا دوتریوم. به بیان ساده، الکترون ها تعیین می کنند اتم ها در چه فاصله ای کنار هم قرار بگیرند. با این حال، جرم متفاوت باعث تغییر در نحوه حرکت اتم ها می شود.
دوتریوم سنگین تر از هیدروژن معمولی است و همین موضوع باعث می شود مولکول DCl آرام تر ارتعاش کند. دامنه این لرزش نیز کمی کمتر است، زیرا اتم سنگین تر کشش کمتری به پیوند وارد می کند. نتیجه این رفتار آن است که فاصله متوسط پیوند در DCl اندکی کوتاه تر از HCl اندازه گیری می شود.
این اختلاف بسیار ناچیز است و در حد چند هزارم آنگستروم قرار دارد، اما ابزارهای دقیق آزمایشگاهی توانسته اند آن را ثبت کنند. بررسی تفاوت های جزئی در داده های طیفی HCl و DCl نیز این موضوع را تایید کرده است. این مثال نشان می دهد حتی تغییرات بسیار کوچک در جرم اتم ها می تواند از دید مکانیک کوانتومی بر طول پیوندهای شیمیایی اثر بگذارد.




