فهرست عناوین
- مقدمه
- فرمول شیمیایی و ترکیب اسید هیدروکلریک
- ساختار مولکولی و پیوند در HCl
- ویژگی های فیزیکی اسید هیدروکلریک
- رفتار HCl در محلول آبی
- قدرت اسیدی و pH اسید هیدروکلریک
- واکنش های شیمیایی اسید هیدروکلریک
- تولید صنعتی اسید هیدروکلریک
- گریدها و غلظت های اسید هیدروکلریک
- ویژگی های اسید هیدروکلریک در غلظت های مختلف
- کاربردها و موارد استفاده اسید هیدروکلریک
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 13-08-1404
تاریخ بروزرسانی مقاله : 13-08-1404
تعداد کلمات : 3100
آدرس مقاله : لینک مقاله
ساختار و فرمول شیمیایی اسید کلریدریک

مقدمه
اسید هیدروکلریک یکی از موادی است که خیلی ها آن را با نام جوهر نمک می شناسند. این ماده در اصل از حل شدن یک گاز در آب به وجود می آید و به همین دلیل خاصیت اسیدی بالایی دارد. ظاهر آن شفاف است، اما بوی تندش خیلی زود حضورش را نشان می دهد.
این اسید توانایی بالایی در حل کردن بعضی مواد دارد و به همین خاطر باید با دقت زیادی از آن استفاده شود. تماس نادرست با آن میتواند باعث آسیب شود، چون واکنش هایش سریع و قوی هستند. به همین دلیل هم همیشه جزو مواد شیمیایی حساس به حساب می آید.
جالب است بدانید همین ماده، به شکل طبیعی در بدن انسان هم وجود دارد. اسید موجود در معده که به هضم غذا کمک می کند، از همین خانواده است و بدون آن فرایند گوارش به درستی انجام نمی شود.
علاوه بر کاربردهای بدن، اسید هیدروکلریک در محیط های مختلف مثل آزمایشگاه ها و کارخانه ها نقش مهمی دارد. از تمیزکاری گرفته تا فرایندهای صنعتی، این ماده یکی از پایه های بسیاری از کارها به شمار می رود و شناخت درست آن برای استفاده ایمن اهمیت زیادی دارد.
فرمول شیمیایی و ترکیب اسید هیدروکلریک
اسید هیدروکلریک فرمول شیمیایی ساده HCl دارند، یعنی هر مولکول آن از یک اتم هیدروژن (H) و یک اتم کلر (Cl) تشکیل شده است. به دلیل همین ترکیب یک به یک، هنگام اشاره به گاز خالص آن را کلرید هیدروژن می نامند. در محلول های آبی، HCl به یون های هیدروژن (به صورت یون هیدرونیوم) و یون های کلرید تفکیک می شود، با این حال فرمول مولکولی اش برای محاسبات استوکیومتری همان HCl باقی می ماند.
اتم هیدروژن در HCl عدد اتمی ۱ و اتم کلر عدد اتمی ۱۷ دارد که موقعیت آن ها را به ترتیب به عنوان یک نافلز سبک و یک هالوژن نشان می دهد. HClیک اسید تک پروتونی است، یعنی هر مولکول آن می تواند یک پروتون (H⁺) در آب آزاد کند. جرم مولکولی HCl تقریباً ۳۶٫۴۶ گرم بر مول است که ۱٫۰۱ گرم بر مول از هیدروژن و ۳۵٫۴۵ گرم بر مول از کلر تشکیل شده. در حالت جامد (در دماهای بسیار پایین)، گاز هیدروژن کلرید می تواند ساختاری بلوری به صورت شبکه یونی [H₂Cl⁺][Cl⁻] تشکیل دهد، اما در شرایط عادی HCl به صورت گاز یا محلول اسید هیدروکلریک مشاهده می شود.
به دلیل ویژگی های منحصر به فرد و کاربردهای گسترده اش در صنایع مختلف، خرید اسید کلریدریک یکی از نیازهای اصلی بسیاری از کارخانه های شیمیایی و آزمایشگاه ها محسوب می شود. فرمول شیمیایی HCl ترکیب ساده اما مؤثر این ماده را نشان می دهد و نبود اکسیژن در ساختار آن، تفاوتش با اسیدهای اکسیژنه مانند H₂SO₄ یا HNO₃ را برجسته می کند.
ساختار مولکولی و پیوند در HCl
ساختار هیدروژن کلرید بسیار ساده و قابل فهم است. این ماده فقط از دو اتم تشکیل شده؛ یک اتم هیدروژن که به یک اتم کلر وصل شده و در کنار هم یک مولکول کوچک و دواتمی را می سازند.
اتصال میان این دو اتم از نوع پیوند کووالانسی است، اما این پیوند حالت یکنواختی ندارد. کلر توانایی بیشتری در جذب الکترون دارد و همین باعث می شود الکترون ها بیشتر به سمت آن کشیده شوند. نتیجه این تفاوت، ایجاد ناحیه ای با بار نسبی مثبت در سمت هیدروژن و ناحیه ای با بار نسبی منفی در سمت کلر است.
به دلیل همین نابرابری در پخش بار، مولکول HCl خاصیتی به نام دوقطبی بودن دارد. شکل این مولکول کاملاً خطی است و فاصله بین دو اتم آن در حد بسیار کوچکی، حدود چند دهم نانومتر، قرار دارد که نشان دهنده سادگی ساختمان آن است.
وقتی هیدروژن کلرید به صورت گاز یا در حلال های غیرقطبی وجود دارد، مولکول ها معمولاً به شکل جدا از هم باقی می مانند. بر خلاف آب، میان مولکول های آن پیوند هیدروژنی قوی شکل نمی گیرد، چون هیدروژن به عنصری مثل اکسیژن یا نیتروژن متصل نیست.
در مجموع می توان گفت HCl یکی از ساده ترین نمونه ها در میان اسیدهاست؛ مولکولی کوچک، خطی و بدون ساختارهای پیچیده که همین سادگی، پایه بسیاری از رفتارهای شیمیایی آن را شکل می دهد.
ویژگی های فیزیکی اسید هیدروکلریک
هیدروژن کلرید بی آب، گازی بی رنگ است که در هوای مرطوب به دلیل تشکیل قطرات ریز اسید، دود می کند. با حل شدن این گاز در آب، اسید هیدروکلریک به وجود می آید که مایعی شفاف و بی رنگ (یا کمی زرد در صورت ناخالصی) با بوی تند و زننده است. خواص فیزیکی اسید کلریدریک به غلظت آن بستگی دارد؛ برای مثال اسید کلریدریک غلیظ معمول حدود ۳۷٪ وزنی HCl دارد و چگالی آن نزدیک به ۱٫۱۹ گرم بر میلی لیتر است، در حالی که محلول های رقیق تر مانند ۲۰٪ یا ۵٪ چگالی و نقطه جوش متفاوتی دارند.
اسید غلیظ بخارات خورنده ای آزاد می کند چون گاز HCl به راحتی از محلول فرار می کند. تمامی محلول های این اسید بسیار خورنده اند و در تماس با فلزات یا بافت های آلی، باعث تخریب و خوردگی می شوند. هرچند خود اسید قابل اشتعال نیست، اما در واکنش با فلزات گاز هیدروژن قابل اشتعال آزاد می کند. از نظر ظاهری، شبیه آب است ولی بخارات سفیدرنگ آن یادآور خطر بالای این ماده و ضرورت رعایت کامل نکات ایمنی است.
رفتار HCl در محلول آبی
وقتی گاز هیدروژن کلرید وارد آب می شود، تقریباً هیچ مولکولی به همان شکل اولیه باقی نمی ماند. این گاز به سرعت با آب واکنش می دهد و اجزای آن از هم جدا می شوند. در این حالت، هیدروژن به آب منتقل شده و یون هیدرونیوم به وجود می آید، در حالی که کلر به صورت یون کلرید در محلول پخش می شود.
به بیان ساده تر، هر مولکول HCl یک پروتون را به آب می دهد و همین اتفاق باعث اسیدی شدن شدید محیط می شود. چون این فرایند تقریباً به طور کامل انجام می گیرد، اسید هیدروکلریک در گروه اسیدهای قوی قرار می گیرد و محلول آن توان بالایی در هدایت جریان برق دارد.
یون های هیدرونیوم نقش اصلی را در ایجاد pH پایین و واکنش پذیری این اسید بازی می کنند. این یون ها هستند که باعث می شوند اسید با مواد قلیایی به شدت واکنش نشان دهد. در مقابل، یون های کلرید معمولاً پایدار باقی می مانند و تغییر شیمیایی خاصی در آب نمی دهند.
نکته مهم دیگر این است که حل شدن HCl در آب همراه با آزاد شدن گرماست. به همین دلیل، هنگام رقیق کردن اسید غلیظ باید با دقت زیادی عمل کرد تا خطر پاشش یا افزایش ناگهانی دما پیش نیاید.
برخلاف بعضی اسیدها که خاصیت اکسیدکنندگی دارند، اسید هیدروکلریک چنین رفتاری از خود نشان نمی دهد. دلیل آن هم این است که یون کلرید در محیط آبی واکنش پذیر نیست. همین یونیزه شدن سریع و کامل در آب، توضیح می دهد چرا این اسید رسانایی بالا و واکنش های تند و قابل توجهی در واکنش های اسید و باز دارد.
قدرت اسیدی و pH اسید هیدروکلریک
اسید هیدروکلریک در میان اسیدها به قدرت بسیار بالای خود شناخته می شود. وقتی این ماده وارد آب می شود، تقریباً همه مولکول های آن پروتون خود را آزاد می کنند و به همین دلیل خاصیت اسیدی شدیدی به محلول می دهند. این رفتار نشان می دهد که تمایل HCl به جدا شدن در آب بسیار زیاد است.
حتی محلول هایی که غلظت بالایی ندارند، pH پایینی ایجاد می کنند. برای نمونه، یک محلول معمولی با غلظت کم هم می تواند محیطی کاملاً اسیدی بسازد و عدد pH را به نزدیکی یک یا حتی کمتر برساند. هرچه غلظت بیشتر شود، این اثر شدیدتر خواهد بود و در نمونه های بسیار غلیظ، pH می تواند به مقادیر منفی هم برسد.
این شدت اسیدی به معنی فعالیت بالای یون های هیدروژن در محلول است. به همین خاطر، اسید هیدروکلریک قادر است با موادی واکنش دهد یا آن ها را حل کند که اسیدهای ضعیف تر از عهده شان برنمی آیند. همین ویژگی باعث شده در بسیاری از واکنش های شیمیایی به عنوان یک اسید قابل اعتماد به کار رود.
از نظر قدرت، این اسید در کنار اسیدهای معدنی نیرومند دیگری مثل اسید نیتریک و اسید سولفوریک قرار می گیرد. تفاوت اصلی آن با اسیدهای ضعیف این است که واکنش هایش با مواد قلیایی تقریباً کامل انجام می شود و بازگشتی در کار نیست، در حالی که اسیدهای ضعیف فقط بخشی از توان خود را نشان می دهند.
البته همین توان بالا باعث می شود کار با اسید هیدروکلریک نیازمند دقت زیادی باشد. مقدار کمی از آن می تواند تعادل یک محیط را به هم بزند و pH را به سرعت پایین بیاورد. در مجموع، قدرت اسیدی زیاد و رفتار ویژه آن در آب دلیل اصلی استفاده گسترده این اسید در آزمایشگاه ها و فرایندهای صنعتی است.
واکنش های شیمیایی اسید هیدروکلریک
اسید هیدروکلریک رفتاری کاملاً شبیه یک اسید قوی دارد و در واکنش ها به سرعت وارد عمل می شود. این ماده به راحتی با بازها ترکیب شده و آن ها را خنثی می کند، به طوری که در پایان واکنش معمولاً آب و یک نمک ساده به وجود می آید. چنین واکنش هایی از شناخته شده ترین نمونه ها در شیمی هستند.
این اسید همچنین با موادی مثل کربنات ها واکنش نشان می دهد و در جریان این فرایند، گاز دی اکسید کربن آزاد می شود. همین ویژگی باعث می شود در بسیاری از آزمایش ها یا کاربردهای صنعتی بتوان از آن برای تشخیص یا تجزیه این ترکیبات استفاده کرد.
در برخورد با فلزات هم رفتار مشخصی دارد. فلزاتی مانند روی یا آهن که واکنش پذیری بیشتری دارند، به آسانی در اسید هیدروکلریک حل می شوند. در این حالت، گاز هیدروژن آزاد شده و نمک کلرید فلز مربوطه تشکیل می شود. این واکنش ها معمولاً سریع و همراه با جوشش گاز هستند.
در مقابل، فلزاتی مثل مس یا نقره در برابر این اسید مقاوم ترند و به تنهایی واکنشی از خود نشان نمی دهند. دلیل آن هم این است که اسید هیدروکلریک خاصیت اکسیدکنندگی ندارد. برای حل کردن فلزات گران بها مثل طلا، به ترکیبی خاص نیاز است که در آن یک ماده دیگر نقش اکسیدکننده را بازی کند.
به طور کلی، نقش اصلی اسید هیدروکلریک در واکنش های شیمیایی دادن پروتون و فراهم کردن یون کلرید است. نتیجه این دو ویژگی، تشکیل نمک های کلریدی است که اغلب در آب حل می شوند. همین خصوصیات باعث شده این اسید در کارهایی مثل تمیزکاری فلزات، از بین بردن زنگار و همچنین در بسیاری از فرایندهای شیمیایی و صنعتی کاربرد گسترده ای داشته باشد.
تولید صنعتی اسید هیدروکلریک
در صنعت، بیشتر اسید هیدروکلریک از راه تولید گاز هیدروژن کلرید و سپس حل کردن آن در آب به دست می آید. یکی از روش های رایج، ترکیب مستقیم گاز هیدروژن با گاز کلر است. این واکنش با آزاد شدن گرما انجام می شود و گاز داغ حاصل را بلافاصله وارد آب می کنند تا اسیدی با خلوص بالا تولید شود.
در کنار این روش مستقیم، بخش قابل توجهی از اسید هیدروکلریک به عنوان محصول جانبی سایر فرایندهای شیمیایی به دست می آید. برای نمونه، در تولید موادی مثل PVC که شامل واکنش های کلردار شدن هستند، گاز HCl آزاد می شود. این گاز جمع آوری شده و دوباره به صورت محلول اسیدی مورد استفاده قرار می گیرد، بدون آن که نیازی به تولید جداگانه باشد.
در گذشته، شیوه های قدیمی تری برای تولید این اسید وجود داشت. یکی از آن ها واکنش نمک خوراکی با اسید سولفوریک بود که در قرن های قبل کاربرد فراوانی داشت. این روش که بخشی از فرایندهای قدیمی صنایع شیمیایی محسوب می شد، امروز به دلیل بازده کمتر و مشکلات زیست محیطی کنار گذاشته شده است.
امروزه تولید اسید هیدروکلریک معمولاً در کنار صنعت کلر و سود سوزآور انجام می شود. در این مجموعه ها، گازهای هیدروژن و کلر که به طور هم زمان تولید می شوند، در همان محل با هم واکنش داده و به هیدروژن کلرید تبدیل می شوند. این کار باعث استفاده بهینه از مواد و کاهش اتلاف می شود.
اسید هیدروکلریک تجاری معمولاً با غلظت هایی در حدود ۳۰ تا ۳۸ درصد عرضه می شود. محلول های غلیظ تر ناپایدارتر هستند، بخار زیادی ایجاد می کنند و نگهداری آن ها به تجهیزات خاص نیاز دارد. به همین دلیل، بیشتر تولیدکنندگان اسید را در همین بازه غلظت به بازار ارائه می دهند.
در عمل، بخش زیادی از اسید تولید شده در همان واحدهای صنعتی مصرف می شود؛ مثلاً در فرایندهای فلزی، تولید کود یا ساخت مواد شیمیایی دیگر. تنها بخشی از آن به عنوان محصول نهایی به بازار می رسد. به طور کلی ترکیب روش های مستقیم تولید و بازیابی از فرایندهای جانبی باعث شده تأمین اسید هیدروکلریک به صورت پایدار و پیوسته انجام شود.
گریدها و غلظت های اسید هیدروکلریک
اسید هیدروکلریک بسته به نوع مصرف، با غلظت ها و درجه های خلوص متفاوتی در دسترس قرار می گیرد. هرچه کاربرد تخصصی تر باشد، معمولاً اسید خالص تر و غلیظ تری استفاده می شود و برای مصارف ساده تر، محلول های رقیق کفایت می کنند.
بیشترین غلظتی که این اسید در شرایط عادی می تواند به صورت پایدار وجود داشته باشد، حدود ۳۸ درصد است که به آن اسید هیدروکلریک غلیظ می گویند. نوع آزمایشگاهی معمولاً کمی پایین تر از این مقدار است و به دلیل بخار زیاد و خاصیت خورندگی بالا، باید با احتیاط کامل از آن استفاده شود.
در صنعت معمولاً محلول هایی با غلظت متوسط تر به کار می رود. اسیدهای ۳۰ تا ۳۳ درصد رایج ترین گزینه برای واحدهای صنعتی هستند، چون هم قدرت کافی دارند و هم جابه جایی و نگهداری آن ها ساده تر و ایمن تر است.
برای استفاده های خانگی، شکل بسیار رقیق تری از این اسید عرضه می شود که بیشتر با نام جوهر نمک شناخته می شود. این محلول معمولاً بین ۱۰ تا ۱۵ درصد اسید دارد و برای کارهایی مثل جرم گیری، تمیز کردن سطوح ساختمانی یا تنظیم اسیدیته آب استخر به کار می رود. به دلیل وجود ناخالصی ها، رنگ آن اغلب کمی متمایل به زرد است.
از نظر خلوص هم دسته بندی های مختلفی وجود دارد. نوع صنعتی برای کاربردهای عمومی ساخته می شود، نوع خوراکی خلوص بالاتری دارد و در صنایع غذایی استفاده می شود و نوع آزمایشگاهی یا معرف شیمیایی بسیار خالص است و برای کارهای دقیق آزمایشگاهی به کار می رود.
به طور معمول، محلول هایی با غلظت بالاتر از حدود ۴۰ درصد وارد بازار نمی شوند، چون تبخیر شدید و خطرات نگهداری دارند. به همین دلیل، هر مصرف کننده بسته به نیاز خود، از اسیدهای بسیار رقیق خانگی تا نمونه های غلیظ صنعتی یا آزمایشگاهی، گزینه مناسب را انتخاب می کند.
ویژگی های اسید هیدروکلریک در غلظت های مختلف
خواص اسید هیدروکلریک به طور قابل توجهی با تغییر غلظت آن تفاوت می کند. با افزایش میزان HCl در آب، چگالی محلول بیشتر می شود، اسیدیته کاهش pH آن افزایش می یابد و نقطه جوش محلول به شکل غیرخطی تغییر می کند که این امر ناشی از تشکیل آزئوتروپ ها است.
در غلظت های بسیار کم، اسید هیدروکلریک رفتاری شبیه آب دارد، اما حتی چند درصد کم از HCl نیز pH را به شدت کاهش می دهد. جدول زیر برخی خواص کلیدی محلول های اسید هیدروکلریک را در غلظت های مختلف (در فشار ~۱ اتمسفر) نشان می دهد.
این جدول نشان می دهد که چگالی، مولاریته، pH و نقطه جوش چگونه به درصد HCl وابسته هستند. یکی از ویژگی های جالب، حداکثر بودن نقطه جوش در ~۲۰٫۲٪ HCl (غلظت آزئوتروپ) است که در غلظت های بالاتر از آن افزودن HCl خالص بر عکس باعث کاهش نقطه جوش محلول می شود. با افزایش غلظت، چگالی محلول به طور یکنواخت زیاد می شود که نشانگر سنگین بودن HCl نسبت به آب است. مقادیر pH در غلظت های بالا به بازه منفی می رسند که نشان دهنده فعالیت بسیار بالای پروتون در این حالت است. توجه شود که ۰٪ در جدول معادل آب خالص (مرجع) است.
این خواص از نظر عملی حائز اهمیت هستند: اسید غلیظ (۳۰٪ به بالا) بخاردار است و در دمای نسبتاً کمی می جوشد، در حالی که محلول های متوسط فراریت کمتری دارند. درک این تغییرات در ذخیره سازی ایمن و استفاده صحیح از اسید هیدروکلریک در غلظت های مختلف مفید است.
| ٪ وزنی HCl | چگالی (g/mL) | مولاریته (M) | پی اچ (تقریبی) | نقطه جوش (°C) |
|---|---|---|---|---|
| ۰٪ (آب) | ۰٫۹۹۸ | ۰ | ~۷ (خنثی) | ۱۰۰ |
| ۵٪ | ~۱٫۰۲ | ~۱٫۴ | ۰٫۱- | ~۱۰۲ |
| ۱۰٪ | ~۱٫۰۵ | ~۲٫۹ | ۰٫۵- | ~۱۰۳ |
| ۲۰٪ | ~۱٫۱۰ | ~۶٫۰ | ۰٫۸- | ~۱۰۹ |
| ۳۰٪ | ~۱٫۱۵ | ~۹٫۵ | ۱٫۰- | ~۹۰ |
| ۳۴٪ | ~۱٫۱۷ | ~۱۰٫۹ | ۱٫۰- | ~۷۱ |
| ۳۶٪ | ~۱٫۱۸ | ~۱۱٫۶ | ۱٫۱- | ~۶۱ |
| ۳۸٪ | ~۱٫۱۹ | ~۱۲٫۴ | ۱٫۱- | ~۴۸ |
همان طور که دیده می شود محلول های بسیار رقیق HCl از نظر نقطه جوش تقریباً مانند آب رفتار می کنند و خاصیت اسیدی متوسط دارند؛ در حالی که محلول های غلیظ pH بسیار پایینی دارند و در دماهای نسبتاً کمی می جوشند زیرا HCl به راحتی تبخیر می شود. وجود آزئوتروپ در غلظت ~۲۰٪ موجب بیشینه شدن نقطه جوش ~۱۰۸–۱۰۹ °C شده است. چگالی های ذکر شده مربوط به دمای حدود ۲۰ °C هستند. این داده ها نشان می دهند که چرا اسید هیدروکلریک غلیظ بخار می کند (فشار بخار بالایی دارد) و چرا در شرایط معمول یک حد عملی برای غلظت آن وجود دارد.
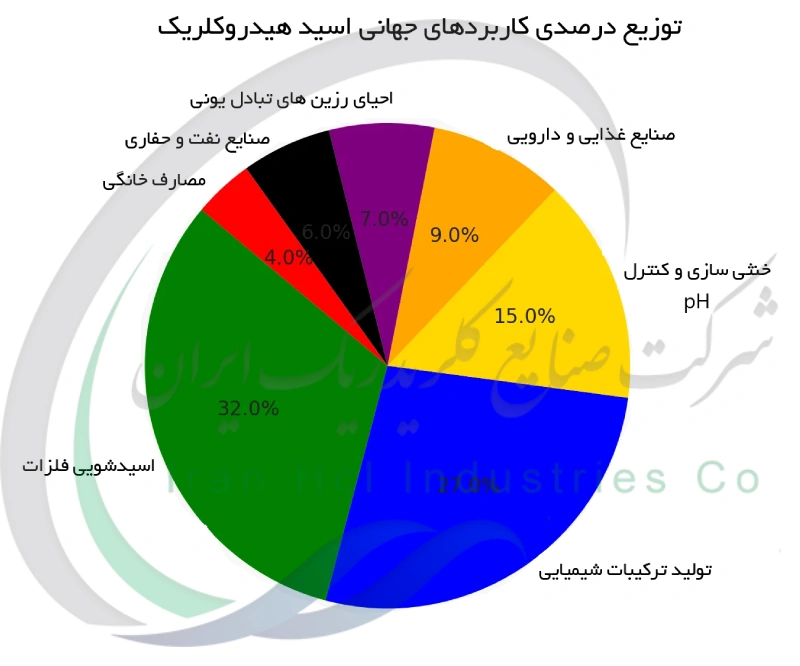
کاربردها و موارد استفاده اسید هیدروکلریک
اسید هیدروکلریک در زمینه های گوناگون کاربرد دارد و به همین دلیل یکی از اسیدهای پرمصرف به شمار می رود. در صنعت، یکی از استفاده های مهم آن تمیزکاری سطوح فلزی است. این اسید قبل از انجام مراحلی مثل پوشش دهی یا گالوانیزه کردن، زنگ زدگی و لایه های اضافی روی فولاد را از بین می برد و سطحی آماده برای ادامه کار فراهم می کند.
در بخش تولید مواد شیمیایی هم نقش پررنگی دارد. از این اسید برای ساخت انواع نمک های کلریدی استفاده می شود؛ موادی که در تصفیه آب، پالایشگاه ها و بسیاری از فرایندهای شیمیایی دیگر به کار می روند. همچنین در تولید برخی ترکیبات آلی، از جمله موادی که پایه ساخت پلاستیک هایی مانند PVC هستند، حضور اسید هیدروکلریک ضروری است.
در صنایع غذایی، نوع خالص تر این اسید به کار گرفته می شود. این گرید برای تنظیم اسیدیته، کمک به فرآوری نشاسته، تولید ژلاتین و بهبود برخی مراحل تولید غذا و نوشیدنی استفاده می شود، البته در چارچوب استانداردهای ایمنی و بهداشتی مشخص.
کنترل pH یکی دیگر از کاربردهای مهم اسید هیدروکلریک است. در بسیاری از واحدهای صنعتی، برای خنثی کردن پساب های قلیایی یا حفظ تعادل اسیدی آب استخرها از این ماده استفاده می شود تا شرایط ایمن و مناسب برقرار بماند.
در مصارف خانگی و خدماتی، شکل رقیق این اسید که بیشتر با نام جوهر نمک شناخته می شود، به عنوان یک پاک کننده قوی کاربرد دارد. این محلول برای از بین بردن رسوبات آهکی، جرم ها و لکه های سخت از روی سطوحی مانند کاشی، بتن و لوله ها به کار می رود.
در آزمایشگاه ها نیز اسید هیدروکلریک جایگاه ویژه ای دارد. این اسید در بسیاری از واکنش ها و آزمایش های شیمیایی استفاده می شود و به ویژه در آزمایش های سنجش اسید و باز، انتخاب مناسبی است چون فرآورده های آن معمولاً اختلالی در نتیجه ایجاد نمی کنند. مجموعه این کاربردها نشان می دهد که اسید هیدروکلریک، از مقیاس های بزرگ صنعتی تا استفاده های روزمره، ماده ای بسیار مهم و پرکاربرد است.





بررسی فرمول مولکولی و جرم مولکولی اسید کلریدریک و تولید صنعتی آن
بررسی ساختار پیوندی و شکل مولکولی اسید کلریدریک و مقایسه آن با سایر هالیدهای هیدروژن
بررسی و درک قطبیت مولکول اسید کلریدریک و الکترونگاتیوی
بررسی یونش اسید کلریدریک در آب و کاربردهای صنعتی و روزمره آن