فهرست عناوین
- مقدمه
- درک یونیزاسیون اسید هیدروکلریک
- معادله شیمیایی HCl در آب
- یونیزاسیون در مقابل تفکیک HCl
- چرا اسید هیدروکلریک در آب یونیزه می شود
- تشکیل یون های هیدرونیوم (H₃O⁺)
- اسید هیدروکلریک به عنوان یک اسید قوی
- تأثیر بر pH محلول
- رسانایی الکتریکی محلول های HCl
- ثابت تفکیک اسیدی (Ka) اسید هیدروکلریک
- مقایسه اسید هیدروکلریک با اسیدهای ضعیف
- تغییرات گرما و انرژی هنگام یونیزاسیون
- واکنش های خنثی سازی HCl
- ماهیت خورندگی و اقدامات ایمنی
- کاربردهای صنعتی و روزمره اسید هیدروکلریک
- اسید هیدروکلریک در معده انسان
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 28-08-1404
تاریخ بروزرسانی مقاله : 28-08-1404
تعداد کلمات : 3400
آدرس مقاله : لینک مقاله
یونش اسید کلریدریک در آب

مقدمه
یونیزاسیون اسید هیدروکلریک در آب یکی از فرآیندهای بنیادی شیمی هستند که نشان می دهد یک اسید قوی در محلول چگونه رفتار می کند. هنگامی که گاز هیدروژن کلرید (HCl) در آب حل می شود، به ذرات باردار تفکیک می گردد و یون های هیدروژن و کلرید تولید می کند. این تبدیل مولکول های خنثی HCl به یون ها عملاً به طور کامل رخ می دهد و به همین دلیل اسید هیدروکلریک نمونه ای از یک اسید قوی است.
در بسیاری از صنایع، آشنایی با این رفتار کاملاً ضروری است، زیرا واحدهای تولیدی هنگام خرید جوهر نمک باید از میزان یونیزاسیون و قدرت خورندگی آن در کاربردهای مختلف آگاهی دقیق داشته باشند. یون های هیدروژن آزاد شده (که در آب یون هیدرونیوم تشکیل می دهند) مسئول خاصیت اسیدی و خورندگی محلول هستند. به زبان ساده، وقتی HCl با آب مخلوط می شود، یک محلول اسیدی ایجاد می کند که قادر به هدایت جریان برق است و با بسیاری از مواد به شدت واکنش نشان می دهد. در ادامه ما این پدیده یونیزاسیون را از جنبه های مختلف بررسی می کنیم.
درک یونیزاسیون اسید هیدروکلریک
اسید هیدروکلریک در محیط آبی تقریباً به طور کامل به یون ها تبدیل می شود، یعنی بیشتر مولکول های HCl پس از ورود به آب از حالت خنثی خارج می گردند. به زبان ساده، یونیزه شدن به فرآیندی گفته می شود که در آن یک ماده بدون بار، هنگام حل شدن در آب، به ذرات باردار مثبت و منفی تبدیل می شود.
هیدروژن کلرید در حالت خالص خود که به صورت گاز وجود دارد، یک ترکیب کووالانسی محسوب می شود. اما زمانی که با آب تماس پیدا می کند، ساختار آن تغییر کرده و یون هیدرونیوم و یون کلرید به وجود می آید. این رفتار بر اساس تعریف آرنیوس از اسیدها قابل توضیح است؛ طبق این دیدگاه، ماده ای اسید نامیده می شود که در آب یون هیدروژن آزاد کند و HCl دقیقاً همین ویژگی را دارد.
فرآیند یونیزاسیون HCl بسیار سریع انجام می شود و عملاً به طور کامل پیش می رود. در یک محلول رقیق معمولی، تقریبا هیچ مولکول سالمی از HCl باقی نمی ماند و محیط شامل یون های آزاد در حال حرکت است، نه مولکول های خنثی.
همین جدایش کامل پایه تمام ویژگی های اسید هیدروکلریک در آب را شکل می دهد؛ از pH بسیار پایین گرفته تا واکنش پذیری بالا. از آنجا که آب توانایی بالایی در پایدار کردن ذرات باردار دارد، این تفکیک از نظر انرژی مطلوب است. به همین دلیل، HCl در محلول آبی یک الکترولیت قوی به شمار می رود.
معادله شیمیایی HCl در آب
فرآیند یونیزه شدن اسید هیدروکلریک را می توان با یک معادله شیمیایی کوتاه و روشن توضیح داد. وقتی HCl در آب حل می شود، با مولکول های آب واکنش می دهد و واکنش به صورت HCl + H₂O → H₃O⁺ + Cl⁻ نمایش داده می شود. این رابطه نشان می دهد که یک پروتون از مولکول HCl جدا شده و به آب منتقل می گردد و یون هیدرونیوم را می سازد، در حالی که کلر به یون کلرید تبدیل می شود.
گاهی برای سادگی، این فرآیند به شکل HCl → H⁺ + Cl⁻ نوشته می شود، اما در واقع یون H⁺ در محیط آبی به تنهایی وجود ندارد و بلافاصله با آب ترکیب می شود. این واکنش در شرایط معمول تقریباً یک طرفه است و بیانگر تفکیک کامل HCl در آب می باشد.
برخلاف اسیدهای ضعیف که تنها بخشی از مولکول هایشان یونیزه می شوند، اسید هیدروکلریک تقریبا به طور کامل به یون تبدیل می شود. هر مول HCl در محلول، یک مول یون هیدرونیوم و یک مول یون کلرید تولید می کند. شیمیدان ها اغلب این رفتار را به صورت HCl (aq) → H⁺ (aq) + Cl⁻ (aq) نشان می دهند که نشان می دهد مولکول خنثی HCl در آب باقی نمی ماند.
یونیزاسیون در مقابل تفکیک HCl
واژه های یونیزاسیون و تفکیک اغلب برای توصیف رفتار HCl در آب به جای هم استفاده می شوند، اما از نظر علمی تفاوت های ظریفی میان آن ها وجود دارد. یونیزاسیون به فرآیندی گفته می شود که در آن یک مولکول خنثی، پس از حل شدن، به یون های باردار تبدیل می گردد؛ اتفاقی که دقیقاً برای مولکول کووالانسی HCl در آب رخ می دهد.
در مقابل، اصطلاح تفکیک بیشتر برای جدا شدن یون هایی به کار می رود که از قبل در یک ترکیب یونی حضور داشته اند، مانند حل شدن نمک طعام و تبدیل آن به یون های سدیم و کلرید. از این رو، برای اسید هیدروکلریک که ذاتاً مولکولی است و هنگام حل شدن یون تولید می کند، به کار بردن واژه یونیزاسیون دقیق تر به نظر می رسد.
با این حال، استفاده از واژه تفکیک برای HCl نیز نادرست محسوب نمی شود، زیرا نتیجه نهایی در هر دو حالت یکی است: تشکیل یون های H₃O⁺ و Cl⁻ در محلول. زمانی که گاز یا مایع HCl وارد آب می شود، هم حل می گردد و هم به یون تبدیل می شود.
در عمل، آنچه اهمیت دارد این است که در محلول آبی، اسید هیدروکلریک به صورت یون های آزاد وجود دارد و نه مولکول های سالم. چه از یونیزه شدن سخن بگوییم و چه از تفکیک، حاصل یک محلول کاملاً یونی است که در آن پیوند H–Cl شکسته شده و گونه های باردار تشکیل شده اند.
چرا اسید هیدروکلریک در آب یونیزه می شود
اسید هیدروکلریک در آب یونیزه می شود زیرا تعاملات بین HCl و مولکول های قطبی آب بسیار قوی است. آب یک حلال بسیار قطبی است؛ اتم اکسیژن آن بار منفی جزئی و اتم های هیدروژن آن بار مثبت جزئی دارند. وقتی HCl وارد آب می شود، قطبیت مولکول اسید کلریدریک و الکترونگاتیوی بالا در آن نقش اساسی دارد، زیرا قطبیت پیوند H–Cl که هیدروژن δ⁺ و کلر δ⁻ دارد با قطبیت آب همسو می گردد.
اکسیژن دارای بار منفی جزئی آب به شدت به هیدروژن با بار مثبت جزئی HCl جذب می شود و در همان زمان هیدروژن های دارای بار مثبت جزئی آب به کلر HCl که بار منفی جزئی دارد کشیده می شوند. این نیروهای جاذبه مولکول HCl را از هم جدا می کند. در نتیجه پیوند H–Cl شکسته می شود؛ پروتون (H⁺) به یک مولکول آب منتقل شده و یون H₃O⁺ را تشکیل می دهد و Cl⁻ توسط مولکول های آب اطراف حلال پوشی و پایدار می گردد.
یون کلرید توسط دوقطبی های آب احاطه کننده پایدار می شود و یون هیدرونیوم نیز به وسیله پیوندهای هیدروژنی با سایر مولکول های آب تثبیت می گردد. علاوه بر این، الکترونگاتیوی بالای عنصر کلر به این معناست که الکترون را نزد خود نگه می دارد و اتم هیدروژن را به صورت H⁺ رها می کند تا به H₂O پیوند دهد. مجموعاً این فرآیند از نظر انرژی به صرفه است، زیرا انرژی آزاد شده از هیدراته شدن یون ها بیشتر از انرژی صرف شده برای شکستن پیوند H–Cl می باشد.
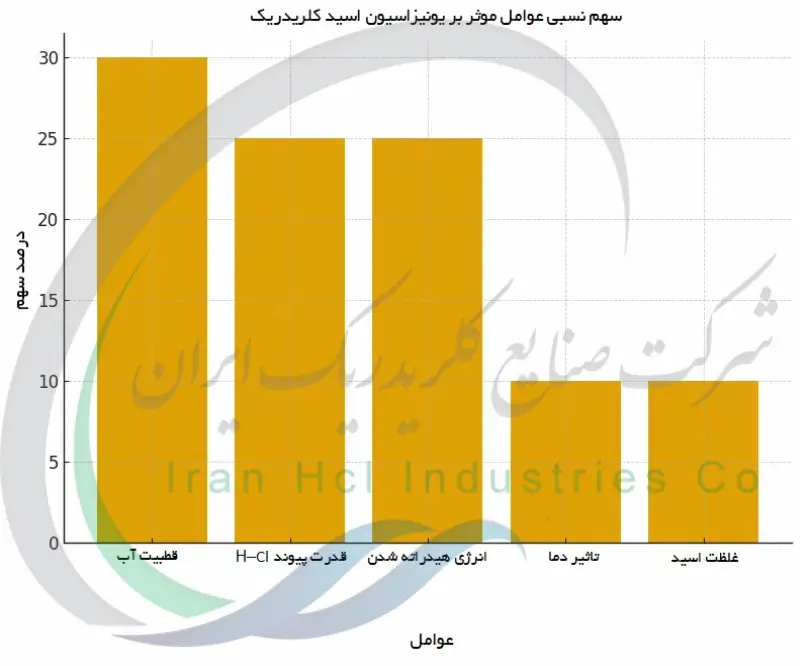
تشکیل یون های هیدرونیوم (H₃O⁺)
یکی از نکات اساسی در یونیزه شدن HCl این است که پروتون های آزاد به تنهایی نمی توانند در آب دوام بیاورند. به محض آنکه اسید هیدروکلریک پروتون خود را رها می کند، این ذره بلافاصله به نزدیک ترین مولکول آب متصل می شود. نتیجه این اتصال، تشکیل یون هیدرونیوم با فرمول H₃O⁺ است که در اصل همان مولکول آب با یک پروتون اضافه محسوب می شود.
در نوشتارهای شیمیایی، برای ساده سازی اغلب این یون را به صورت H⁺ (aq) نشان می دهند، اما در واقعیت پروتون همیشه به آب متصل است و حتی در بسیاری موارد با چند مولکول آب اطراف خود شبکه ای تشکیل می دهد. با این حال، نام هیدرونیوم به عنوان نمایش رایج این حالت به کار می رود.
یون H₃O⁺ دارای بار مثبت است و نقش اصلی را در ایجاد خاصیت اسیدی محلول ایفا می کند. این گونه باردار می تواند پروتون را در محیط آبی پایدار نگه دارد و امکان ادامه واکنش ها را فراهم سازد.
در فرآیندهای خنثی سازی اسید و باز، این یون هیدرونیوم است که پروتون را به ماده بازی منتقل می کند. به طور کلی، بسیاری از ویژگی های اسیدی محلول اسید هیدروکلریک، از خورندگی گرفته تا واکنش پذیری، به حضور و فعالیت یون H₃O⁺ وابسته است.
اسید هیدروکلریک به عنوان یک اسید قوی
اسید هیدروکلریک در گروه اسیدهای قوی قرار می گیرد، یعنی وقتی در آب حل می شود تقریباً به طور کامل به یون های خود تبدیل می گردد. در چنین اسیدی عملاً مولکول سالمی در محلول باقی نمی ماند و نزدیک به صد درصد آن به یون های هیدرونیوم و کلرید تبدیل می شود.
این رفتار کاملاً با اسیدهای ضعیف تفاوت دارد. اسیدهایی مانند اسید استیک یا اسید کربنیک تنها بخشی از مولکول هایشان یونیزه می شوند و هم زمان مولکول های خنثی و یون ها در کنار هم وجود دارند. اما در مورد HCl، واکنش تفکیک تقریباً به طور کامل به سمت تشکیل یون ها پیش می رود و به همین دلیل ثابت تفکیک اسیدی آن بسیار بزرگ در نظر گرفته می شود.
از نظر عملی، اگر محلولی با غلظت ۰٫۱ مولار اسید هیدروکلریک تهیه شود، تقریباً همان مقدار یون هیدرونیوم و یون کلرید در محلول حضور خواهد داشت. این یونیزاسیون کامل باعث می شود محلول های HCl pH بسیار پایینی داشته باشند، رسانایی الکتریکی بالایی نشان دهند و رفتار اسیدی شدیدی از خود بروز دهند.
همین ویژگی سبب می شود محاسبات شیمیایی مربوط به HCl ساده باشد، زیرا می توان فرض کرد هر مولکول آن یک پروتون آزاد می کند.
تأثیر بر pH محلول
یونیزه شدن کامل اسید هیدروکلریک اثر مستقیمی بر مقدار pH محلول دارد. pH به صورت منفی لگاریتم غلظت یون هیدرونیوم تعریف می شود (pH = –log₁₀[H⁺]). چون هر مولکول HCl دقیقاً یک یون H⁺ آزاد می کند، محاسبه pH این محلول ها بسیار ساده است و تنها به دانستن غلظت اسید بستگی دارد.
برای نمونه، در یک محلول ۰٫۱ مولار HCl، غلظت یون هیدروژن تقریباً ۰٫۱ مولار است و pH عددی نزدیک به ۱٫۰ خواهد بود. اگر غلظت به ۰٫۰۱ مولار کاهش یابد، pH به حدود ۲٫۰ می رسد.
در غلظت های بالاتر، شدت اسیدیته بیشتر می شود. یک محلول ۱ مولار HCl دارای pH نزدیک به صفر است و در محلول های بسیار غلیظ تر حتی مقادیر منفی pH نیز دیده می شود.
در مقابل، محلول های بسیار رقیق HCl به pH آب خالص نزدیک می شوند. در مجموع، چون HCl کاملاً تفکیک می شود، pH آن مستقیماً از غلظت اسید پیروی می کند و محاسبه آن بدون پیچیدگی انجام می گیرد.
رسانایی الکتریکی محلول های HCl
از آنجا که اسید هیدروکلریک به طور کامل به یون ها تبدیل می شود، محلول های آبی آن توانایی بالایی در هدایت جریان الکتریسیته دارند. آب خالص به دلیل کمبود یون های آزاد تقریباً رسانا نیست، اما با حل شدن HCl، مقدار زیادی یون هیدرونیوم و کلرید در محلول پخش می شود و عبور بار الکتریکی به سادگی انجام می گیرد.
در آزمایش های عملی، وقتی یک رسانایی سنج یا لامپ درون محلول HCl قرار داده می شود، شدت روشنایی آن بالا است که نشان دهنده رسانایی زیاد این محلول می باشد. حتی محلول های نسبتاً رقیق اسید هیدروکلریک، مانند ۰٫۰۱ مولار، رسانایی بسیار بیشتری نسبت به محلول هم غلظت یک اسید ضعیف مانند اسید استیک دارند.
دلیل این تفاوت آن است که اسیدهای ضعیف تنها بخش کوچکی از مولکول های خود را یونیزه می کنند، در حالی که HCl تقریباً تمام مولکول هایش را به یون تبدیل می سازد. حضور فراوان یون های متحرک H₃O⁺ و Cl⁻ باعث می شود این اسید یک الکترولیت قوی به حساب آید و جریان برق را به خوبی منتقل کند.
ثابت تفکیک اسیدی (Ka) اسید هیدروکلریک
قدرت اسیدها را می توان با عددی به نام ثابت تفکیک اسیدی یا Ka بیان کرد. این عدد نشان می دهد یک اسید تا چه اندازه تمایل دارد در آب یون هیدروژن آزاد کند. به طور کلی، هرچه مقدار Ka بزرگ تر باشد، اسید قوی تر است و راحت تر به یون ها تبدیل می شود.
برای اسید هیدروکلریک، رفتار کاملاً متفاوت از اسیدهای معمولی است. وقتی HCl وارد آب می شود، واکنش آن تقریباً به طور کامل به سمت تشکیل یون های هیدرونیوم و کلرید پیش می رود. به همین دلیل اگر بخواهیم مقدار Ka آن را محاسبه کنیم، با عددی بسیار بزرگ روبه رو می شویم.
برآوردها نشان می دهد pKa اسید هیدروکلریک عددی منفی و در حدود منفی شش تا منفی هفت است. این موضوع یعنی مقدار Ka آن میلیون ها برابر بزرگ تر از اسیدهای ضعیف است و در محلول، تقریباً هیچ مولکول سالمی از HCl باقی نمی ماند.
به دلیل این تفکیک کامل، معمولاً مقدار Ka برای HCl ذکر نمی شود و این اسید به عنوان معیار سنجش قدرت اسیدهای دیگر در نظر گرفته می شود.
مقایسه اسید هیدروکلریک با اسیدهای ضعیف
برای فهم بهتر کامل بودن یونیزاسیون اسید هیدروکلریک، مقایسه آن با اسیدهای ضعیف تر کمک کننده است. اسیدهای قوی مانند HCl در آب تقریباً به طور کامل به یون ها تبدیل می شوند، اما اسیدهای ضعیف فقط بخشی از مولکول های خود را یونیزه می کنند. به زبان ساده، این یعنی در غلظت برابر، یک اسید قوی مقدار بسیار بیشتری یون هیدرونیوم نسبت به یک اسید ضعیف تولید می کند.
به عنوان نمونه، در غلظت ۰٫۱ مولار، اسید هیدروکلریک تقریباً همین مقدار یون H₃O⁺ ایجاد می کند و pH نزدیک به ۱ به دست می آید. در مقابل، اسید استیک با همان غلظت تنها بخش کوچکی یون آزاد می کند و pH آن حدود ۳ است.
این اختلاف در میزان یونیزاسیون باعث تفاوت محسوس در ویژگی هایی مانند اسیدیته و رسانایی الکتریکی می شود. اسیدهای قوی مانند HCl، HBr، HNO₃ و H₂SO₄ تقریباً به طور کامل یونیزه هستند، در حالی که اسیدهایی مثل HF، اسید استیک، اسید کربنیک یا HCN فقط درصد کمی تفکیک می شوند.
همین تفاوت روشن می کند چرا اسید هیدروکلریک در محلول آبی بسیار قوی تر عمل می کند، چون محیط را از یون هیدروژن غنی می سازد، اما اسیدهای ضعیف تنها مقدار محدودی پروتون آزاد می کنند.
| اسید (فرمول) | نوع اسید | pKa | ~٪ یونیزاسیون در ۰٫۱ مولار | pH محلول ۰٫۱ مولار |
|---|---|---|---|---|
| اسید هیدروکلریک (HCl) | قوی | -۷ | ~۱۰۰٪ | ~۱.۰ |
| اسید هیدروبرومیک (HBr) | قوی | -۹ | ~۱۰۰٪ | ~۱.۰ |
| اسید نیتریک (HNO₃) | قوی | -۱.۴ | ~۱۰۰٪ | ~۱.۰ |
| اسید سولفوریک (H₂SO₄) | قوی | -۳ (اول) | ~۱۰۰٪ | ~۰.۹ |
| اسید هیدروفلوئوریک (HF) | ضعیف | ۳.۲ | ~۸٪ | ~۲.۱ |
| اسید استیک (CH₃COOH) | ضعیف | ۴.۸ | ~۱٪ | ~۲.۹ |
| اسید کربنیک (H₂CO₃) | ضعیف | ۶.۳ | ~۰.۲٪ | ~۳.۷ |
| اسید هیدروسیانیک (HCN) | ضعیف | ۹.۲ | ~۰.۱٪ | ~۵.۱ |
تغییرات گرما و انرژی هنگام یونیزاسیون
فرآیند یونیزه شدن HCl در آب نه تنها سریع، بلکه از نظر انرژی نیز قابل توجه است. وقتی هیدروژن کلرید در آب حل شده و تفکیک می شود، گرما آزاد می کند این واکنش گرماده می باشد. این گرما از تشکیل برهمکنش های قوی بین یون ها و مولکول های آب (فرآیند هیدراته شدن) ناشی می شود. شکستن پیوند H–Cl انرژی نیاز دارد، اما پیوند خوردن H⁺ به H₂O و احاطه شدن Cl⁻ توسط آب انرژی بیشتری آزاد می کند.
نتیجه نهایی آزاد شدن انرژی گرمایی در محلول است. اگر اسید هیدروکلریک غلیظ را در آب رقیق کنید، مشاهده می کنید که ظرف محلول گرم می شود. در واقع افزودن HCl غلیظ به آب می تواند محلول را به شدت گرم کند، به همین دلیل در رقیق سازی صحیح باید همیشه اسید را به آرامی به آب اضافه کرد (و نه بالعکس) تا حرارت آزاد شده به طور ایمن پخش گردد. گرماده بودن فرآیند یونیزاسیون HCl نشان می دهد که یون های حاصل در محیط آبی از نظر انرژی پایدارتر از مولکول های اولیه HCl هستند. این تغییر انرژی مطلوب یکی دیگر از دلایلی است که یونیزاسیون HCl به طور کامل پیش می رود.
واکنش های خنثی سازی HCl
اسید هیدروکلریک به سادگی وارد واکنش های خنثی سازی با مواد قلیایی می شود. در این نوع واکنش ها، یون H⁺ که به صورت یون هیدرونیوم در محلول حضور دارد، با یون OH⁻ باز ترکیب شده و آب می سازد، در حالی که اجزای باقی مانده به شکل یک نمک پایدار در محلول می مانند.
به عنوان نمونه رایج، واکنش اسید هیدروکلریک با سدیم هیدروکسید انجام می شود و حاصل آن سدیم کلرید و آب است. اگر واکنش را به صورت یونی بررسی کنیم، بخش اصلی فرآیند ترکیب H⁺ و OH⁻ و تشکیل مولکول آب است و یون های سدیم و کلرید تنها نقش همراه دارند.
از آنجا که HCl یک اسید قوی به شمار می رود، در صورت رعایت نسبت صحیح، واکنش خنثی سازی به طور کامل انجام می شود و اثری از اسید یا باز باقی نمی ماند. این واکنش ها معمولاً با آزاد شدن گرما همراه هستند که نشان دهنده تشکیل محصولات پایدار است.
در کاربردهای عملی، همین ویژگی باعث شده اسید هیدروکلریک برای تنظیم pH، تیتر کردن بازها و واکنش با ترکیبات قلیایی مانند کربنات ها بسیار پرکاربرد باشد. برای مثال، واکنش آن با کربنات کلسیم همراه با آزاد شدن گاز دی اکسید کربن و ایجاد جوشش قابل مشاهده است.
ماهیت خورندگی و اقدامات ایمنی
محلول آبی اسید هیدروکلریک به علت حضور فراوان یون های هیدروژن خاصیت خورندگی شدیدی دارد. این یون ها به راحتی به مواد مختلف حمله می کنند و ساختار آن ها را دچار آسیب می سازند. فلزاتی مانند آهن و روی که واکنش پذیری بالاتری نسبت به هیدروژن دارند، در تماس با این اسید حل می شوند و هم زمان گاز هیدروژن آزاد می گردد.
این اسید برای بافت های زنده نیز بسیار خطرناک است. برخورد آن با پوست یا چشم می تواند در مدت کوتاهی سوختگی شیمیایی جدی ایجاد کند. pH بسیار پایین محلول های HCl باعث می شود موادی مانند بتن، پارچه و برخی سطوح ساختمانی به مرور تخریب شوند. نمونه های غلیظ تر همچنین بخار اسیدی آزاد می کنند که تنفس آن برای دستگاه تنفسی آزاردهنده و زیان آور است.
به همین دلیل رعایت نکات ایمنی هنگام کار با اسید هیدروکلریک اهمیت زیادی دارد. استفاده از دستکش، عینک محافظ و لباس مقاوم ضروری است. هنگام رقیق سازی نیز باید اسید به آب افزوده شود تا از پاشش جلوگیری گردد. تهویه مناسب محیط کار نقش مهمی در کاهش خطرات دارد.
کاربردهای صنعتی و روزمره اسید هیدروکلریک
محلول آبی اسید هیدروکلریک هم در صنعت و هم در زندگی روزمره کاربرد فراوانی دارد و از ویژگی اسیدی قوی و خورنده آن استفاده می شود. یکی از مصرف های مهم این اسید در صنعت فولاد، عملیات اسیدشویی یا پیکلینگ است؛ روشی که برای پاک کردن زنگ و لایه های اکسیدی از سطح آهن و فولاد پیش از ادامه مراحل تولید انجام می گیرد. در این فرایند، HCl اکسیدهای فلزی را حل می کند و سطح فلز را آماده می سازد.
اسید هیدروکلریک در ساخت بسیاری از مواد شیمیایی نیز نقش دارد؛ از جمله در تولید ترکیبات آلی کلردار یا بازسازی رزین های تبادل یونی. در حفاری چاه های نفت، این اسید به داخل سازند تزریق می شود تا سنگ آهک را حل کرده و جریان نفت را بهتر کند.
در مصارف خانگی، محلول رقیق آن که به نام جوهر نمک شناخته می شود، برای پاک کردن رسوبات معدنی، زنگ زدگی و لکه ها به کار می رود. همچنین برای کاهش pH آب استخر و در برخی فرایندهای غذایی مانند تولید ژلاتین استفاده می شود.
اسید هیدروکلریک در معده انسان
اسید هیدروکلریک فقط محدود به آزمایشگاه ها نیست و به طور طبیعی در بدن انسان هم حضور دارد. معده برای انجام وظیفه خود شیره ای اسیدی ترشح می کند که بخش اصلی آن HCl است و غلظتی در حدود ۰٫۱ مولار دارد. این محیط اسیدی با pH نزدیک ۱ تا ۲ شرایط لازم برای هضم مناسب غذا را فراهم می سازد.
در فضای آبی معده، اسید هیدروکلریک کاملاً به یون ها تبدیل می شود و یون های هیدرونیوم نقش اصلی را بر عهده دارند. این یون ها باعث فعال شدن آنزیم هایی مانند پپسین می شوند و تجزیه پروتئین ها را آسان تر می کنند. افزون بر این، اسیدیته بالا بسیاری از باکتری ها و عوامل بیماری زا را که همراه غذا وارد بدن می شوند از بین می برد.
برای جلوگیری از آسیب، دیواره معده با لایه ای مخاطی محافظت می شود و مواد قلیایی مانند بی کربنات ترشح می گردد تا تماس مستقیم اسید با بافت کاهش یابد. اگر این تعادل به هم بخورد یا اسید به مری بازگردد، خاصیت خورنده HCl می تواند موجب سوزش و التهاب شود. داروهای ضداسید با کاهش یا خنثی کردن همین اسید عمل می کنند و تعادل را دوباره برقرار می سازند.




