فهرست عناوین
- مقدمه
- اسید هیدروکلریک چیست؟
- فرمول شیمیایی اسید هیدروکلریک
- وزن مولکولی اسید هیدروکلریک
- ترکیب و ساختار مولکول های HCl
- محاسبه جرم مولی HCl
- خواص فیزیکی اسید هیدروکلریک
- خواص شیمیایی و واکنش های اسید هیدروکلریک
- اسید هیدروکلریک در محلول آبی
- تولید صنعتی اسید هیدروکلریک
- کاربردهای رایج اسید هیدروکلریک
- اسید هیدروکلریک در آزمایشگاه
- نقش بیولوژیکی اسید هیدروکلریک
- ایمنی و احتیاطات کار با اسید هیدروکلریک
- تاریخچه کشف اسید هیدروکلریک
- اسید هیدروکلریک در مقایسه با سایر اسیدها
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 15-08-1404
تاریخ بروزرسانی مقاله : 15-08-1404
تعداد کلمات : 3200
آدرس مقاله : لینک مقاله
فرمول مولکولی و جرم مولکولی اسید کلریدریک

مقدمه
اسید هیدروکلریک که با نام هایی مانند اسید کلریدریک، موریاتیک یا جوهر نمک هم شناخته می شود، یکی از مهم ترین مواد شیمیایی پرمصرف در سراسر جهان به شمار می آید. این ماده معدنی یک اسید قوی و به شدت خورنده است که بوی تند و مشخصی دارد و به راحتی قابل تشخیص است.
فرمول مولکولی این اسید HCl است و نشان می دهد هر مولکول از یک اتم هیدروژن و یک اتم کلر تشکیل شده است. وزن مولکولی اسید هیدروکلریک در حدود ۳۶٫۴۶ گرم بر مول می باشد و همین ترکیب ساده، رفتار شیمیایی بسیار فعالی به آن می دهد.
به عنوان یک اسید قوی، اسید هیدروکلریک هنگام حل شدن در آب به طور کامل یونیزه می شود و یون های هیدروژن (H⁺) و کلرید (Cl⁻) آزاد می کند. همین ویژگی عامل اصلی اسیدیته بالا و واکنش پذیری شدید این ماده در برابر بسیاری از ترکیبات است.
اسید هیدروکلریک کاربردهای گسترده ای در صنایع گوناگون، آزمایشگاه های علمی و حتی در سیستم گوارش انسان دارد و نقش های متفاوتی ایفا می کند. در ادامه مقاله، موضوعاتی مانند فرمول و وزن مولکولی، ساختار، ویژگی ها، شیوه های تولید، موارد مصرف، نکات ایمنی و تاریخچه این اسید به طور کامل بررسی خواهد شد.
اسید هیدروکلریک چیست؟
اسید هیدروکلریک (HCl) یک مولکول ساده دو اتمی و یک اسید معدنی متداول است که به داشتن خاصیت خورندگی بسیار قوی معروف می باشد. در حالت خالص به صورت هیدروژن کلرید گازی وجود دارد؛ گازی بی رنگ که به دلیل تمایل شدید به آب در هوای مرطوب دود ایجاد می کند. هنگامی که گاز هیدروژن کلرید در آب حل می شود، اسید هیدروکلریک را تشکیل می دهد که معمولاً به صورت یک محلول مایع شفاف و بی رنگ دیده می شود.
خرید اسید کلریدریک سمنان در میان صنایع مختلف ایران، به ویژه در حوزه های تصفیه آب، فلزکاری و تولید مواد شیمیایی، بسیار رایج است؛ زیرا این اسید با قدرت واکنش پذیری بالا و خلوص مناسب، در فرآیندهای صنعتی نقش کلیدی دارد. این اسید به عنوان یک اسید قوی طبقه بندی می شود زیرا در آب به طور کامل یونش یافته و یون های هیدروژن آزاد می کند. اسید هیدروکلریک بوی تند و تیزی دارد و برای فلزات و بافت های زنده بسیار خورنده است.
این اسید در غلظت های مختلفی عرضه می گردد؛ برای مثال، نوع تجاری آن که موریاتیک اسید نام دارد معمولاً حاوی حدود ۳۰٪ تا ۳۵٪ HCl است. این اسید به طور طبیعی در معده انسان و بسیاری حیوانات به صورت اسید معده حضور دارد و با تجزیه غذا به فرآیند هضم کمک می کند. به طور خلاصه، اسید هیدروکلریک یک ماده شیمیایی اساسی با ترکیب شیمیایی ساده اما رفتار اسیدی بسیار قوی در محلول آبی است.
فرمول شیمیایی اسید هیدروکلریک
فرمول شیمیایی اسید هیدروکلریک HCl نوشته می شود. این فرمول بیانگر مولکولی است که از پیوند یک اتم هیدروژن (H) با یک اتم کلر (Cl) به وجود آمده است. HCl جزو ساده ترین ساختارهای اسیدی به شمار می رود، زیرا تنها از دو اتم تشکیل شده است. نسبت یک به یک هیدروژن و کلر در این فرمول، اجزای سازنده آن را به شکل واضح نشان می دهد.
در نگارش علمی، برای مشخص کردن حالت فیزیکی، گاهی اسید هیدروکلریک محلول در آب را به صورت HCl (aq) نمایش می دهند، در حالی که حالت گازی آن با HCl (g) نشان داده می شود. با این حال، هر دو نماد به یک ماده شیمیایی اشاره دارند و تفاوت آن ها فقط در حالت فیزیکی است.
پیوند موجود بین اتم های هیدروژن و کلر در مولکول HCl از نوع کووالانسی قطبی است. در این پیوند، اتم کلر به دلیل الکترونگاتیوی بالاتر، الکترون های مشترک را بیشتر به سمت خود جذب می کند. همین قطبی بودن پیوند سبب می شود اسید هیدروکلریک در آب رفتار اسیدی بسیار قوی از خود نشان دهد و به راحتی یونیزه شود.
در مجموع، فرمول مولکولی HCl ساختار ساده اسید هیدروکلریک را توصیف می کند و نشان می دهد که هر مولکول این اسید تنها از همین دو عنصر تشکیل شده است.
وزن مولکولی اسید هیدروکلریک
وزن مولکولی اسید هیدروکلریک حدود ۳۶٫۴۶ واحد جرم اتمی است که برابر با ۳۶٫۴۶ گرم بر مول در نظر گرفته می شود. این عدد از جمع جرم اتمی عناصر سازنده مولکول HCl به دست می آید. اتم هیدروژن جرمی در حدود ۱٫۰۰۸ دارد و اتم کلر دارای جرم اتمی نزدیک به ۳۵٫۴۵ است.
وقتی این دو مقدار با هم جمع می شوند، وزن مولکولی HCl عددی نزدیک به ۳۶٫۴۵۸ به دست می دهد که برای سهولت محاسبات معمولاً به ۳۶٫۴۶ g/mol گرد می شود. وزن مولکولی یکی از ویژگی های پایه ای هر ماده است و نشان می دهد یک مول از آن ماده چه جرمی دارد.
در مورد اسید هیدروکلریک، این موضوع به این معناست که یک مول HCl جرمی در حدود ۳۶٫۴۶ گرم خواهد داشت. این عدد در آماده سازی محلول ها و انجام محاسبات شیمیایی نقش مهمی ایفا می کند، زیرا به شیمیدانان کمک می کند مقدار مشخصی از HCl را برای واکنش ها و بررسی های آزمایشگاهی به درستی اندازه گیری کنند.
ترکیب و ساختار مولکول های HCl
هر مولکول اسید هیدروکلریک ترکیب و ساختار ساده ای دارد و از یک اتم هیدروژن و یک اتم کلر تشکیل شده است؛ موضوعی که در ساختار پیوندی و شکل مولکولی اسید کلریدریک به وضوح دیده می شود. پیوند میان H و Cl یک پیوند کووالانسی یگانه است، اما به شدت قطبی محسوب می شود زیرا الکترونگاتیوی کلر بسیار بیشتر از هیدروژن است. همین اختلاف باعث می شود الکترون های اشتراکی به سمت کلر کشیده شده و مولکول H–Cl دارای بار جزئی مثبت در سمت هیدروژن و بار جزئی منفی در سمت کلر شود.
از نظر هندسی، مولکول HCl کاملاً خطی است و طول پیوند آن حدود ۱۲۷ پیکومتر اندازه گیری می شود. بخش عمده جرم مولکول نیز مربوط به اتم کلر است، چون سنگین تر از هیدروژن می باشد. این ساختار ساده دو اتمی در آب به راحتی متلاشی شده و به یون های H⁺ و Cl⁻ تبدیل می شود که دلیل اسیدیته بسیار قوی اسید کلریدریک است.
محاسبه جرم مولی HCl
محاسبه جرم مولی HCl با توجه به ساختار ساده آن کار دشواری نیست. برای به دست آوردن وزن مولکولی اسید هیدروکلریک، کافی است جرم اتمی اجزای تشکیل دهنده را با یکدیگر جمع کنیم. طبق جدول تناوبی، اتم هیدروژن جرمی در حدود ۱٫۰۰۸ دارد و اتم کلر دارای جرم اتمی تقریبی ۳۵٫۴۵ است. با جمع این دو عدد، مقدار ۳۶٫۴۵۸ حاصل می شود که به طور معمول به صورت ۳۶٫۴۶ گرم بر مول گرد می گردد. در نتیجه، یک مول HCl جرمی نزدیک به ۳۶٫۴۶ گرم خواهد داشت. شیمیدانان از این روش برای تعیین دقیق مقدار اسید هیدروکلریک در واکنش های شیمیایی استفاده می کنند. برای نمونه، اگر یک واکنش به ۰٫۱ مول HCl احتیاج داشته باشد، می توان جرم لازم را با ضرب ۳۶٫۴۶ در ۰٫۱ محاسبه کرد که تقریبا برابر با ۳٫۶۴۶ گرم HCl خالص است.
خواص فیزیکی اسید هیدروکلریک
اسید هیدروکلریک خالص در حالت گاز هیدروژن کلرید، ماده ای بی رنگ و غیرقابل اشتعال با بویی تند و آزاردهنده به شمار می رود. زمانی که این گاز در آب حل می شود، به صورت اسید هیدروکلریک در می آید و محلولی شفاف و بدون رنگ به وجود می آورد. یکی از خصوصیات فیزیکی شاخص اسید هیدروکلریک غلیظ، دود کردن آن در هوای آزاد است؛ این محلول بخار HCl آزاد می کند که هنگام برخورد با رطوبت هوا، مه ای سفید رنگ ایجاد می کند.
خود گاز HCl از هوا سنگین تر است و قابلیت حل شدن بسیار بالایی در آب دارد. نقطه جوش و نقطه انجماد محلول های اسید هیدروکلریک با توجه به غلظت آن ها تغییر می کند؛ یک ترکیب آزئوتروپ با حدود ۲۰٪ HCl در دمایی نزدیک به ۱۱۰ درجه سانتی گراد به جوش می آید. در مقابل، هیدروژن کلرید خالص دارای نقطه جوش منفی ۸۵ و نقطه ذوب منفی ۱۱۴ درجه سانتی گراد در فشار استاندارد است.
محلول های غلیظ اسید هیدروکلریک چگالی تقریبی بین ۱٫۱۸ تا ۱٫۱۹ دارند و خاصیت خورندگی بسیار شدیدی از خود نشان می دهند. به طور کلی، اسید هیدروکلریک در حالت محلول یک مایع است که به شدت در آب حل می شود، بخارات خفه کننده آزاد می کند و ویژگی های فیزیکی رایج یک اسید قوی را داراست.
خواص شیمیایی و واکنش های اسید هیدروکلریک
اسید هیدروکلریک رفتار شیمیایی رایج یک اسید قوی و غیر اکسیدکننده را از خود نشان می دهد. این ماده با ترکیبات قلیایی به سرعت وارد واکنش می شود و در فرآیندهای خنثی سازی، نمک و آب به وجود می آورد. برای مثال، HCl با سدیم هیدروکسید واکنش داده و سدیم کلرید به همراه آب تولید می کند. به همین شکل، با اکسیدها و هیدروکسیدهای فلزی واکنش انجام می دهد و نمک های کلرید محلول تشکیل می شوند.
اسید هیدروکلریک با بسیاری از فلزات نیز واکنش شدیدی دارد که در جریان آن گاز هیدروژن آزاد می شود. نمونه شناخته شده این واکنش مربوط به فلز روی است:
Zn + 2 HCl → ZnCl₂ + H₂↑ .
همچنین در واکنش با کربنات ها و بی کربنات ها، این اسید باعث آزاد شدن گاز دی اکسید کربن شده و هم زمان آب و نمک های کلرید محلول ایجاد می کند.
برخلاف اسیدهای اکسیدکننده، اسید هیدروکلریک خالص معمولاً توانایی حل کردن فلزات نجیب مانند طلا یا پلاتین را ندارد، مگر اینکه یک عامل اکسنده در محیط حضور داشته باشد. یون کلریدی که در این واکنش ها شکل می گیرد اغلب نقش تماشاچی دارد، هرچند در برخی شرایط می تواند با بعضی کاتیون ها ترکیب شده و رسوبات کلرید نامحلول بسازد.
در مجموع، رفتار شیمیایی اسید هیدروکلریک بر پایه ویژگی های یک اسید قوی تعریف می شود: انتقال پروتون به بازها، آزادسازی گاز در واکنش با فلزات یا کربنات ها، و تشکیل نمک های کلرید در واکنش های گوناگون.
اسید هیدروکلریک در محلول آبی
در محیط آبی، اسید هیدروکلریک ویژگی های مشخص یک اسید قوی را بروز می دهد و به طور کامل به اجزای یونی خود تجزیه می شود. هر مولکول HCl که در آب حل می گردد، یک یون هیدروژن H⁺ آزاد می کند که بلافاصله به صورت یون هیدرونیوم H₃O⁺ در می آید و در کنار آن یک یون کلرید (Cl⁻) نیز تشکیل می شود. به دلیل این تفکیک کامل، حتی محلول های نسبتا رقیق اسید هیدروکلریک هم دارای pH بسیار پایینی هستند.
یک محلول غلیظ اسید هیدروکلریک، با غلظتی در حدود ۳۷ درصد وزنی یا نزدیک به ۱۲ مولار، آن قدر خاصیت اسیدی بالایی دارد که مقدار pH آن می تواند به ناحیه منفی برسد. هنگام آماده سازی یا رقیق کردن محلول های HCl باید توجه داشت که این فرایند همراه با آزاد شدن گرماست؛ به همین دلیل روش ایمن این است که اسید به آب افزوده شود تا از جوشش ناگهانی و پاشش جلوگیری گردد.
در محلول آبی، عملا مولکول HCl به صورت خنثی باقی نمی ماند و تقریبا به طور کامل به یون های H₃O⁺ و Cl⁻ تبدیل می شود. همین تفکیک کامل در آب علت اصلی قدرت اسیدی بالای HCl است و باعث می شود این ماده در محلول به عنوان یک الکترولیت قوی شناخته شود.
تولید صنعتی اسید هیدروکلریک
اسید هیدروکلریک به شکل صنعتی از چند مسیر مختلف تهیه می شود. یکی از روش های رایج امروزی، تولید مستقیم HCl از عناصر سازنده آن است؛ در این شیوه گاز هیدروژن با گاز کلر واکنش می دهد و گاز هیدروژن کلرید تشکیل می شود، سپس این گاز در آب حل شده و اسید هیدروکلریک به دست می آید. این روش محصولی با خلوص بالا ایجاد می کند و زمانی به کار می رود که اسید بسیار خالص مورد نیاز باشد.
منبع مهم دیگر برای تولید HCl، حاصل شدن آن به عنوان محصول جانبی در فرایند ساخت ترکیبات آلی کلردار است. برای نمونه، در تولید پلی وینیل کلراید (PVC) یا تفلون، مقدار زیادی گاز هیدروژن کلرید آزاد می شود که با جذب آن می توان اسید هیدروکلریک تولید کرد.
در گذشته، اسید هیدروکلریک از واکنش سدیم کلرید با اسید سولفوریک به دست می آمد که این روش با نام فرایند مانهایم شناخته می شود. همچنین در دوران انقلاب صنعتی، فرایند لبلاک برای تولید کربنات سدیم باعث آزاد شدن HCl به عنوان محصول فرعی می شد.
امروزه اسید هیدروکلریک در حجم بسیار بالا تولید و مصرف می گردد و معمولا به صورت محلول آبی با غلظتی تا حدود ۳۷ درصد در بازار عرضه می شود.
کاربردهای رایج اسید هیدروکلریک
اسید هیدروکلریک در دامنه وسیعی از صنایع مختلف و حتی کاربردهای روزمره مورد استفاده قرار دارد. در صنعت فلزات، یکی از مهم ترین موارد مصرف آن اسیدشویی فولاد است؛ یعنی حذف زنگ زدگی و لایه های اکسیدی از سطح آهن یا فولاد پیش از انجام فرایندهایی مانند گالوانیزه کردن. HCl با این لایه های اکسیدی وارد واکنش شده و سطح فلز را پاک سازی می کند.
این اسید در تولید ترکیبات غیرآلی نیز نقش مهمی ایفا می کند؛ زیرا می تواند فلزات، اکسیدهای فلزی و کربنات ها را حل کرده و کلریدهای محلول آن ها را به وجود آورد. در صنایع شیمیایی، اسید هیدروکلریک به عنوان ماده واکنش دهنده در سنتز آلی و همچنین برای تنظیم pH محیط به کار گرفته می شود.
یکی دیگر از کاربردهای مهم آن در تصفیه آب و نگهداری استخرهاست؛ به این صورت که HCl به آب افزوده می شود تا میزان قلیاییت و pH در محدوده مناسب کنترل گردد. در صنعت غذا نیز اسید هیدروکلریک با گرید خوراکی در تولید محصولاتی مانند شربت گلوکز و ژلاتین استفاده می شود.
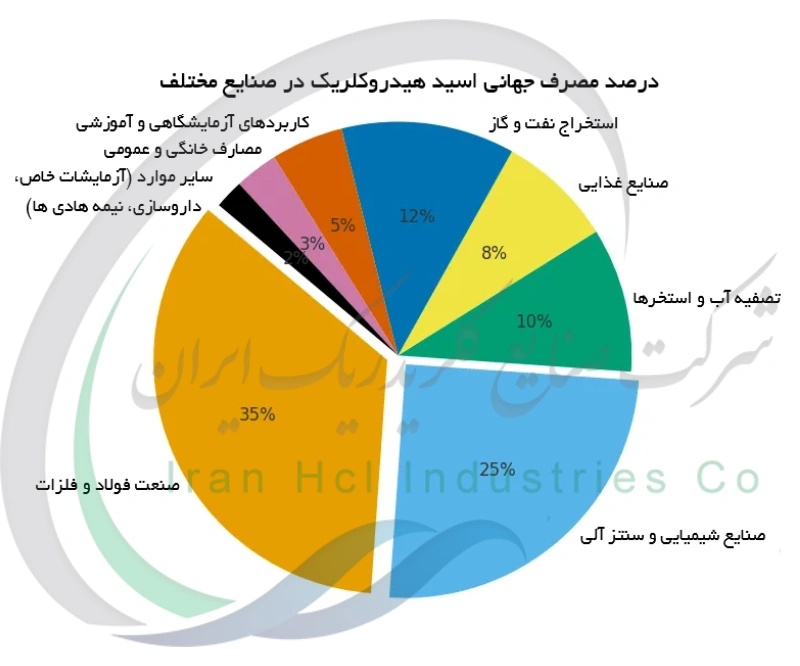
در بخش استخراج نفت و گاز، این اسید را به درون چاه ها تزریق می کنند تا رسوبات معدنی حل شده و جریان سیالات بهبود پیدا کند. در مصارف خانگی هم شکل رقیق شده آن برای از بین بردن لکه های معدنی سخت به کار می رود، هرچند استفاده از آن نیازمند دقت و رعایت نکات ایمنی است.
اسید هیدروکلریک در آزمایشگاه
در محیط های آزمایشگاهی، اسید هیدروکلریک به عنوان یک ماده واکنش دهنده پایه شناخته می شود که به علت قدرت اسیدی بالا و ساختار ساده خود کاربرد فراوانی دارد. این اسید معمولا در تیتر کردن های اسید و باز به عنوان اسید مرجع استفاده می شود، چون تک پروتونی است و در واکنش های خنثی سازی با بازها نقطه پایانی مشخص و قابل تشخیص ایجاد می کند. محلول HCl با غلظت معلوم می تواند برای اندازه گیری دقیق مقدار باز موجود در یک نمونه، از طریق تیتر کردن، به کار گرفته شود.
علاوه بر این، اسید هیدروکلریک در آزمایش های تجزیه ای برای اسیدی کردن محلول ها مورد استفاده قرار می گیرد و در حل کردن ترکیباتی مانند کربنات ها و هیدروکسیدها نقش دارد. از آنجایی که HCl به جز یون کلرید، یون اضافی دیگری وارد محلول نمی کند، در شرایطی که وجود کلرید ایجاد مشکل نکند، انتخاب مناسبی به شمار می رود.
همچنین از اسید هیدروکلریک رقیق برای پاک سازی شیشه آلات آزمایشگاهی استفاده می شود که البته پس از آن باید شستشوی کامل انجام گیرد. پایداری نسبی محلول های HCl و در دسترس بودن آسان آن باعث شده است این اسید به گزینه ای مناسب و نسبتا ایمن برای بسیاری از فعالیت های آزمایشگاهی تبدیل شود.
نقش بیولوژیکی اسید هیدروکلریک
اسید هیدروکلریک نقش مهمی در زیست شناسی ایفا می کند که شناخته شده ترین آن در دستگاه گوارش انسان و بسیاری جانوران است. معده مقادیر قابل توجهی اسید معده ترشح می کند که عمدتاً از HCl رقیق تشکیل شده است (حدود ۰٫۵٪). این محیط اسیدی کردن محتویات معده تا pH حدود ۱ تا ۲ برای فعال سازی آنزیم های گوارشی مانند پپسین ضروری است. محیط بسیار اسیدی همچنین به جذب برخی مواد مغذی مانند آهن و کلسیم کمک می کند.
علاوه بر کمک به هضم، اسیدیته بالا به عنوان مکانیزم دفاعی عمل کرده و بسیاری از میکروارگانیسم ها را از بین می برد. بدن ترشح HCl را از طریق سلول های جداری تنظیم می کند و در پاسخ به غذا اسید آزاد می کند. عدم تعادل در تولید HCl می تواند منجر به مشکلاتی مانند رفلاکس اسید یا زخم معده شود. در کل اسید هیدروکلریک برای هضم مناسب و دفاع ایمنی در معده حیاتی است.
ایمنی و احتیاطات کار با اسید هیدروکلریک
اسید هیدروکلریک غلیظ ماده ای پرخطر به شمار می رود و استفاده از آن نیازمند دقت بالاست. خاصیت خورنده این اسید می تواند در صورت تماس با پوست یا چشم، سوختگی های جدی ایجاد کند و بخارهای آن نیز برای سیستم تنفسی زیان آور است. هنگام کار با HCl استفاده از دستکش مناسب، عینک محافظ و پوشش ایمنی کاملا ضروری می باشد. انجام هرگونه فعالیت با این اسید باید در فضایی با تهویه کافی صورت گیرد.
در زمان رقیق سازی، لازم است همیشه اسید به آب افزوده شود تا از بروز واکنش گرمازای ناگهانی و پاشش جلوگیری گردد. نشت های جزئی را می توان با به کارگیری یک ماده قلیایی مناسب خنثی کرده و سپس جمع آوری نمود، اما نشت های گسترده تر نیازمند اقدامات تخصصی هستند.
اسید هیدروکلریک باید در ظروف مقاوم و دارای درب محکم نگهداری شود و تحت هیچ شرایطی نباید با موادی مانند وایتکس یا پرمنگنات ها ترکیب گردد، زیرا امکان آزاد شدن گاز کلر وجود دارد. با رعایت دقیق اصول ایمنی، کار با این اسید بدون حادثه انجام می شود، اما توجه و احتیاط همیشگی شرط اصلی است.
تاریخچه کشف اسید هیدروکلریک
پیشینه شناسایی و به کارگیری اسید هیدروکلریک به سال های ابتدایی شکل گیری علم شیمی بازمی گردد. در دوره قرون وسطی، شیمیدانانی مانند زکریای رازی با گرم کردن ترکیب هایی از نمک و سولفات ها، به احتمال زیاد گاز هیدروژن کلرید تولید می کردند. در ادامه، تیزاب سلطانی که مخلوطی از نیتریک اسید و نشادر بود، برای حل طلا مورد استفاده قرار گرفت و در عمل HCl را در همان فرایند ایجاد می کرد.
نخستین گزارش های روشن درباره جداسازی اسید هیدروکلریک خالص به اواخر قرن شانزدهم و اوایل قرن هفدهم بازمی گردد. در این دوره، شیمیدانانی مانند گلابر و لیباویوس با واکنش دادن نمک و اسید سولفوریک توانستند این اسید را تولید کنند که آن زمان با نام روح نمک شناخته می شد.
با آغاز انقلاب صنعتی، اسید هیدروکلریک به صورت گسترده به عنوان محصول جانبی فرایند لبلاک در تولید کربنات سدیم به دست می آمد. در قرن نوزدهم، وضع قوانین زیست محیطی باعث شد جمع آوری، جذب و فروش این ماده رواج بیشتری پیدا کند.
از آن دوران تا امروز، اسید هیدروکلریک همواره به عنوان یکی از مواد پایه و اساسی در صنایع گوناگون و محیط های آزمایشگاهی جایگاه خود را حفظ کرده است.
اسید هیدروکلریک در مقایسه با سایر اسیدها
اسید هیدروکلریک را می توان از نظر قدرت، ترکیب و خواص با چند اسید دیگر مقایسه کرد. به عنوان یک اسید قوی تک پروتونی، HCl در آب کاملاً تفکیک می شود؛ اسید سولفوریک دو پروتونی است و مایع غلیظ به شمار می رود، در حالی که HCl در شکل خالص گاز است. نیتریک اسید اکسیدکننده قوی است ولی HCl غیراکسیدکننده می باشد.. HCl فرارتر از بسیاری از اسیدهای قوی است و به آسانی دود می کند. در میان اسیدهای هالوژنه، HCl قوی است هرچند HBr و HI قوی تر هستند، و HF ضعیف تر ولی بسیار خطرناک است. جدول زیر چند مقایسه کلیدی را نشان می دهد:
| نام اسید | فرمول شیمیایی | وزن مولکولی (g/mol) | قدرت اسیدی (pKa) | نقطه جوش (°C) |
|---|---|---|---|---|
| اسید هیدروکلریک | HCl | ۳۶٫۴۶ | -۶٫۰ | -۸۵ |
| اسید سولفوریک | H₂SO₄ | ۹۸٫۰۸ | -۳٫۰ | ۳۳۷ |
| اسید نیتریک | HNO₃ | ۶۳٫۰۱ | -۱٫۴ | ۸۳ |
| اسید هیدروبرومیک | HBr | ۸۰٫۹۱ | -۹٫۰ | -۶۷ |
| اسید هیدرویدیک | HI | ۱۲۷٫۹۱ | -۱۰ | -۳۵ |
| اسید هیدروفلوئوریک | HF | ۲۰٫۰۱ | ۳٫۲ | ۱۹٫۵ |
| اسید پرکلریک | HClO₄ | ۱۰۰٫۴۶ | -۱۰ | ۲۰۳ |
| اسید استیک | CH₃COOH | ۶۰٫۰۵ | ۴٫۷۶ | ۱۱۸ |





بررسی خواص فیزیکی و فرمول شیمیایی اسید کلریدریک (HCL) و اجزای آن
بررسی اهمیت جرم مولکولی اسید کلریدریک و محاسبه آن و استفاده در آزمایشگاه
بررسی اهمیت پیکربندی الکترونی اتم های سازنده اسید کلریدریک و ترکیب آن
مقایسه جرم مولکولی اسید کلریدریک با سایر ترکیبات ساده و اهمیت تفاوت های جرم مولکولی