فهرست عناوین
- مقدمه
- فرمول شیمیایی و ترکیب اسید هیدروکلریک (HCl)
- هیدروژن کلراید در مقابل اسید هیدروکلریک
- هیدروژن: جزء H در HCl
- کلر: جزء Cl در HCl
- تشکیل و سنتز اسید هیدروکلریک
- خواص فیزیکی اسید هیدروکلریک
- خواص شیمیایی و واکنش های HCl
- غلظت و گریدهای محلول های HCl
- کاربردهای صنعتی اسید هیدروکلریک
- کاربردهای روزمره اسید هیدروکلریک
- اسید هیدروکلریک در بدن انسان
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 29-08-1404
تاریخ بروزرسانی مقاله : 29-08-1404
تعداد کلمات : 3100
آدرس مقاله : لینک مقاله
فرمول شیمیایی اسید کلریدریک (HCL) و اجزای آن

مقدمه
اسید هیدروکلریک با فرمول HCl یک اسید معدنی بسیار قوی و خورنده است که در صنعت، علوم و حتی بدن انسان نقش مهمی دارد. این ماده که به نام جوهر نمک نیز شناخته می شود، در اصل یک محلول آبی از گاز هیدروژن کلراید است. فرمول شیمیایی HCl نشان می دهد که هر مولکول آن از یک اتم هیدروژن و یک اتم کلر تشکیل شده است.
ترکیب این دو عنصر یک اسید بسیار واکنش پذیر را ایجاد می کند که در آب به طور کامل به یون های تشکیل دهنده ی آن تفکیک می شود (یون هیدروژن و یون کلرید). اسید هیدروکلریک محلولی بی رنگ با بوی تند و زننده است و در غلظت های بالا بخارات اسیدی خطرناک از آن متصاعد می گردد. این اسید به طور طبیعی در شیره معده انسان و بسیاری از جانوران وجود دارد و به هضم غذا و نابودی میکروب های مضر کمک می کند.
در صنایع مختلف نیز، اسید هیدروکلریک در بسته بندی های متنوع مورد استفاده قرار می گیرد و خرید اسید کلریدریک کلر پارس تبریز گالن 20 لیتری یکی از گزینه های رایج برای مصرف کنندگان صنعتی و کارگاه هایی است که نیاز به حجم متوسط و حمل آسان این ماده دارند. به صورت صنعتی، HCl در حجم عظیم تولید می شود و در کاربردهایی از قبیل تصفیه فلزات، سنتز مواد شیمیایی و تنظیم pH به کار می رود. در بخش های بعدی به طور جامع به فرمول و اجزای تشکیل دهنده ی اسید هیدروکلریک، خواص فیزیکی و شیمیایی آن، روش های تولید، کاربردها، نکات ایمنی، تاثیرات زیست محیطی و پیشینه تاریخی این ماده مهم می پردازیم.
فرمول شیمیایی و ترکیب اسید هیدروکلریک (HCl)
فرمول مولکولی اسید هیدروکلریک HCl است که نشان دهنده ترکیب یک به یک اتم های هیدروژن (H) و کلر (Cl) است. HCl یک مولکول دواتمی ساده است و در فاز گازی (کلرید هیدروژن) به صورت مولکول های مجزا وجود دارد. پیوند بین اتم هیدروژن و کلر در این مولکول از نوع کووالانسی است، اما به دلیل الکترونگاتیوی بالای کلر، این پیوند قطبی است؛ به طوری که اتم هیدروژن بار جزئی مثبت و اتم کلر بار جزئی منفی پیدا می کند.
قطبیت پیوند H–Cl علت رفتار اسیدی این ماده است، زیرا مولکول HCl می تواند در آب به آسانی یونیزه شده و یک پروتون (H^+) و یک یون کلرید (Cl^-) آزاد کند. در مباحث آموزشی شیمی، زمانی که درباره جرم مولکولی اسید کلریدریک و محاسبه آن صحبت می شود، معمولاً همین ساختار دو اتمی و نقش اختلاف جرم میان عناصر تشکیل دهنده مورد تأکید قرار می گیرد. جرم مولکولی HCl حدود ۳۶٫۴۶ گرم بر مول است که بخش عمده آن ناشی از اتم کلر است.
به عبارتی، از نظر جرمی، حدود ۹۷٪ این ترکیب را کلر و تنها ۳٪ آن را هیدروژن تشکیل می دهد. فرمول شیمیایی HCl در هر حالت ماده (گاز یا محلول در آب) به همین صورت باقی می ماند، هرچند خصوصیات آن بسته به حالت (به شکل گاز هیدروژن کلراید یا محلول اسید هیدروکلریک) متفاوت خواهد بود. این فرمول مختصر ماهیت پایه ای ترکیب و حضور دو عنصر هیدروژن و کلر را در ساختار آن نشان می دهد.
هیدروژن کلراید در مقابل اسید هیدروکلریک
در نگاه اول، هیدروژن کلراید و اسید هیدروکلریک یک چیز به نظر می رسند، چون هر دو از یک فرمول شیمیایی یعنی HCl استفاده می کنند. اما واقعیت این است که این دو اصطلاح به یک ماده در شرایط متفاوت اشاره دارند و همین تفاوت شرایط باعث تغییر رفتار و کاربرد آن ها می شود. شناخت این تفاوت، به ویژه برای مصرف کنندگان و فعالان صنعتی، اهمیت زیادی دارد.
هیدروژن کلراید به شکل خالص خود، یک گاز است. این گاز در دمای معمولی محیط، بی رنگ و دارای بویی تند و آزاردهنده است. تا زمانی که این گاز به صورت خشک باقی بماند و با آب تماس نداشته باشد، خاصیت اسیدی واقعی از خود نشان نمی دهد و رسانای جریان الکتریکی هم نیست. به همین دلیل، HCl گازی به تنهایی یک اسید فعال محسوب نمی شود.
اما زمانی که گاز هیدروژن کلراید وارد آب می شود، شرایط کاملا تغییر می کند. در این حالت، مولکول های HCl در آب شکسته شده و به یون های مثبت هیدروژن و یون های منفی کلر تبدیل می شوند. نتیجه این فرآیند، تشکیل اسید هیدروکلریک است؛ مایعی بسیار اسیدی، خورنده و با قدرت واکنش بالا که pH آن می تواند به مقادیر بسیار پایین و حتی منفی برسد.
یکی از ویژگی های جالب گاز HCl این است که در مجاورت هوای مرطوب، به سرعت بخار آب را جذب می کند. این جذب رطوبت باعث تشکیل قطرات بسیار ریز اسید هیدروکلریک می شود که به صورت دود سفید در هوا دیده می شوند. همین موضوع نشان می دهد که این گاز چقدر تمایل دارد به حالت محلول و اسیدی تبدیل شود.
به طور معمول، هیدروژن کلراید بیشتر به شکل محلول آبی یعنی اسید هیدروکلریک مورد استفاده قرار می گیرد. دلیل این انتخاب، سهولت حمل و نقل و ایمنی بالاتر کار با محلول نسبت به گاز فشرده و بی آب است. در نهایت، هرچند فرمول شیمیایی در هر دو حالت یکسان است، اما تفاوت بین گاز HCl و اسید هیدروکلریک محلول، تفاوتی اساسی و تعیین کننده در کاربرد، خطرات و رفتار شیمیایی آن ها به شمار می آید.
هیدروژن: جزء H در HCl
هیدروژن بخش فعال ترکیب HCl است و نقش اصلی در خاصیت اسیدی آن دارد. این عنصر با عدد اتمی یک، سبک ترین عضو جدول تناوبی به شمار می رود و در طبیعت اغلب به صورت مولکول دو اتمی H2 دیده می شود.
در ساختار HCl، اتم هیدروژن فقط به یک اتم کلر متصل است و به دلیل تفاوت الکتریکی میان آن ها، بار جزئی مثبت می گیرد. همین ویژگی باعث می شود پیوند حالتی قطبی داشته باشد.
زمانی که HCl در آب حل می شود، اتم هیدروژن از مولکول جدا شده و به شکل پروتون آزاد درمی آید. این پروتون بلافاصله با مولکول های آب ترکیب شده و یون هیدرونیوم را تشکیل می دهد.
در واقع، هیدروژن موجود در HCl همان بخشی است که در واکنش ها به مواد دیگر منتقل می شود. به همین دلیل، اسیدی بودن این ترکیب مستقیما به رفتار هیدروژن وابسته است.
با اینکه سهم هیدروژن در جرم کل HCl کم است، اهمیت آن بالاست. توانایی جدا شدن به صورت پروتون، عامل اصلی واکنش پذیری است.
کلر: جزء Cl در HCl
کلر بخش کلری ترکیب HCl را تشکیل می دهد و یکی از اجزای اصلی این اسید به شمار می رود. این عنصر با عدد اتمی ۱۷ در گروه هالوژن ها قرار دارد و در حالت طبیعی به صورت گاز دو اتمی سبز مایل به زرد با بویی تند و خفه کننده دیده می شود.
در ساختار مولکول HCl، اتم کلر به هیدروژن متصل است و به دلیل قدرت بالای جذب الکترون، بار جزئی منفی پیدا می کند. همین ویژگی باعث می شود پیوند میان این دو عنصر حالت قطبی داشته باشد.
زمانی که HCl در آب حل می شود، کلر به شکل یون کلرید آزاد می گردد. این یون از پایداری بالایی برخوردار است و واکنش پذیری کمی دارد. همین موضوع یکی از دلایل قدرت بالای اسید هیدروکلریک محسوب می شود.
حضور کلر در این ترکیب باعث تشکیل نمک های کلرید در واکنش با فلزات و بازها می شود. برای مثال، واکنش آن با سدیم هیدروکسید منجر به تولید نمک خوراکی می گردد. همچنین یون کلرید نقش مهمی در واکنش های شیمیایی و تعادل الکترولیتی بدن انسان دارد.
تشکیل و سنتز اسید هیدروکلریک
اسید هیدروکلریک را می توان به روش های مختلفی تولید کرد؛ گاهی با ترکیب مستقیم عناصر سازنده آن و گاهی هم به عنوان نتیجه جانبی سایر فرآیندهای صنعتی. ساده ترین روش، واکنش میان گاز هیدروژن و گاز کلر است که در نهایت گاز هیدروژن کلراید به وجود می آید.
این واکنش مقدار زیادی گرما آزاد می کند و به همین دلیل در صنعت داخل تجهیزات مخصوصی انجام می شود تا کنترل و ایمنی حفظ شود. گاز تولیدشده سپس وارد آب می شود و اسید هیدروکلریک مایع با خلوص بالا به دست می آید که برای مصارف گوناگون آماده است.
در مقیاس صنعتی، این اسید اغلب همزمان با تولید مواد دیگر ساخته می شود. برای نمونه، در فرآیند کلر-آلکالی که از الکترولیز آب نمک انجام می گیرد، هیدروژن و کلر آزاد می شوند و می توان آن ها را در همان مجموعه به HCl تبدیل کرد.
در برخی صنایع شیمیایی نیز اسید هیدروکلریک به صورت محصول جانبی واکنش های کلردار کردن ترکیبات آلی به دست می آید و بعد از بازیابی، مورد استفاده قرار می گیرد. حتی در طبیعت هم منابعی مانند فعالیت های آتشفشانی وجود دارند که گاز HCl را وارد هوا کرده و در نهایت به شکل اسید در بارش ها ظاهر می شود.
خواص فیزیکی اسید هیدروکلریک
اسید هیدروکلریک معمولا به شکل یک مایع شفاف و بی رنگ دیده می شود و از نظر ظاهری شباهت زیادی به آب دارد، اما بوی تند و آزاردهنده آن به راحتی قابل تشخیص است. در نمونه های غلیظ تر، به دلیل خارج شدن گاز HCl از محلول، بخار اسیدی در هوا دیده می شود که حالتی شبیه دود ایجاد می کند.
ویژگی های فیزیکی این اسید تا حد زیادی به میزان غلظت آن بستگی دارد. اسید هیدروکلریک غلیظ که حدود ۳۶ تا ۳۸ درصد HCl دارد، چگالی بیشتری نسبت به آب دارد و به همین دلیل سنگین تر است. نقطه جوش آن پایین تر از آب است، چون گاز محلول به آسانی از مایع جدا می شود.
در مقابل، محلول های رقیق تر رفتاری شبیه آب نشان می دهند و در دماهای نزدیک به ۱۰۰ درجه سانتیگراد به جوش می آیند. در یک غلظت مشخص حدود ۲۰ درصد، این اسید مخلوطی پایدار تشکیل می دهد که هنگام جوشیدن، ترکیب آن تغییر نمی کند.
از نظر انجماد نیز، با افزایش غلظت، دمای یخ زدن کاهش می یابد و برخی محلول ها در دماهای بسیار پایین منجمد می شوند. این اسید در آب به شدت حل می شود و قدرت اسیدی بالایی دارد. به دلیل خاصیت خورندگی شدید، نگهداری آن نیازمند ظروف مقاوم و ایمن است.
خواص شیمیایی و واکنش های HCl
اسید هیدروکلریک از نظر شیمیایی رفتار یک اسید قوی معدنی را دارد و به همین دلیل در واکنش های مختلف بسیار فعال عمل می کند. این ماده در آب تقریبا به طور کامل به یون های هیدروژن و کلرید تفکیک می شود و به راحتی یون هیدروژن خود را در اختیار مواد دیگر قرار می دهد.
یکی از مهم ترین واکنش های این اسید، خنثی سازی با بازها است. زمانی که HCl با موادی مانند هیدروکسیدهای فلزی ترکیب می شود، حاصل واکنش آب و یک نمک محلول است. این نوع واکنش ها پایه بسیاری از فرآیندهای شیمیایی ساده و صنعتی به شمار می آیند.
اسید هیدروکلریک همچنین با بسیاری از فلزات فعال واکنش نشان می دهد. فلزاتی مانند روی، آهن و آلومینیوم در تماس با این اسید حل می شوند و همزمان گاز هیدروژن آزاد می کنند. این واکنش ها معمولا با سرعت بالا و همراه با ایجاد حباب انجام می شود.
در مقابل، فلزاتی مانند مس، نقره و طلا نسبت به HCl مقاوم هستند و به تنهایی در آن حل نمی شوند. برای واکنش دادن این فلزات، حضور مواد اکسیدکننده قوی لازم است که شرایط شیمیایی پیچیده تری ایجاد می کند.
این اسید با کربنات ها و بی کربنات ها نیز واکنش می دهد و گاز دی اکسید کربن آزاد می کند که به صورت جوشش قابل مشاهده است. در شرایط خاص و در حضور اکسیدکننده های قوی، HCl می تواند منجر به آزاد شدن گاز کلر شود.
در مجموع، توانایی اسید هیدروکلریک در واگذاری پروتون و تشکیل ترکیبات کلریدی باعث شده این ماده نقش مهمی در واکنش های شیمیایی معدنی و آلی ایفا کند و کاربرد گسترده ای در صنعت و آزمایشگاه داشته باشد.
غلظت و گریدهای محلول های HCl
اسید هیدروکلریک در بازار و صنعت با غلظت های گوناگونی عرضه می شود؛ از محلول های بسیار رقیق گرفته تا نمونه های غلیظ. بیشترین غلظتی که می توان این اسید را به شکل محلول پایدار نگهداری کرد حدود ۳۸ درصد وزنی است. در این وضعیت، محلول تقریبا به حالت اشباع می رسد و اگر مقدار بیشتری HCl اضافه شود، به صورت گاز از آن خارج می گردد.
نگهداری محلول هایی با غلظت بالاتر از حدود ۴۰ درصد کار ساده ای نیست. در این شرایط، تبخیر گاز HCl شدت می گیرد و برای کنترل آن نیاز به ظروف خاص، فشار مناسب و حتی خنک سازی وجود دارد. به همین دلیل، در عمل اسید هیدروکلریک غلیظ معمولا با غلظتی نزدیک به ۳۷ درصد تولید و توزیع می شود. این نوع اسید در تماس با هوا بخار می کند و حالتی دودمانند ایجاد می نماید.
در کاربردهای صنعتی و ساختمانی، محلول های رقیق تر نیز رایج هستند. اصطلاح جوهر نمک یا موریاتیک اسید به نمونه هایی با خلوص کمتر، معمولا حدود ۳۰ درصد یا پایین تر گفته می شود. این محلول ها اغلب رنگ زرد کمرنگ دارند که ناشی از ناخالصی های جزئی است و برای تمیزکاری یا کارهای ساختمانی استفاده می شوند.
برای مصارف خانگی مانند شست وشوی سطوح یا استخر، غلظت های پایین تر در حدود ۱۰ درصد یا کمتر کاربرد دارند و معمولا قبل از مصرف نیز رقیق تر می شوند. در محیط های آزمایشگاهی، اسید هیدروکلریک رقیق به محلول های ۵ تا ۱۰ درصد گفته می شود و نمونه غلیظ همان حدود ۳۷ درصد در نظر گرفته می شود.
| غلظت (% وزنی) | مولاریته (M) | pH تقریبی | ویژگی ها | کاربردهای معمول |
|---|---|---|---|---|
| ۰٫۵٪ | ۰٫۱۵ | ~۱ | بسیار رقیق (معادل اسید معده) | اسید معده (شیره گوارشی) |
| ۵٪ | ۱٫۳ | ~۰ | اسید رقیق ولی همچنان قوی | تمیزکاری سبک |
| ۱۰٪ | ۲٫۸ | -۰٫۵ | درجه خانگی، خورنده | پاک کننده خانگی (کاشی، توالت) |
| ۱۸٪ | ~۵٫۵ | -۰٫۸ | اسید درجه صنعتی | اسیدشویی فولاد (زنگ زدایی) |
| ۲۰٪ | ۶٫۰ | -۰٫۸ | محلول آزئوتروپیک (نقطه جوش ثابت) | اسید صنعتی رایج |
| ۳۲٪ | ~۱۰٫۲ | -۱٫۰ | غلظت بالا، دودکننده | "جوهر نمک" (مصارف صنعتی) |
| ۳۷٪ | ~۱۲٫۰ | -۱٫۱ | اسید غلیظ، دودکننده | اسید غلیظ آزمایشگاهی (~۳۷٪) |
| ۴۰٪ | ~۱۳ | -۱٫۲ | نزدیک به اشباع، بسیار دودکننده | حداکثر غلظت (نیازمند نگهداری ویژه) |
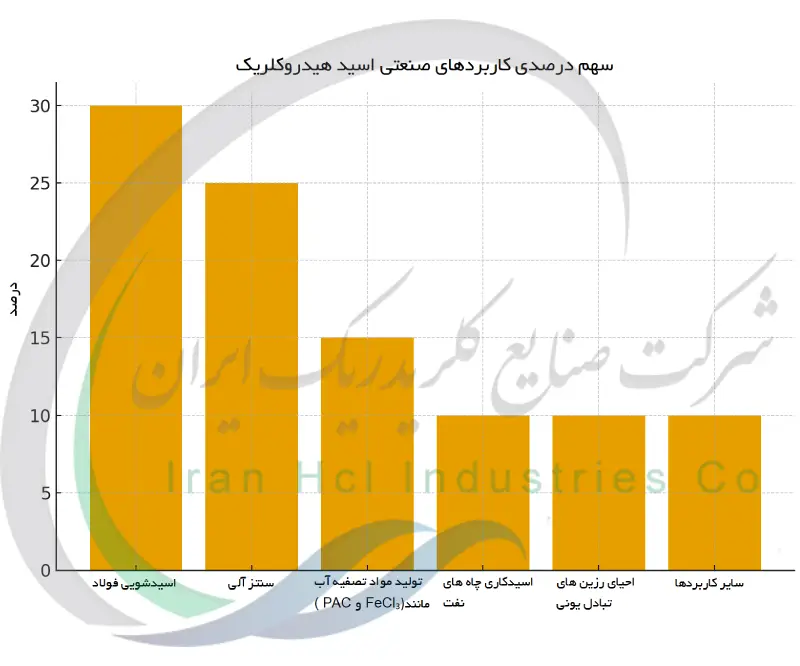
کاربردهای صنعتی اسید هیدروکلریک
اسید هیدروکلریک به خاطر قدرت اسیدی بالا و واکنش پذیری زیاد، جایگاه ویژه ای در صنایع مختلف دارد. این ماده به راحتی با ترکیبات گوناگون وارد واکنش می شود و همین ویژگی باعث شده در فرآیندهای صنعتی به طور گسترده مورد استفاده قرار گیرد.
یکی از مهم ترین کاربردهای آن در صنعت فولاد است. در این حوزه، اسید هیدروکلریک برای تمیز کردن سطح آهن و فولاد به کار می رود. این فرآیند که به اسیدشویی معروف است، لایه های زنگ و اکسید را از سطح فلز جدا می کند و فلز را برای مراحل بعدی مانند گالوانیزه کردن یا نورد آماده می سازد.
در صنایع شیمیایی و آلی، HCl نقش مهمی در تولید مواد مختلف دارد. این اسید در ساخت وینیل کلراید که ماده اولیه PVC است، همچنین در تولید برخی حلال ها و ترکیبات دارویی استفاده می شود. در بسیاری از این فرآیندها، اسید هیدروکلریک به عنوان تنظیم کننده pH یا تسهیل کننده واکنش ها به کار می رود.
از نظر معدنی نیز این اسید اهمیت بالایی دارد. ترکیباتی مانند کلرید کلسیم، کلرید آهن و پلی آلومینیوم کلرید که در تصفیه آب کاربرد دارند، با کمک اسید هیدروکلریک تولید یا فرآوری می شوند.
در صنعت نفت و گاز، از این اسید برای بهبود تولید چاه ها استفاده می شود. تزریق HCl به درون چاه باعث حل شدن بخشی از سنگ های اطراف و باز شدن مسیر جریان نفت یا گاز می گردد. همچنین در سیستم های تصفیه آب، این اسید برای احیای رزین های تبادل یونی به کار می رود. مجموعه این کاربردها نشان می دهد اسید هیدروکلریک یکی از مواد پایه و پرمصرف در صنعت به شمار می آید.
کاربردهای روزمره اسید هیدروکلریک
با وجود اینکه اسید هیدروکلریک جزو مواد شیمیایی قوی به حساب می آید، اما در زندگی روزمره هم به شکل کنترل شده و رقیق مورد استفاده قرار می گیرد. زمانی که این اسید با غلظت پایین تر عرضه می شود، می توان از توان بالای آن بدون ایجاد خطر جدی بهره برد.
یکی از شناخته شده ترین نمونه های مصرفی، جوهر نمک است که در واقع همان اسید هیدروکلریک با درصد خلوص کمتر محسوب می شود. این ماده در خانه ها و پروژه های ساختمانی برای تمیز کردن سطوح مختلف کاربرد دارد. از بین بردن شوره آجر، لکه های سیمانی، رسوبات آهکی و آثار زنگ زدگی از جمله استفاده های رایج آن است.
بسیاری از شوینده های قوی مخصوص کاشی، سرامیک و سرویس های بهداشتی نیز حاوی مقدار کمی HCl هستند. این نوع پاک کننده ها به حل شدن جرم های قدیمی، رسوبات آب سخت و باقی مانده صابون کمک می کنند و باعث می شوند سطوح دوباره تمیز و براق شوند.
در نگهداری استخرهای شنا، اسید هیدروکلریک رقیق برای تنظیم pH آب به کار می رود. اضافه کردن مقدار مشخصی از این اسید باعث می شود تعادل شیمیایی آب حفظ شود و از مشکلاتی مانند رسوب گذاری یا تحریک پوست جلوگیری گردد.
کاربرد این ماده فقط به نظافت محدود نمی شود. در صنایع غذایی نیز نوع خوراکی اسید هیدروکلریک، آن هم در مقدار بسیار کم، برای تنظیم اسیدیته برخی محصولات استفاده می شود. هرچند مصرف کننده به صورت مستقیم با آن روبه رو نیست، اما نقش آن در فرآوری مواد غذایی قابل توجه است.
در مجموع، حضور اسید هیدروکلریک در زندگی روزمره بیشتر به صورت غیرمستقیم و کنترل شده است؛ جایی که قدرت پاک کنندگی و تنظیم کنندگی آن به شکلی ایمن و حساب شده مورد استفاده قرار می گیرد.
اسید هیدروکلریک در بدن انسان
بدن انسان به صورت طبیعی از اسید هیدروکلریک به عنوان یکی از اجزای اصلی فرآیند گوارش استفاده می کند. در معده، سلول های خاصی این اسید را ترشح می کنند و محیطی بسیار اسیدی به وجود می آورند که pH آن معمولاً بین ۱ تا ۲ قرار دارد. این شرایط برای عملکرد درست دستگاه گوارش ضروری است.
یکی از وظایف مهم اسید معده، آماده سازی مواد غذایی برای هضم بهتر است. این اسید باعث باز شدن ساختار پروتئین ها می شود و آن ها را به شکلی درمی آورد که آنزیم های گوارشی بتوانند راحت تر روی آن ها اثر بگذارند. همچنین اسید هیدروکلریک نقش کلیدی در فعال شدن آنزیم پپسین دارد که وظیفه تجزیه پروتئین ها را بر عهده دارد.
محیط اسیدی معده تنها به هضم غذا محدود نمی شود، بلکه نقش دفاعی هم دارد. بسیاری از میکروب ها و عوامل بیماری زا که همراه غذا وارد بدن می شوند، در این شرایط اسیدی توان زنده ماندن ندارند و از بین می روند. به این ترتیب، اسید معده مانند یک سد محافظ عمل می کند.
غلظت اسید هیدروکلریک در شیره معده بسیار کم و حدود نیم درصد است، اما همین مقدار برای انجام وظایف آن کافی است. دیواره معده نیز با لایه ای محافظ پوشانده شده تا از آسیب اسید جلوگیری شود. اگر این تعادل به هم بخورد، مشکلاتی مانند رفلاکس، زخم معده یا اختلال در هضم ممکن است ایجاد شود. بنابراین وجود مقدار مناسب اسید هیدروکلریک برای سلامت گوارش اهمیت زیادی دارد.




