فهرست عناوین
- مقدمه
- درک پیوندهای شیمیایی
- مبانی پیوند کووالانسی
- الکترونگاتیویته و قطبیت پیوند
- پیوندهای کووالانسی قطبی در برابر غیرقطبی
- آیا HCl یونی است یا کووالانسی؟
- بررسی کلی هیدروژن کلرید (HCl)
- تشکیل مولکول HCl
- الکترونگاتیویته هیدروژن و کلر
- چرا مولکول HCl قطبی است؟
- گشتاور دوقطبی مولکول HCl
- خواص HCl ناشی از پیوند کووالانسی قطبی آن
- گاز HCl در مقایسه با اسید کلریدریک در آب
- مقایسه HCl با ترکیبات غیرقطبی و یونی
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 19-09-1404
تاریخ بروزرسانی مقاله : 19-09-1404
تعداد کلمات : 3400
آدرس مقاله : لینک مقاله
نوع پیوند (کووالانسی قطبی) در مولکول اسید کلریدریک

مقدمه
هیدروژن کلرید (HCl) یک مولکول دو اتمی ساده است که نمونه ی کلاسیکی از یک پیوند کووالانسی قطبی را نشان می دهد. این مولکول از یک اتم هیدروژن و یک اتم کلر تشکیل شده است. این دو اتم توسط یک جفت الکترون مشترک به هم متصل شده اند. اما این الکترون ها به طور مساوی بین دو اتم به اشتراک گذاشته نمی شوند. اتم کلر نسبت به هیدروژن کشش بسیار بیشتری بر الکترون های پیوندی اعمال می کند که باعث توزیع نابرابر چگالی الکترون می شود.
این نابرابری پیوند H–Cl را قطبی می کند، به این معنی که یک سر پیوند اندکی بار مثبت دارد در حالی که سر دیگر اندکی بار منفی دارد. هیدروژن کلرید قابل توجه است زیرا هنگام حل شدن در آب، اسید کلریدریک تشکیل می دهد، اما به عنوان یک مولکول مستقل توسط پیوند کووالانسی در کنار هم نگه داشته می شود. در کاربردهای صنعتی، زمانی که بحث هایی مانند خرید اسید کلریدریک کلر پارس تبریز تانکر مطرح می شود، در واقع همین رفتار مولکول HCl در محلول است که اهمیت پیدا می کند؛ زیرا قطبیت شدید پیوند موجب قدرت اسیدی بالا و واکنش پذیری قابل توجه اسید کلریدریک می شود.
در این مقاله ماهیت پیوند کووالانسی قطبی در HCl را بررسی خواهیم کرد و توضیح می دهیم که پیوند کووالانسی چیست، چگونه الکترونگاتیویته منجر به قطبیت پیوند می شود، و این پیوند قطبی HCl چه تأثیری بر ویژگی ها و رفتار آن دارد.
درک پیوندهای شیمیایی
پیوندهای شیمیایی نیروهایی هستند که اتم ها را درون ترکیبات کنار هم نگه می دارند. دو نوع اصلی پیوند شیمیایی قوی عبارتند از پیوند یونی و پیوند کووالانسی. پیوند یونی زمانی رخ می دهد که الکترون ها از یک اتم به اتم دیگر منتقل شوند و یون های دارای بار مثبت و منفی ایجاد شوند که یکدیگر را جذب می کنند. در مقابل، پیوند کووالانسی زمانی شکل می گیرد که اتم ها الکترون های خود را به اشتراک بگذارند.
در واقع، بسیاری از پیوندها نه کاملاً یونی هستند و نه کاملاً کووالانسی، بلکه در جایی بین این دو حالت قرار می گیرد و طیفی از انواع پیوند را به وجود می آورد. رفتار یک پیوند تا حد زیادی به نوع اتم های شرکت کننده و نحوه ی تعامل آنها با الکترون ها بستگی دارد. در همین چارچوب، بررسی شکل هندسی مولکول اسید کلریدریک و زاویه پیوند نمونه ای واضح از رفتار یک پیوند کووالانسی قطبی است که نشان می دهد چگونه نوع پیوند می تواند ساختار سه بعدی و ویژگی های مولکولی را تعیین کند.
درک تفاوت بین پیوند یونی و کووالانسی بسیار مهم هستند، زیرا کمک می کند بفهمیم چرا برخی ترکیبات (مانند سدیم کلرید) یون ها را به صورت یک شبکه ی بلوری مرتب می کنند، در حالی که ترکیبات دیگر (مثل هیدروژن کلرید) از مولکول های مجزایی تشکیل شده اند که توسط الکترون های مشترک کنار هم نگه داشته شده اند.
مبانی پیوند کووالانسی
در پیوند کووالانسی، دو اتم با سهیم شدن یک جفت الکترون به یکدیگر متصل می شوند و از این راه به وضعیت پایدارتر الکترونی می رسند. این نوع اتصال بیشتر میان اتم های نافلز دیده می شود، زیرا تمایل آن ها برای جذب الکترون تقریبا نزدیک به هم است. وقتی الکترون ها مشترک می شوند، هر اتم احساس می کند لایه بیرونی آن کامل تر شده است.
این پیوند می تواند شکل های مختلفی داشته باشد. اگر یک جفت الکترون مشترک باشد، پیوند یگانه شکل می گیرد، با دو جفت پیوند دوگانه و با سه جفت پیوند سه گانه ایجاد می شود. الکترون های مشترک در فضای بین دو هسته قرار می گیرند و ناحیه ای از کشش به وجود می آورند که اتم ها را کنار هم نگه می دارد.
بسیاری از مولکول های شناخته شده مانند هیدروژن، اکسیژن، آب و ترکیبات آلی بر پایه پیوند کووالانسی ساخته شده اند. در مولکول هیدروژن کلرید نیز هیدروژن و کلر به جای تبدیل شدن به یون، الکترون های خود را شریک می شوند. نتیجه این فرآیند تشکیل یک مولکول خنثی است که پیوند آن بر پایه جذب مشترک به الکترون ها شکل گرفته است.
الکترونگاتیویته و قطبیت پیوند
همه پیوندهای کووالانسی به یک شکل الکترون ها را میان اتم ها تقسیم نمی کنند. دلیل این تفاوت را می توان با مفهوم الکترونگاتیویته توضیح داد. این واژه به توانایی هر اتم برای کشیدن الکترون های پیوندی به سمت خود اشاره دارد و نشان می دهد کدام اتم نفوذ بیشتری بر الکترون ها دارد.
برای هر عنصر عدد مشخصی از نظر الکترونگاتیویته تعریف شده است که معمولا بر اساس مقیاس پاولینگ بیان می شود. اختلاف این عددها میان دو اتم تعیین می کند الکترون های مشترک چگونه پخش شوند. اگر دو اتم از نظر این ویژگی تقریبا برابر باشند، الکترون ها به صورت یکنواخت بین آن ها قرار می گیرند و پیوند غیرقطبی شکل می گیرد.
در مقابل، زمانی که یکی از اتم ها قدرت بیشتری در جذب الکترون داشته باشد، الکترون ها بیشتر به سمت همان اتم متمایل می شوند. در این حالت پیوند حالت قطبی پیدا می کند و توزیع بار در مولکول نامتعادل می شود. هرچه اختلاف الکترونگاتیویته بیشتر باشد، این نابرابری نیز شدت می گیرد.
برای نمونه، پیوندهایی مانند کربن و اکسیژن یا هیدروژن و کلر به دلیل تفاوت در این ویژگی تا حدی قطبی هستند. شناخت الکترونگاتیویته کمک می کند رفتار مولکول ها، نوع پیوندها و بسیاری از خواص شیمیایی مواد بهتر پیش بینی شوند.
پیوندهای کووالانسی قطبی در برابر غیرقطبی
پیوند کووالانسی می تواند به دو شکل قطبی یا غیرقطبی دیده شود. در نوع غیرقطبی، الکترون ها به صورت برابر میان دو اتم تقسیم می شوند. این وضعیت بیشتر زمانی اتفاق می افتد که دو اتم یکسان به هم متصل باشند، مانند مولکول نیتروژن یا کلر، یا وقتی اختلاف الکترونگاتیویته میان آن ها بسیار ناچیز است. در چنین پیوندی جدایش بار شکل نمی گیرد و هیچ بخش مولکول بار مثبت یا منفی مشخصی ندارد، بنابراین مولکول از نظر الکتریکی خنثی باقی می ماند.
در مقابل، پیوند کووالانسی قطبی زمانی به وجود می آید که دو اتم توانایی یکسانی در جذب الکترون نداشته باشند. در این حالت، الکترون ها بیشتر به سمت اتمی که قدرت جذب بالاتری دارد متمایل می شوند. در نتیجه، یک سر پیوند اندکی منفی و سر دیگر کمی مثبت می گردد و بارهای جزئی در مولکول ایجاد می شود.
مولکول آب نمونه شناخته شده ای از این حالت است. در پیوندهای بین اکسیژن و هیدروژن، اکسیژن بخش منفی تر و هیدروژن ها بخش مثبت تر را تشکیل می دهند و همین موضوع باعث قطبی شدن کل مولکول می شود. در هیدروژن کلرید نیز وضعیت مشابهی دیده می شود؛ سمت کلر بار جزئی منفی و سمت هیدروژن بار جزئی مثبت دارد.
شناخت تفاوت میان پیوندهای قطبی و غیرقطبی اهمیت زیادی دارد، زیرا این تفاوت ها بر رفتار مولکول ها، نحوه حل شدن آن ها در حلال ها، نقطه جوش و نوع نیروهای بین مولکولی اثر مستقیم می گذارد و در بسیاری از کاربردهای شیمیایی نقش تعیین کننده دارد.
آیا HCl یونی است یا کووالانسی؟
هیدروژن کلرید معمولا این سوال را به وجود می آورد که آیا باید آن را یک ماده یونی دانست یا یک ترکیب مولکولی. پاسخ روشن است؛ HCl در اصل یک ماده کووالانسی است که از مولکول های مستقل تشکیل شده و پیوند میان اتم های آن از نوع کووالانسی می باشد. با این حال، این پیوند کاملا یکنواخت نیست و در دسته پیوندهای کووالانسی قطبی قرار می گیرد.
دلیل اینکه HCl یونی به حساب نمی آید این است که در حالت جامد، شبکه ای منظم از یون ها مانند نمک طعام ایجاد نمی کند. حتی در فاز گازی نیز هیدروژن و کلر به صورت یک واحد مولکولی کنار هم باقی می مانند و از هم جدا نمی شوند. اختلاف تمایل این دو اتم به جذب الکترون وجود دارد، اما این اختلاف آنقدر شدید نیست که الکترون به طور کامل منتقل شود.
در نتیجه، به جای شکل گیری یون های آزاد، یک جفت الکترون میان دو اتم مشترک می شود، هرچند این اشتراک بیشتر به سمت کلر متمایل است. همین موضوع باعث قطبی شدن پیوند می گردد. در مقابل، ترکیبی مانند سدیم کلرید به طور واقعی یونی است، زیرا الکترون به طور کامل جابه جا می شود و یون های جداگانه تشکیل می شوند.
نکته گیج کننده زمانی مطرح می شود که HCl در آب حل می گردد. در این حالت اسید کلریدریک به وجود می آید و یون های آزاد دیده می شوند، اما خود HCl خالص همچنان یک ماده مولکولی و کووالانسی محسوب می شود.
بررسی کلی هیدروژن کلرید (HCl)
هیدروژن کلرید مولکولی دو اتمی است که از یک اتم هیدروژن و یک اتم کلر تشکیل می شود. این ماده در دمای معمولی به صورت گازی بی رنگ با بویی تند و آزاردهنده دیده می شود. هنگامی که در تماس با هوای مرطوب قرار می گیرد، با بخار آب واکنش می دهد و مه سفید و غلیظی ایجاد می کند که در واقع ذرات ریز اسید کلریدریک هستند.
این ترکیب نخستین بار توسط شیمیدانان سده های هفدهم و هجدهم مورد توجه قرار گرفت و در حالت محلول آبی، نام اسید موریاتیک نیز برای آن به کار می رفته است. هیدروژن کلرید به صورت گاز آزاد، جرم مولکولی حدود ۳۶٫۵ گرم بر مول دارد و از نظر ساختاری شکلی خطی دارد، زیرا تنها از دو اتم ساخته شده است. فاصله میان اتم های هیدروژن و کلر در این مولکول نزدیک به ۱۲۷ پیکومتر است.
به دلیل نابرابری در جذب الکترون میان هیدروژن و کلر، پیوند موجود در HCl از نوع کووالانسی قطبی است و همین موضوع باعث ایجاد گشتاور دوقطبی در آن می شود. در حالت خالص، این گاز رسانای جریان برق نیست، زیرا یون آزاد ندارد و از مولکول های خنثی تشکیل شده است.
اما زمانی که HCl در آب حل می شود، اسید کلریدریک به وجود می آید که یک الکترولیت قوی محسوب می شود. در کاربردهای صنعتی، هم گاز هیدروژن کلرید و هم محلول آبی آن اهمیت زیادی دارند و در تولید نمک های کلریدی، تنظیم اسیدیته و فرآیندهای شیمیایی گوناگون استفاده می شوند. شناخت ساختار و نوع پیوند این ماده به درک بهتر رفتار و واکنش پذیری آن کمک می کند.
تشکیل مولکول HCl
تشکیل مولکول هیدروژن کلرید را می توان با بررسی الکترون های لایه بیرونی هیدروژن و کلر توضیح داد. هیدروژن تنها یک الکترون در لایه ظرفیت خود دارد و کلر هفت الکترون در لایه بیرونی اش، به همین دلیل هر دو اتم به دنبال رسیدن به حالت پایدارتر هستند. هیدروژن با داشتن یک الکترون، تمایل دارد لایه خود را کامل کند و کلر نیز به یک الکترون دیگر نیاز دارد تا آرایش پایدار به دست آورد.
وقتی این دو اتم به هم نزدیک می شوند، راه حل ساده ای شکل می گیرد. هر کدام یک الکترون را در اختیار پیوند قرار می دهند و یک جفت الکترون مشترک ایجاد می شود. در نتیجه، پیوندی یگانه بین هیدروژن و کلر به وجود می آید که باعث اتصال آن ها به یکدیگر می شود.
با این اشتراک، هیدروژن عملا به آرایشی شبیه گاز نجیب هلیوم می رسد و کلر نیز ساختاری نزدیک به آرایش آرگون پیدا می کند. این وضعیت برای هر دو اتم پایدارتر از حالت جداگانه است و انرژی کمتری دارد.
پیوند ایجاد شده از نوع سیگما است و از هم پوشانی مستقیم اربیتال های هیدروژن و کلر به وجود می آید. البته این اشتراک کاملا برابر نیست، زیرا کلر توان بیشتری در جذب الکترون دارد. همین موضوع باعث می شود پیوند H–Cl حالتی قطبی داشته باشد و توزیع الکترون ها کمی به سمت کلر متمایل شود.
الکترونگاتیویته هیدروژن و کلر
قطبی بودن پیوند میان هیدروژن و کلر به طور مستقیم به تفاوت توان آن ها در جذب الکترون مربوط می شود. این ویژگی که با نام الکترونگاتیویته شناخته می شود، نشان می دهد هر اتم تا چه اندازه می تواند الکترون های یک پیوند را به سمت خود بکشد. بر اساس مقیاس پاولینگ، مقدار این ویژگی برای هیدروژن حدود ۲٫۲ و برای کلر نزدیک به ۳٫۲ در نظر گرفته می شود.
این اختلاف تقریبا یک واحدی باعث می شود کلر قدرت بیشتری در نگه داشتن الکترون های مشترک داشته باشد. در علم شیمی به طور معمول گفته می شود اگر اختلاف الکترونگاتیویته از مقدار مشخصی بیشتر باشد، پیوند حالت قطبی پیدا می کند. در مورد HCl، این اختلاف نه آن قدر کم است که پیوند کاملا خنثی باشد و نه آن قدر زیاد که پیوند را یونی بدانیم، بلکه دقیقا در محدوده یک پیوند کووالانسی قطبی قرار می گیرد.
به دلیل این کشش قوی تر، ابر الکترونی در مولکول HCl بیشتر به سمت کلر متمایل می شود. در نتیجه، ناحیه اطراف کلر اندکی بار منفی و ناحیه نزدیک به هیدروژن کمی بار مثبت پیدا می کند. کلر از جمله عناصری است که الکترونگاتیویته بالایی دارد و همین ویژگی نقش اصلی را در ایجاد قطبیت این پیوند ایفا می کند.
در مقابل، هیدروژن با الکترونگاتیویته متوسط خود توان رقابت با کلر را ندارد و نمی تواند الکترون ها را به همان اندازه نگه دارد. به همین دلیل، در این مولکول به صورت جزئی مثبت ظاهر می شود و ساختاری قطبی شکل می گیرد که بر رفتار شیمیایی HCl تاثیر می گذارد.
چرا مولکول HCl قطبی است؟
هیدروژن کلرید نمونه روشنی از یک مولکول کووالانسی قطبی است، زیرا الکترون ها در پیوند میان دو اتم آن به صورت برابر پخش نمی شوند. کلر توان بیشتری در جذب الکترون دارد و به همین دلیل الکترون های مشترک بیشتر در اطراف این اتم قرار می گیرند. نتیجه این وضعیت آن است که بخش مربوط به کلر اندکی بار منفی می گیرد و سمت هیدروژن کمی بار مثبت پیدا می کند.
این جدایی نسبی بار باعث می شود مولکول HCl دو سر متفاوت داشته باشد؛ یک سر با تمایل منفی و سر دیگر با تمایل مثبت. به چنین ساختاری دوقطبی گفته می شود. از آنجا که HCl تنها از دو اتم تشکیل شده و فقط یک پیوند دارد، همین اختلاف کوچک برای قطبی شدن کل مولکول کافی است و اثر آن در رفتار ماده به خوبی دیده می شود.
اگر مولکول های هیدروژن کلرید در یک میدان الکتریکی قرار بگیرند، تمایل دارند جهت مشخصی بگیرند. در این حالت، سمت کلر به طرف بخش مثبت میدان و سمت هیدروژن به طرف بخش منفی آن قرار می گیرد. این رفتار در مولکول های غیرقطبی دیده نمی شود.
برای مقایسه، در مولکولی مانند Cl₂ هر دو اتم یکسان هستند و الکترون ها به طور مساوی میان آن ها تقسیم می شوند، بنابراین هیچ دوقطبی شکل نمی گیرد. قطبی بودن HCl بسیاری از ویژگی های آن را توضیح می دهد، از جمله حل شدن آسان در آب و توانایی تبدیل شدن به یون در محلول. در مجموع، کشش بیشتر کلر نسبت به الکترون ها دلیل اصلی قطبی بودن این پیوند است و باعث می شود یک سر مولکول منفی تر و سر دیگر مثبت تر باشد.
گشتاور دوقطبی مولکول HCl
یکی از راه های سنجش عددی قطبیت در پیوندها و مولکول ها، بررسی گشتاور دوقطبی است. گشتاور دوقطبی کمیتی است که از حاصل ضرب مقدار جدایش بار در فاصله میان بارهای مثبت و منفی به دست می آید و معمولا با واحد دبی بیان می شود. مولکول هیدروژن کلرید دارای گشتاور دوقطبی حدود 1.03 دبی است و همین عدد نشان می دهد که این مولکول ماهیتی قطبی دارد.
این مقدار نه بسیار کوچک است و نه بسیار بزرگ، بلکه قطبیتی متوسط و قابل توجه را نشان می دهد. برای مقایسه، هیدروژن فلوئورید که اختلاف الکترونگاتیویته بیشتری دارد، گشتاور دوقطبی بزرگ تری نزدیک به 1.82 دبی نشان می دهد، در حالی که مولکولی مانند کلر دو اتمی هیچ قطبیتی ندارد و مقدار آن صفر است.
در HCl مرکز بار منفی در اطراف کلر و مرکز بار مثبت در نزدیکی هیدروژن قرار دارد و این دو مرکز به اندازه طول پیوند از هم جدا هستند. اندازه این گشتاور حتی امکان برآورد درصدی از ویژگی یونی پیوند را فراهم می کند. این مفهوم برای مقایسه قطبیت مولکول ها بسیار کاربردی است.
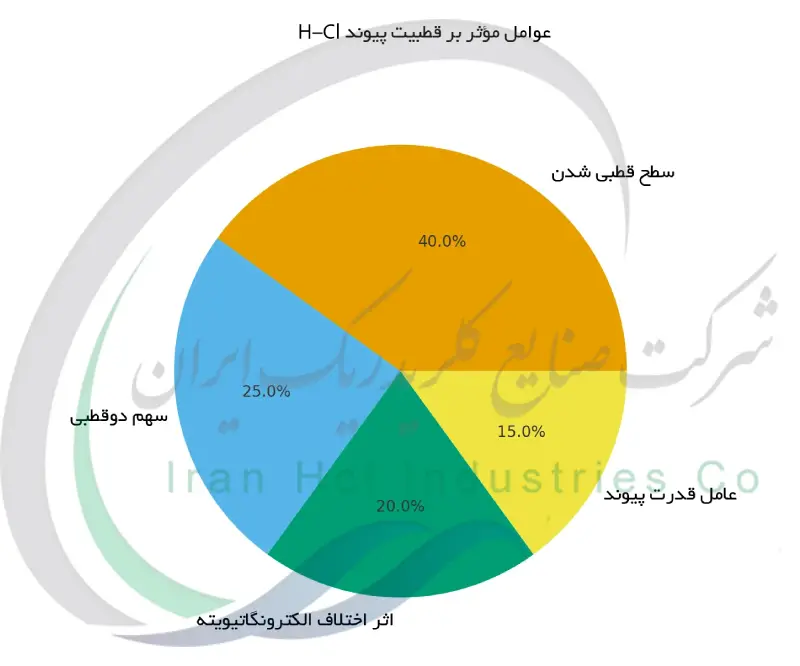
خواص HCl ناشی از پیوند کووالانسی قطبی آن
قطبی بودن پیوند در مولکول هیدروژن کلرید نقش مهمی در ویژگی های آن دارد. یکی از اثرات اصلی این ویژگی، حل شدن بسیار خوب HCl در حلال های قطبی مانند آب است. زمانی که گاز هیدروژن کلرید وارد آب می شود، مولکول های آب که خود قطبی هستند، به راحتی آن را جذب می کنند. در این فرایند، بخش منفی مولکول آب به سمت قسمت مثبت HCl و بخش مثبت آب به سمت قسمت منفی آن کشیده می شود و همین جذب متقابل باعث حل شدن سریع گاز می گردد.
قدرت حل پذیری HCl در آب بسیار بالاست، به طوری که حجم زیادی از این گاز می تواند در مقدار کمی آب حل شود و محلولی به نام اسید کلریدریک بسازد. این ویژگی در بسیاری از کاربردهای آزمایشگاهی و صنعتی اهمیت دارد.
اثر دیگر قطبیت پیوند، مربوط به نقطه جوش است. مولکول های HCl نسبت به مواد غیرقطبی هم اندازه، در دمای بالاتری می جوشند. دلیل این موضوع وجود نیروهای جاذبه بین مولکول های قطبی است که جدا شدن آن ها را دشوارتر می کند. البته چون HCl پیوند هیدروژنی قوی ندارد، نقطه جوش آن همچنان پایین باقی می ماند.
قطبیت پیوند H–Cl همچنین باعث افزایش واکنش پذیری این ماده می شود. هیدروژن در این مولکول حالت مثبت تری دارد و به همین دلیل HCl به آسانی می تواند نقش یک اسید را ایفا کند. هنگام حل شدن در آب، این ویژگی باعث آزاد شدن یون هیدروژن و تشکیل یون های هیدرونیوم می شود. در مجموع، پیوند کووالانسی قطبی HCl دلیل اصلی حل پذیری بالا، رفتار خاص فازی و قدرت اسیدی این ترکیب است.
گاز HCl در مقایسه با اسید کلریدریک در آب
تفاوت میان گاز هیدروژن کلرید و اسید کلریدریک اهمیت زیادی دارد، هرچند این دو به هم وابسته هستند. هیدروژن کلرید در حالت خالص، یک ماده مولکولی با پیوند کووالانسی قطبی است. در فاز گازی یا زمانی که در دماهای پایین به مایع تبدیل می شود، این ماده از مولکول های جداگانه HCl تشکیل شده است که یون آزاد در آن ها وجود ندارد. به همین دلیل، هیدروژن کلرید خالص رسانای جریان برق نیست و رفتاری شبیه مواد یونی از خود نشان نمی دهد.
اما شرایط زمانی کاملا تغییر می کند که گاز HCl وارد آب شود. آب به دلیل قطبی بودن، تعامل بسیار قوی ای با مولکول های HCl برقرار می کند. این برهم کنش باعث می شود پیوند میان هیدروژن و کلر شکسته شود و مولکول HCl دیگر به شکل اولیه خود باقی نماند. در این فرآیند، هیدروژن به مولکول های آب متصل می شود و یون هیدرونیوم تشکیل می دهد، در حالی که کلر به صورت یون کلرید در محلول پخش می شود.
در این حالت، محلولی شامل یون های مثبت و منفی داریم که آن را اسید کلریدریک می نامند. این محلول کاملا یونی است و به خوبی جریان الکتریسیته را هدایت می کند. بنابراین، پیوند H–Cl تنها پیش از حل شدن معنا دارد و پس از تفکیک، هیدروژن و کلر دیگر مستقیما به هم متصل نیستند.
این تغییر نشان می دهد که پیوندهای کووالانسی قطبی در حضور حلالی مانند آب می توانند به طور کامل شکسته شوند. همین ویژگی توضیح می دهد چرا اسید کلریدریک یک اسید بسیار قوی است و در محلول های رقیق، تقریبا تمام مولکول های HCl به یون تبدیل می شوند.
مقایسه HCl با ترکیبات غیرقطبی و یونی
برای فهم بهتر ماهیت پیوند کووالانسی قطبی در هیدروژن کلرید، مقایسه آن با پیوندهای دیگر بسیار کمک کننده است. اگر به مولکولی مانند کلر دو اتمی نگاه کنیم، می بینیم که دو اتم کاملا مشابه کنار هم قرار گرفته اند و الکترون ها را به طور مساوی تقسیم می کنند. در چنین حالتی هیچ ناحیه مثبت یا منفی مشخصی شکل نمی گیرد و پیوند کاملا غیرقطبی باقی می ماند.
در سوی دیگر، ترکیبی مانند سدیم کلرید قرار دارد که ساختاری کاملا متفاوت دارد. در این ماده، سدیم که یک فلز است، الکترون خود را به طور کامل به کلر می دهد. نتیجه این جابه جایی کامل، تشکیل یون های مثبت و منفی و ایجاد یک شبکه یونی منظم است، نه مولکول های جداگانه.
هیدروژن کلرید میان این دو حالت قرار می گیرد. در این مولکول، اختلاف توان جذب الکترون میان هیدروژن و کلر باعث ایجاد بارهای جزئی می شود، اما الکترون به طور کامل منتقل نمی گردد. بنابراین HCl همچنان یک مولکول مستقل باقی می ماند، نه یک ساختار یونی گسترده.
این مقایسه نشان می دهد پیوند HCl نه کاملا غیرقطبی است و نه یونی خالص، بلکه نمونه ای روشن از یک پیوند کووالانسی قطبی به شمار می رود که ویژگی هایی میان این دو حالت دارد.
| ویژگی | HCl (کووالانسی قطبی) | HF (کووالانسی قطبی) | Cl₂ (کووالانسی غیرقطبی) | NaCl (یونی) |
|---|---|---|---|---|
| عناصر سازنده | H + Cl (نافلزها) | H + F (نافلزها) | Cl + Cl (هر دو نافلز) | Na (فلز) + Cl (نافلز) |
| اختلاف الکترونگاتیویته | ~۰٫۹ | ~۱٫۸ | ۰ | ~۲٫۱ |
| نوع پیوند | کووالانسی قطبی | کووالانسی قطبی | کووالانسی غیرقطبی | یونی |
| گشتاور دوقطبی (دبای) | ۱٫۰۳ | ۱٫۸۲ | ۰ | — |
| نقطه جوش (°C) | -۸۵ | ۱۹٫۵ | -۳۴ | ۱۴۶۵ |
| حلالیت در آب | بسیار زیاد (تشکیل اسید) | زیاد (محلول اسیدی) | کم (محدود) | زیاد (به یون ها تفکیک می شود) |
| نیروهای بین مولکولی | دوقطبی-دوقطبی، پراکندگی | پیوند هیدروژنی | تنها پراکندگی | جاذبه یونی (شبکه بلوری) |




