فهرست عناوین
- مقدمه
- تعریف الکترونگاتیوی در شیمی
- نحوه اندازه گیری الکترونگاتیوی در مقیاس پاولینگ
- الکترونگاتیوی هیدروژن و تأثیرات آن
- الکترونگاتیوی بالای کلر و توضیح آن
- تشکیل پیوند هیدروژن-کلر در مولکول HCl
- اختلاف الکترونگاتیوی در اسید هیدروکلریک (HCl)
- ویژگی های پیوند کووالانسی قطبی در HCl
- بار های جزئی و گشتاور دوقطبی مولکول HCl
- چرا HCl یک مولکول قطبی است
- رفتار اسید هیدروکلریک در آب
- مقایسه اختلاف الکترونگاتیوی: HCl در برابر سایر ترکیبات
- اختلاف الکترونگاتیوی و نوع پیوند (ناقطبی، قطبی، یونی)
- تأثیر الکترونگاتیوی بر ویژگی های فیزیکی HCl
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 03-10-1404
تاریخ بروزرسانی مقاله : 03-10-1404
تعداد کلمات : 3200
آدرس مقاله : لینک مقاله
اختلاف الکترونگاتیوی بین اتم های هیدروژن و کلر در اسید کلریدریک

مقدمه
اسید هیدروکلریک (HCl) یک مولکول دو اتمی ساده متشکل از هیدروژن و کلر است. این دو اتم اختلاف قابل توجهی در مقادیر الکترونگاتیوی خود دارند، یعنی جفت الکترون های مشترک را به طور نابرابر به سمت خود می کشند. این عدم تعادل در اشتراک الکترون، پیوند H–Cl را قطبی می کند و به مولکول خواص متمایزی می دهد. در کاربردهای صنعتی و تجاری که شناخت دقیق رفتار شیمیایی این اسید اهمیت دارد، مفاهیمی مانند قطبیت پیوند و واکنش پذیری نقش تعیین کننده ای دارند و به همین دلیل موضوعاتی مرتبط با تأمین و مصرف، از جمله خرید اسید کلریدریک کلران سمنان فله، برای صنایع مصرف کننده اهمیت عملی پیدا می کند. درک اختلاف الکترونگاتیوی بین هیدروژن و کلر در اسید هیدروکلریک دیدگاهی درباره پیوند های شیمیایی، قطبیت مولکولی و واکنش پذیری این اسید متداول به ما می دهد.
تعریف الکترونگاتیوی در شیمی
الکترونگاتیویته یکی از مفاهیم اصلی در شیمی است که نشان می دهد هر اتم تا چه اندازه تمایل دارد الکترون های یک پیوند را به سمت خود بکشد. به بیان ساده، این مفهوم قدرت کشش اتم بر الکترون های مشترک را توصیف می کند و کمک می کند رفتار پیوندهای شیمیایی بهتر درک شود.
برای سنجش این ویژگی، به عناصر عددی نسبت داده می شود که معمولاً بر اساس مقیاس پاولینگ بیان می گردد. هرچه این عدد بزرگ تر باشد، تمایل اتم برای جذب الکترون بیشتر است. به عنوان نمونه، فلوئور در بالاترین جایگاه این مقیاس قرار دارد، در حالی که فلزاتی مانند سزیم در انتهای آن دیده می شوند.
الکترونگاتیویته در جدول تناوبی الگوی مشخصی دارد. با حرکت در یک دوره از چپ به راست افزایش پیدا می کند و با پایین آمدن در یک گروه کاهش می یابد. همین روند توضیح می دهد چرا رفتار پیوندها در عناصر مختلف متفاوت است.
وقتی دو اتم دارای الکترونگاتیویته برابر یا بسیار نزدیک باشند، الکترون ها به طور یکنواخت میان آن ها تقسیم می شوند و پیوندی غیرقطبی شکل می گیرد. اما اگر اختلاف این تمایل قابل توجه باشد، الکترون ها بیشتر به سمت اتم قوی تر کشیده می شوند و پیوند حالت قطبی پیدا می کند. این موضوع پایه درک مولکول هایی مانند HCl است که در آن توزیع الکترون کاملاً مساوی نیست.
نحوه اندازه گیری الکترونگاتیوی در مقیاس پاولینگ
برای این که مفهوم الکترونگاتیوی به صورت عددی بیان شود، شیمیدان ها بیشتر از مقیاس پاولینگ استفاده می کنند؛ مقیاسی که توسط لینوس پاولینگ طراحی شد. در این روش، به هر عنصر یک عدد بدون واحد داده می شود که نشان دهنده قدرت آن اتم در جذب الکترون های یک پیوند شیمیایی است. هرچه این عدد بزرگ تر باشد، تمایل اتم برای کشیدن الکترون ها بیشتر خواهد بود.
در این مقیاس، فلوئور با عدد ۴٫۰ به عنوان بیشترین مقدار در نظر گرفته شده و سایر عناصر بر اساس آن سنجیده می شوند. برای نمونه، عدد الکترونگاتیوی هیدروژن حدود ۲٫۲ و برای کلر نزدیک به ۳٫۲ است. این تفاوت به خوبی نشان می دهد چرا کلر در یک پیوند، الکترون ها را قوی تر از هیدروژن به سمت خود می کشد.
پاولینگ این مقیاس را با بررسی انرژی پیوندها معرفی کرد. او متوجه شد پیوندهایی که میان اتم های با تفاوت زیاد در تمایل الکترونی شکل می گیرند، به دلیل داشتن ویژگی یونی جزئی، انرژی بیشتری دارند.
در سال های بعد، مقیاس های دیگری نیز پیشنهاد شد، اما به دلیل سادگی و کاربردی بودن، روش پاولینگ همچنان رایج ترین گزینه است. این اعداد به شیمیدان ها کمک می کند نوع پیوند را پیش بینی کنند و مثلاً توضیح دهند چرا پیوند H–Cl یک پیوند کووالانسی قطبی به شمار می آید.
الکترونگاتیوی هیدروژن و تأثیرات آن
الکترونگاتیویته هیدروژن حدود ۲٫۲ است و همین مقدار باعث می شود جایگاه ویژه ای میان عناصر داشته باشد. هیدروژن نه به اندازه نافلزهای بالای جدول، مانند اکسیژن یا کلر، تمایل شدید به الکترون دارد و نه رفتاری شبیه فلزات نشان می دهد. این حالت میانی، ویژگی های شیمیایی خاصی به آن می بخشد.
این تمایل متوسط در نوع پیوندهای هیدروژن به خوبی دیده می شود. وقتی هیدروژن با عناصری که الکترونگاتیویته بالایی دارند پیوند می سازد، الکترون های مشترک بیشتر به سمت آن اتم ها کشیده می شوند. در چنین شرایطی، هیدروژن اندکی بار مثبت پیدا می کند و نقش متفاوتی در مولکول ایفا می نماید.
اما داستان همیشه یکسان نیست. در ترکیب با فلزات فعال، مانند سدیم در هیدرید سدیم، وضعیت کاملاً تغییر می کند. در این حالت، هیدروژن می تواند الکترون بگیرد و رفتاری شبیه یک یون منفی از خود نشان دهد. این تفاوت رفتاری نشان دهنده انعطاف پذیری بالای هیدروژن است.
در اسید هیدروکلریک، الکترونگاتیویته هیدروژن آن قدر نیست که الکترون خود را کاملاً واگذار کند، اما به اندازه ای پایین است که کلر سهم بیشتری از الکترون ها را در اختیار بگیرد. به همین دلیل، هیدروژن در این مولکول کمی مثبت می شود و این موضوع بر نحوه جذب و واکنش HCl با مواد دیگر اثر می گذارد، به ویژه در برخورد با نواحی منفی یا جفت الکترون های آزاد مولکول های اطراف.
الکترونگاتیوی بالای کلر و توضیح آن
کلر از خانواده هالوژن هاست و به دلیل تمایل زیادش به جذب الکترون، الکترونگاتیوی بالایی دارد. عدد این ویژگی برای کلر در مقیاس پاولینگ حدود ۳٫۲ است و تنها عناصری مانند فلوئور و اکسیژن مقدار بیشتری دارند. این ویژگی به ساختار اتمی کلر برمی گردد؛ هسته آن کشش مؤثری بر الکترون ها دارد و اتم به دنبال کامل کردن لایه ظرفیت خود است.
جایگاه کلر در جدول تناوبی نیز در این رفتار نقش دارد. با عدد اتمی ۱۷، کلر شعاع نسبتاً کوچکی دارد و همین موضوع باعث می شود نیروی جاذبه هسته بر الکترون های اطراف قوی تر احساس شود. به همین دلیل، کلر به راحتی یک الکترون می گیرد و در ترکیبات یونی به شکل یون کلرید ظاهر می شود.
در پیوندهای کووالانسی هم این ویژگی کاملاً مشهود است. وقتی کلر با عنصری که الکترونگاتیوی کمتری دارد پیوند می سازد، معمولاً سهم بیشتری از الکترون های مشترک را به سمت خود می کشد. نمونه روشن آن مولکول HCl است که در آن الکترون ها بیشتر در نزدیکی کلر قرار می گیرند.
نتیجه این توزیع نامساوی آن است که کلر در این مولکول بار منفی جزئی پیدا می کند و هیدروژن کمی مثبت می شود. در واقع، همین تمایل قوی کلر به الکترون ها عامل اصلی قطبی شدن پیوند H–Cl به شمار می آید.
تشکیل پیوند هیدروژن-کلر در مولکول HCl
هیدروژن کلرید زمانی شکل می گیرد که یک اتم هیدروژن و یک اتم کلر تصمیم می گیرند یک جفت الکترون را میان خودشان به اشتراک بگذارند. با این کار، بین آن ها یک پیوند کووالانسی ساده به وجود می آید. هیدروژن فقط یک الکترون در لایه بیرونی دارد و برای رسیدن به حالت پایدار، به یک الکترون دیگر نیازمند است. در مقابل، کلر با داشتن هفت الکترون والانس، تنها یک الکترون کم دارد تا لایه ظرفیتش کامل شود.
وقتی این دو اتم به هم نزدیک می شوند، با شریک شدن یک جفت الکترون، نیاز هر دو برطرف می شود. با این حال، این اشتراک کاملاً برابر نیست. کلر به دلیل تمایل بیشترش به الکترون، این جفت مشترک را کمی بیشتر به سمت خود می کشد. همین موضوع باعث می شود پیوند H–Cl حالت قطبی پیدا کند.
در شرایط عادی، HCl به صورت مولکول های جدا از هم وجود دارد و در دمای محیط یک گاز به شمار می رود. این رفتار با موادی مانند نمک طعام تفاوت دارد که ساختار شبکه ای یونی دارند.
تشکیل پیوند در HCl نمونه خوبی است برای این که ببینیم دو نافلز چگونه می توانند پیوند کووالانسی بسازند، اما به دلیل تفاوت در کشش الکترونی، پیوندی با قطبیت مشخص ایجاد کنند. همین ویژگی، بسیاری از خصوصیات HCl مانند نقطه جوش بالاتر از انتظار و تمایل زیاد به حل شدن در حلال های قطبی را توضیح می دهد.
اختلاف الکترونگاتیوی در اسید هیدروکلریک (HCl)
اختلاف الکترونگاتیوی میان هیدروژن و کلر در مولکول HCl حدود یک واحد برآورد می شود. هیدروژن عددی نزدیک به ۲٫۲ دارد و کلر در حدود ۳٫۲ قرار می گیرد. این فاصله عددی به اندازه ای هست که باعث شود پیوند میان آن ها حالت قطبی پیدا کند. معمولاً گفته می شود اگر اختلاف الکترونگاتیوی دو اتم از حدود ۰٫۴ بیشتر باشد، پیوند کاملاً خنثی نخواهد بود.
در مورد HCl، این اختلاف نه آن قدر کم است که پیوند غیرقطبی محسوب شود و نه آن قدر زیاد که بتوان آن را یونی دانست. همین موقعیت میانی باعث می شود پیوند H–Cl در دسته پیوندهای کووالانسی قطبی قرار بگیرد. کلر نسبت به هیدروژن توان بیشتری در جذب الکترون دارد و به همین دلیل الکترون های مشترک بیشتر به سمت آن متمایل می شوند.
در نتیجه این کشش نامتعادل، توزیع الکترون ها در مولکول یکنواخت نیست. بخش کلر مولکول چگالی الکترونی بیشتری دارد و سمت هیدروژن اندکی دچار کمبود الکترون می شود. همین نابرابری ساده، دلیل اصلی قطبیت در اسید هیدروکلریک است.
وقتی شیمیدان ها درباره قطبی یا غیرقطبی بودن یک پیوند صحبت می کنند، نخستین چیزی که بررسی می شود اختلاف الکترونگاتیوی است. در HCl این معیار به روشنی نشان می دهد چرا این مولکول قطبی است؛ زیرا یک سر پیوند الکترون ها را بسیار قوی تر از سر دیگر به سمت خود می کشد.
ویژگی های پیوند کووالانسی قطبی در HCl
در مولکول هیدروژن کلرید، پیوند میان هیدروژن و کلر از نوع کووالانسی قطبی است. یعنی الکترون ها میان دو اتم مشترک اند، اما این اشتراک کاملاً برابر نیست. کلر به دلیل تمایل بیشترش به جذب الکترون، سهم بزرگ تری از ابر الکترونی پیوند را به خود اختصاص می دهد و همین موضوع تعادل را بر هم می زند.
به دنبال این نابرابری، روی اتم کلر بار منفی جزئی و روی اتم هیدروژن بار مثبت جزئی شکل می گیرد. در این حالت، برخلاف پیوندهای یونی، الکترون ها به طور کامل جابه جا نمی شوند و همچنان میان دو اتم باقی می مانند، فقط جهت گیری آن ها تغییر کرده است. همین جدایی نسبی بارها باعث می شود HCl رفتاری متفاوت از گازهای غیرقطبی داشته باشد.
مولکول های HCl می توانند یکدیگر را از طریق جاذبه های دوقطبی جذب کنند، به طوری که بخش مثبت یک مولکول به بخش منفی مولکول دیگر نزدیک می شود. این ویژگی در موادی مانند H₂ یا Cl₂ دیده نمی شود، چون آن ها فاقد قطبیت هستند و تنها نیروهای بسیار ضعیف تری دارند.
همچنین، در حضور میدان الکتریکی، مولکول های HCl تمایل دارند در راستای میدان قرار بگیرند و سمت کلر به سوی قطب مثبت بچرخد. به همین دلیل، پیوند H–Cl اغلب با یک فلش نمایش داده می شود که جهت جابه جایی الکترون را نشان می دهد. این مثال به خوبی نشان می دهد اختلاف تمایل الکترونی چگونه به توزیع نامتقارن الکترون ها منجر می شود.
بار های جزئی و گشتاور دوقطبی مولکول HCl
به دلیل این که الکترون ها در مولکول HCl به صورت نابرابر میان دو اتم پخش شده اند، هر اتم دارای بار جزئی مشخصی است. هیدروژن کمی مثبت می شود و کلر به همان نسبت بار منفی جزئی می گیرد. همین جدایی بار باعث می شود مولکول HCl یک دوقطبی واقعی و قابل اندازه گیری داشته باشد.
اندازه این دوقطبی در آزمایش ها حدود ۱٫۰۷ دبی به دست آمده است؛ عددی که میزان قطبیت مولکول را نشان می دهد. در مولکول های قطبی، مرکز بار مثبت و منفی دقیقاً روی هم قرار نمی گیرند و همین فاصله منجر به ایجاد گشتاور دوقطبی می شود. در مورد HCl، این جدایی بار تقریباً معادل حدود ۱۷ درصد از بار کامل یک الکترون است که در امتداد طول پیوند توزیع شده است.
به بیان ساده تر، پیوند H–Cl نه کاملاً یونی است و نه کاملاً اشتراکی. بخش عمده آن ماهیت کووالانسی دارد، اما سهم یونی قابل توجهی نیز در آن دیده می شود. این ترکیب ویژگی ها همان چیزی است که از اختلاف الکترونگاتیوی میان هیدروژن و کلر انتظار می رود.
وجود این بارهای جزئی باعث می شود HCl واکنش پذیری بالایی در محیط های قطبی داشته باشد. برای نمونه، این مولکول به راحتی در آب حل می شود، چون سر مثبت و منفی آن به بخش های مخالف مولکول های آب جذب می گردد. در نهایت، دوقطبی بودن HCl نتیجه مستقیم تفاوت تمایل الکترونی دو اتم سازنده آن است و بسیاری از رفتارهای شیمیایی این ماده را توضیح می دهد.
چرا HCl یک مولکول قطبی است
مولکول هیدروژن کلرید قطبی محسوب می شود، چون تنها پیوند موجود در آن یعنی پیوند H–Cl ذاتاً قطبی است و کل ساختار فقط از دو اتم تشکیل شده است. در چنین مولکولی هیچ تقارن هندسی وجود ندارد که بتواند اثر این قطبیت را خنثی کند. برخلاف بعضی مولکول های بزرگ تر که پیوندهای قطبی آن ها یکدیگر را بی اثر می کنند، در HCl این امکان وجود ندارد و اثر پیوند به طور کامل باقی می ماند.
از آنجا که این مولکول تنها یک پیوند دارد، همان پیوند تعیین کننده رفتار کلی آن است. لحظه دوقطبی مولکول اسید کلریدریک (قطبیت مولکولی) مستقیماً از پیوند H–Cl ناشی می شود و جهت آن از سمت اتم هیدروژن به سوی اتم کلر در نظر گرفته می شود. به همین دلیل، یک سر مولکول بار مثبت جزئی دارد و سر دیگر آن بار منفی جزئی مشخصی را نشان می دهد.
این دوقطبی بودن بسیاری از ویژگی های HCl را توضیح می دهد. برای مثال، این ماده به آسانی در آب حل می شود، زیرا بخش های باردار مولکول HCl به شدت با مولکول های قطبی آب برهمکنش برقرار می کنند. همین جاذبه ها باعث می شود آب بتواند مولکول را از هم باز کند.
علاوه بر این، قطبیت بر خواص فیزیکی HCl نیز اثرگذار است. در مقایسه با گازهای غیرقطبی با اندازه مشابه، هیدروژن کلرید نقطه جوش بالاتری دارد، چون جدا شدن مولکول های قطبی از یکدیگر به انرژی بیشتری نیاز دارد.
رفتار اسید هیدروکلریک در آب
وقتی گاز هیدروژن کلرید وارد آب می شود، محلولی به نام اسید هیدروکلریک به وجود می آید که در دسته اسیدهای قوی قرار می گیرد. دلیل اصلی این رفتار، قطبی بودن پیوند H–Cl است. آب خودش یک حلال بسیار قطبی است و به محض تماس با HCl، میان آن ها برهمکنش شدیدی شکل می گیرد.
در این برخورد، بخش منفی مولکول HCl به سمت هیدروژن های آب جذب می شود و هم زمان بخش مثبت آن به سوی اکسیژن آب کشیده می گردد. این کشش دوطرفه باعث می شود مولکول HCl نتواند ساختار خود را حفظ کند و به سرعت از هم باز شود.
در نتیجه، هیدروژن به صورت یک پروتون جدا می گردد و بلافاصله به مولکول آب می چسبد و یون هیدرونیوم را می سازد. از سوی دیگر، کلر الکترون های پیوند را نگه می دارد و به یون کلرید تبدیل می شود. به این ترتیب، پیوند H–Cl عملاً شکسته می شود و محلول پر از یون های باردار می گردد.
اختلاف قابل توجه تمایل الکترونی میان هیدروژن و کلر، پیوند را هم قطبی و هم نسبتاً سست کرده است. همین موضوع اجازه می دهد آب آن را کاملاً تجزیه کند. به همین دلیل HCl در آب تقریباً به طور کامل یونیزه می شود و رفتار یک اسید قوی را نشان می دهد. در مقایسه، موادی مانند HF با وجود قطبیت بیشتر، به دلیل پیوند محکم تر چنین تفکیکی ندارند.
مقایسه اختلاف الکترونگاتیوی: HCl در برابر سایر ترکیبات
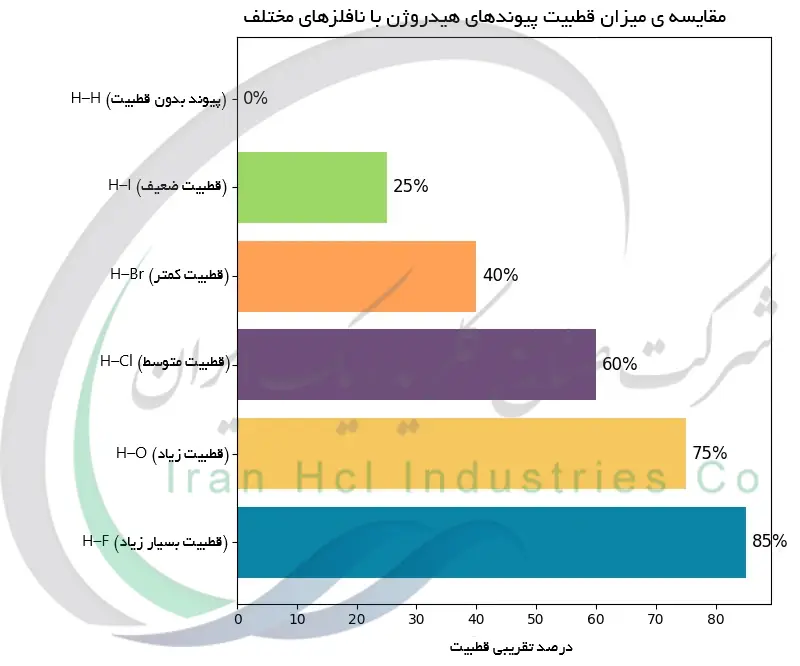
برای درک بهتر پیوند HCl، مفید است که اختلاف الکترونگاتیوی آن را با پیوند های دیگر مقایسه کنیم. در ادامه مقادیر الکترونگاتیوی چند پیوند مختلف شامل هیدروهالید ها HF، HCl، HBr، HI و چند مثال مرجع آورده شده است. مقادیر الکترونگاتیوی تقریبی هر اتم (بر اساس مقیاس پاولینگ) و اختلاف الکترونگاتیوی (ΔEN) ذکر شده است. این اختلاف با نوع یا ویژگی پیوند همبستگی دارد:
| ترکیب | الکترونگاتیوی اتم اول | الکترونگاتیوی اتم دوم | اختلاف الکترونگاتیوی (ΔEN) | نوع پیوند |
|---|---|---|---|---|
| H₂ (H–H) | ۲٫۲ | ۲٫۲ | ۰٫۰ | کووالانسی ناقطبی (اشتراک برابر الکترون ها) |
| HF (H–F) | ۲٫۲ | ۴٫۰ | ۱٫۸ | کووالانسی قطبی (قطبیت بسیار قوی) |
| HCl (H–Cl) | ۲٫۲ | ۳٫۲ | ۱٫۰ | کووالانسی قطبی (قطبیت متوسط) |
| HBr (H–Br) | ۲٫۲ | ۲٫۸ | ۰٫۶ | کووالانسی قطبی (قطبیت کمتر از HCl) |
| HI (H–I) | ۲٫۲ | ۲٫۷ | ۰٫۵ | کووالانسی کمی قطبی (تقریباً غیرقطبی) |
| H₂O (H–O) | ۲٫۲ | ۳٫۴ | ۱٫۲ | کووالانسی قطبی (مولکول خمیده قطبی است) |
| NaCl (Na–Cl) | ۰٫۹ | ۳٫۲ | ۲٫۳ | پیوند یونی (انتقال تقریباً کامل الکترون) |
همانطور که در جدول مشاهده می شود، اختلاف الکترونگاتیوی HCl (~۱٫۰) آن را در محدوده پیوند های کووالانسی قطبی قرار می دهد. پیوند HCl از HBr یا HI قطبی تر است اما از HF قطبیّت کمتری دارد. H₂ با ΔEN صفر یک پیوند کاملاً کووالانسی ناقطبی دارد، در حالی که NaCl با ΔEN بسیار بزرگ یک پیوند یونی است. HCl بین این دو حالت قرار می گیرد و به صورت مولکولی با قطبیت قابل توجه رفتار می کند بدون اینکه یک ترکیب کاملاً یونی باشد.
اختلاف الکترونگاتیوی و نوع پیوند (ناقطبی، قطبی، یونی)
مقدار اختلاف الکترونگاتیوی میان دو اتم، نشانه خوبی برای تشخیص نوع پیوند میان آن هاست. اگر این اختلاف بسیار کم یا نزدیک به صفر باشد، الکترون ها تقریباً به شکل برابر میان اتم ها پخش می شوند و پیوند حالت غیرقطبی پیدا می کند. نمونه های ساده آن مولکول هایی مانند H₂ یا Cl₂ هستند که در آن ها هیچ سمت مثبت یا منفی مشخصی دیده نمی شود.
با بیشتر شدن این اختلاف، اما نه در حد بسیار زیاد، پیوند وارد محدوده کووالانسی قطبی می شود. در چنین حالتی الکترون ها هنوز مشترک اند، ولی یکی از اتم ها سهم بیشتری از آن ها را در اختیار دارد. مولکول هایی مثل HCl یا آب از این نوع هستند و به همین دلیل دارای سر مثبت و منفی مشخص می باشند.
اگر اختلاف الکترونگاتیوی خیلی بزرگ شود، به ویژه زمانی که یک فلز در برابر یک نافلز قرار گیرد، پیوند معمولاً یونی در نظر گرفته می شود. در این وضعیت، الکترون ها عملاً منتقل می شوند و یون های با بار مخالف شکل می گیرند؛ مانند آنچه در نمک طعام دیده می شود.
البته این مرزبندی کاملاً سخت و قطعی نیست و بیشتر یک راهنمای تقریبی محسوب می شود. معمولاً گفته می شود اختلاف های کوچک پیوند غیرقطبی، اختلاف های میانی پیوند قطبی و اختلاف های بزرگ پیوند یونی می سازند. برای مثال، اختلاف الکترونگاتیوی در HCl آن قدر هست که پیوند را قطبی کند، اما نه آن قدر که ساختار یونی بسازد. همین تفاوت توضیح می دهد چرا HCl یک گاز مولکولی است، در حالی که ترکیبی مانند NaCl یک جامد یونی پایدار به شمار می آید.
تأثیر الکترونگاتیوی بر ویژگی های فیزیکی HCl
اختلاف الکترونگاتیوی میان هیدروژن و کلر و قطبیتی که از آن به وجود می آید، نقش مهمی در ویژگی های فیزیکی HCl دارد. یکی از جاهایی که این اثر به خوبی دیده می شود، دمای تغییر فاز، به ویژه نقطه جوش است. مولکول های قطبی به دلیل داشتن سرهای مثبت و منفی، یکدیگر را از راه نیروهای دوقطبی جذب می کنند. این جاذبه ها از نیروهایی که میان مولکول های غیرقطبی هم اندازه وجود دارد، قوی تر هستند.
به عنوان نمونه، هیدروژن کلرید با جرم مولی نزدیک به ۳۶٫۵ در دمای حدود منفی ۸۵ درجه سانتی گراد به جوش می آید. در مقابل، آرگون که جرمی تقریباً مشابه دارد اما غیرقطبی و تک اتمی است، در دمای بسیار پایین تری می جوشد. این تفاوت نشان می دهد جدا کردن مولکول های قطبی HCl از یکدیگر به انرژی بیشتری نیاز دارد.
قطبیت HCl بر حلالیت آن نیز اثر مستقیم می گذارد. این ماده به راحتی در آب حل می شود، زیرا آب خود یک حلال قطبی است و میان آن ها برهمکنش قوی برقرار می شود. برعکس، گازهایی مانند کلر که قطبیت ندارند، در آب به سختی حل می شوند.
در مجموع، اختلاف تمایل الکترونی در HCl باعث تقویت جاذبه های بین مولکولی و افزایش تعامل آن با محیط های قطبی می شود. همین موضوع دلیل بسیاری از رفتارهای فیزیکی متفاوت این ترکیب است.