فهرست عناوین
- مقدمه
- درک جرم مولکولی
- محاسبه جرم مولکولی
- جرم مولکولی اسید هیدروکلریک (HCl)
- مقایسه جرم مولکولی اسید هیدروکلریک با آب
- مقایسه جرم مولکولی اسید هیدروکلریک با آمونیاک
- مقایسه جرم مولکولی اسید هیدروکلریک با متان
- مقایسه جرم مولکولی اسید هیدروکلریک با اکسیژن
- مقایسه جرم مولکولی اسید هیدروکلریک با نیتروژن
- مقایسه جرم مولکولی اسید هیدروکلریک با دی اکسید کربن
- مقایسه جرم مولکولی اسید هیدروکلریک با گاز هیدروژن
- مقایسه جرم مولکولی اسید هیدروکلریک با گاز کلر
- مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن فلوئورید
- مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن برومید
- مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن یدید
- اهمیت تفاوت های جرم مولکولی
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 13-09-1404
تاریخ بروزرسانی مقاله : 13-09-1404
تعداد کلمات : 3600
آدرس مقاله : لینک مقاله
مقایسه جرم مولکولی اسید کلریدریک با سایر ترکیبات ساده
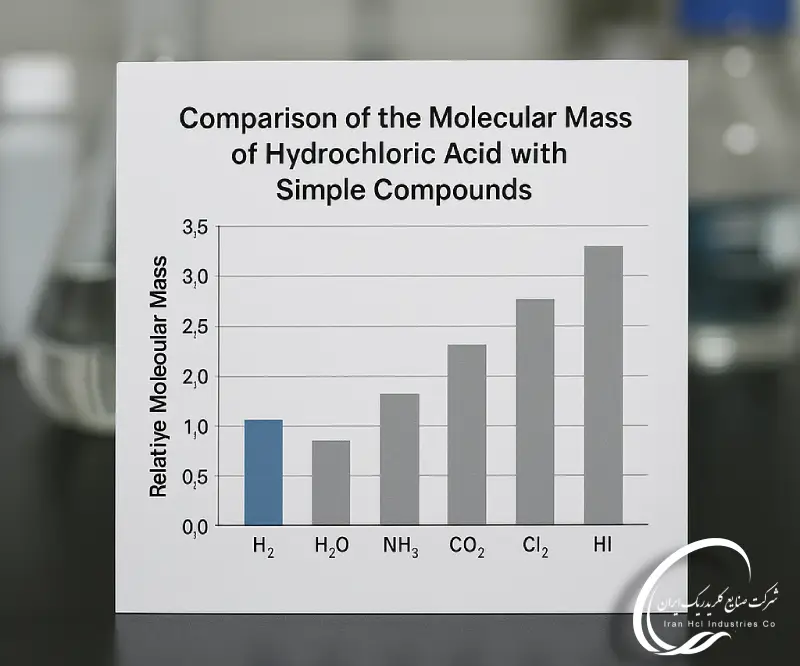
مقدمه
علم شیمی شامل مجموعه ی گسترده ای از مواد است و درک خواص بنیادی آن ها بسیار مهم است. در میان این خواص، جرم مولکولی به عنوان یک معیار پایه ای برای مقایسه ی ترکیبات مختلف مطرح است. ترکیبات ساده ی زیادی در شیمی وجود دارد که از گازهای دو اتمی تا مولکول های کوچک را شامل می شوند و دانستن این که مولکول های آن ها نسبت به یکدیگر چقدر سنگین هستند به دانشمندان در پیش بینی رفتارشان کمک می کند.
در این مقاله ی جامع، جرم مولکولی اسید هیدروکلریک را با سایر ترکیبات ساده مقایسه خواهد شد. اسید هیدروکلریک (HCl) یک ماده ی شناخته شده است و بررسی جرم آن نسبت به دیگر مواد می تواند روندهای گوناگونی را آشکار سازد؛ به ویژه برای صنایعی که در زمینه تأمین و خرید اسید کلریدریک کلر پارس تبریز فله فعالیت دارند، شناخت دقیق ویژگی های مولکولی این ماده اهمیت بیشتری پیدا می کند.
ما بررسی می کنیم که جرم مولکولی چه معنایی دارد و چگونه محاسبه می شود و سپس به مقایسه ی جرم مولکولی HCl با آب، آمونیاک، متان و دیگر ترکیبات ساده ی متداول می پردازیم. در پایان، مشخص خواهد شد که جرم HCl در زمینه ی مولکول های کوچک چه جایگاهی دارد و نمونه های سبک تر و سنگین تر را برجسته می کند. این دید کلی، درکی جامع از جایگاه جرم مولکولی HCl ارائه می دهد بدون این که فقط بر یک جنبه تاکید کند، و بدین ترتیب یک دیدگاه متعادل از این ویژگی اساسی شیمیایی فراهم می شود.
درک جرم مولکولی
جرم مولکولی به وزن یک مولکول از یک ماده گفته می شود و معمولا آن را با یکای جرم اتمی یا به صورت جرم مولی بر حسب گرم بر مول بیان می کنند. این مفهوم از پایه ای ترین و قابل فهم ترین مباحث شیمی به شمار می رود و برای درک بسیاری از رفتارهای مواد اهمیت دارد. به زبان ساده، جرم مولکولی نشان می دهد که یک مولکول از یک ترکیب تا چه اندازه سنگین است.
برای به دست آوردن این مقدار، کافی است جرم اتم های تشکیل دهنده یک مولکول را با هم جمع کنیم. هر عنصر دارای جرم اتمی مشخصی است که از بررسی ایزوتوپ های آن عنصر به دست آمده است؛ برای نمونه، هیدروژن جرمی نزدیک به 1.008 و اکسیژن جرمی حدود 15.999 واحد جرم اتمی دارد. وقتی این عددها را بر اساس فرمول شیمیایی کنار هم می گذاریم، وزن نهایی مولکول مشخص می شود.
محاسبه جرم مولکولی به شیمیدان ها کمک می کند تا مواد مختلف را با هم مقایسه کنند، چه در مقیاس یک مولکول و چه در مقیاس یک مول. این کمیت ساده اما کاربردی، نقش مهمی در بررسی ویژگی های فیزیکی مواد دارد و پایه بسیاری از محاسبات آزمایشگاهی و صنعتی محسوب می شود.
جرم مولکولی همچنین بر ویژگی هایی مانند چگالی و سرعت پخش اثر می گذارد، به ویژه زمانی که با گازها سروکار داریم. مولکول های سبک تر معمولا سریع تر حرکت می کنند و در یک محیط مشابه زودتر پخش می شوند، در حالی که مولکول های سنگین تر رفتار کندتری دارند.
شناخت این مفهوم امکان مقایسه موادی مانند اسید هیدروکلریک با سایر ترکیبات را فراهم می کند، زیرا به شکل مستقیم نشان می دهد که مولکول های هر ماده در برابر هم چه میزان وزن دارند. به همین دلیل، جرم مولکولی یکی از پایه های اصلی درک و تحلیل مواد شیمیایی به شمار می رود.
محاسبه جرم مولکولی
محاسبه جرم مولکولی یک ترکیب با داشتن فرمول شیمیایی و آگاهی از جرم های اتمی عناصر سازنده آن روندی ساده و قابل فهم دارد. در این مسیر، ابتدا عناصر موجود در ساختار مولکول شناسایی می شوند و تعداد اتم های هر عنصر به طور دقیق مشخص می گردد. این مرحله کمک می کند تصویر روشنی از اجزای تشکیل دهنده مولکول به دست آید.
در ادامه، جرم اتمی هر عنصر که معمولا از جدول تناوبی استخراج می شود، در تعداد اتم های همان عنصر در مولکول ضرب می گردد. به این ترتیب سهم هر عنصر در وزن نهایی ترکیب محاسبه می شود. پس از انجام این ضرب ها، همه مقادیر به دست آمده با یکدیگر جمع می شوند تا جرم مولکولی کل محاسبه شود.
به عنوان نمونه، برای تعیین جرم مولکولی اسید هیدروکلریک با فرمول HCl، جرم اتمی هیدروژن که حدود 1.008 amu است با جرم اتمی کلر در حدود 35.45 amu جمع می شود و عددی نزدیک به 36.46 amu به دست می آید. این مقدار در قالب جرم مولی نیز برابر با 36.46 گرم بر مول خواهد بود.
همین روش برای سایر ترکیبات نیز کاربرد دارد. برای آب با فرمول H2O که شامل دو اتم هیدروژن و یک اتم اکسیژن است، محاسبه به صورت 2*(1.008) + 15.999 انجام می شود و نتیجه ای نزدیک به 18.02 به دست می آید. در مورد آمونیاک NH3 نیز با سه اتم هیدروژن و یک اتم نیتروژن، مقدار تقریبی 17.03 محاسبه می شود.
با استفاده از این شیوه، می توان جرم مولکولی مواد مختلف را با دقت مناسب تعیین کرد و ترکیبات گوناگون را از نظر وزن مولکولی به شکل قابل اعتمادی با هم مقایسه نمود.
جرم مولکولی اسید هیدروکلریک (HCl)
اسید هیدروکلریک (HCl) یک مولکول ساده ی دو اتمی متشکل از یک اتم هیدروژن و یک اتم کلر است. HCl دارای جرم مولی تقریبا 36.46 گرم بر مول هستند. این مقدار از مجموع جرم های اتمی اجزای آن به دست آمده است: هیدروژن حدود 1.008 گرم بر مول و کلر حدود 35.45 گرم بر مول وزن دارند که جمعا حدود 36.46 گرم بر مول برای هر مولکول HCl می شود. این جرم مولکولی نسبتا متوسط نشان دهنده ی این واقعیت است که هیدروژن سبک ترین عنصر است در حالی که کلر یک اتم نسبتا سنگین محسوب می شود.
در نتیجه، جرم مولکولی HCl به طور قابل ملاحظه ای بالاتر از ترکیباتی است که تنها از اتم های هیدروژن، کربن یا اکسیژن با تعداد مشابه تشکیل شده اند. در عمل، گاز کلرید هیدروژن فرم گازی HCl به دلیل جرم مولکولی خود چگال تر از بسیاری از گازهای معمول مانند هوا است. در محلول آبی، که به عنوان اسید هیدروکلریک شناخته می شود، جرم مولکولی برای هر واحد HCl تغییری نمی کند و این امر در تعیین ویژگی هایی مانند رفتار اسید در واکنش ها و سهم جرمی آن در غلظت محلول ها نقش کلیدی دارد.
دانستن جرم دقیق HCl برای تهیه ی محلول ها و مقایسه ی آن با سایر مواد ضروری است و همین موضوع درک بهتر پیکربندی الکترونی اتم های سازنده اسید کلریدریک را نیز ضروری می سازد، زیرا ویژگی های مولکولی و رفتاری HCl ارتباط مستقیمی با ساختار الکترونی آن دارند.
مقایسه جرم مولکولی اسید هیدروکلریک با آب
آب با فرمول H2O یکی از ساده ترین و آشناترین ترکیبات شیمیایی است و وقتی جرم مولکولی آن با اسید هیدروکلریک مقایسه می شود، تفاوت قابل توجهی دیده می شود. جرم مولکولی آب حدود 18.02 گرم بر مول است، در حالی که این عدد برای اسید هیدروکلریک به حدود 36.46 گرم بر مول می رسد. به بیان ساده، هر مولکول HCl تقریبا دو برابر یک مولکول آب وزن دارد.
دلیل اصلی این اختلاف به نوع اتم های سازنده این دو ماده برمی گردد. آب از دو اتم بسیار سبک هیدروژن و یک اتم اکسیژن با جرم متوسط تشکیل شده است، اما اسید هیدروکلریک علاوه بر هیدروژن، یک اتم کلر دارد که نسبت به اکسیژن جرم بسیار بیشتری دارد. همین موضوع باعث افزایش وزن مولکولی HCl می شود.
این تفاوت وزنی فقط یک عدد تئوری نیست و در عمل هم اثر دارد. در حالت گازی، گاز هیدروژن کلرید سنگین تر است و بیشتر به سمت پایین هوا حرکت می کند، در حالی که بخار آب سبک تر بوده و راحت تر در هوا پخش می شود. همچنین در دمای برابر، مولکول های آب به طور میانگین سریع تر از مولکول های HCl حرکت می کنند. این مقایسه نشان می دهد ترکیب عناصر چگونه وزن و رفتار فیزیکی مواد را تعیین می کند.
مقایسه جرم مولکولی اسید هیدروکلریک با آمونیاک
آمونیاک با فرمول NH3 یکی از مولکول های سبک و پرکاربرد است و وقتی آن را از نظر جرم مولکولی با اسید هیدروکلریک مقایسه می کنیم، اختلاف قابل توجهی دیده می شود. جرم مولکولی آمونیاک حدود 17.03 گرم بر مول است، در حالی که جرم مولکولی HCl به حدود 36.46 گرم بر مول می رسد. این یعنی هر مولکول اسید هیدروکلریک بیش از دو برابر یک مولکول آمونیاک وزن دارد.
ریشه این تفاوت به نوع اتم های سازنده بازمی گردد. آمونیاک از یک اتم نیتروژن و سه اتم هیدروژن تشکیل شده که همگی نسبتا سبک هستند، اما در HCl یک اتم کلر وجود دارد که جرم بالاتری دارد و وزن کلی مولکول را افزایش می دهد.
این اختلاف در آزمایش های ساده هم دیده می شود. گاز آمونیاک به دلیل سبکی سریع تر پخش می شود و مسیر بیشتری را طی می کند. در آزمایش لوله انتشار، نقطه برخورد گازها به سمت HCl نزدیک تر است، چون آمونیاک مسافت طولانی تری را می پیماید. همچنین آمونیاک تمایل به بالا رفتن دارد، اما HCl بیشتر به سمت پایین حرکت می کند. این تفاوت ها نقش جرم مولکولی را در رفتار مواد به خوبی نشان می دهند.
مقایسه جرم مولکولی اسید هیدروکلریک با متان
متان با فرمول CH4 یک هیدروکربن ساده و بخش اصلی گاز طبیعی است. جرم مولکولی آن حدود 16.04 گرم بر مول محاسبه می شود که از کربن و چهار اتم هیدروژن به دست می آید. اگر این مقدار با جرم مولکولی اسید هیدروکلریک مقایسه شود، اختلاف قابل توجهی دیده می شود، زیرا HCl جرمی نزدیک به 36.46 گرم بر مول دارد. به بیان ساده، یک مولکول متان کمتر از نصف وزن یک مولکول اسید هیدروکلریک را داراست.
علت این تفاوت به نوع عناصر تشکیل دهنده برمی گردد. متان تنها از اتم های سبک کربن و هیدروژن ساخته شده است، اما در ساختار HCl یک اتم کلر حضور دارد که نسبت به این عناصر جرم بسیار بیشتری دارد و وزن نهایی مولکول را افزایش می دهد.
سبکی متان باعث می شود این گاز از هوا سبک تر باشد و پس از آزاد شدن به سرعت به سمت بالا حرکت کند. در مقابل، گاز هیدروژن کلرید به دلیل جرم بیشتر تمایل دارد نزدیک سطح زمین باقی بماند. این مقایسه نشان می دهد جرم مولکولی چگونه رفتار فیزیکی گازها را تعیین می کند.
مقایسه جرم مولکولی اسید هیدروکلریک با اکسیژن
اکسیژن با فرمول O2 یکی از مهم ترین مولکول های دو اتمی برای ادامه حیات به شمار می رود و هر مولکول آن از دو اتم اکسیژن تشکیل شده است. جرم مولکولی این گاز حدود 32.00 گرم بر مول است، زیرا هر اتم اکسیژن جرمی نزدیک به 16.00 دارد. زمانی که این مقدار با جرم مولکولی اسید هیدروکلریک مقایسه می شود، مشخص می گردد که اکسیژن کمی سبک تر از HCl است که جرم مولکولی آن حدود 36.46 گرم بر مول می باشد.
با وجود آنکه هر دو ماده از دو اتم تشکیل شده اند، تفاوت اصلی آن ها به وزن اتم های سازنده بازمی گردد. در اسید هیدروکلریک، حضور اتم کلر که جرم بالاتری نسبت به اکسیژن دارد، باعث افزایش وزن نهایی مولکول می شود. در مقابل، مولکول O2 تنها از اکسیژن تشکیل شده و همین موضوع آن را سبک تر نگه می دارد.
این اختلاف در رفتار گازی نیز قابل مشاهده است. گاز اکسیژن چگالی کمتری نسبت به گاز هیدروژن کلرید دارد و در شرایط مشابه، حجم برابر از HCl وزن بیشتری خواهد داشت. همچنین اگر HCl در محیط آزاد شود، می تواند بخاراتی سنگین تر از هوا ایجاد کند، در حالی که اکسیژن به دلیل نزدیکی جرم مولکولی آن به میانگین هوای اطراف، رفتاری طبیعی تر در فضا دارد. این مقایسه نشان می دهد تغییر نوع اتم در یک مولکول چگونه بر جرم و ویژگی های فیزیکی آن اثر می گذارد.
مقایسه جرم مولکولی اسید هیدروکلریک با نیتروژن
نیتروژن با فرمول N2 یک مولکول دو اتمی ساده است و بخش عمده هوای اطراف ما را تشکیل می دهد، به طوری که حدود 78 درصد اتمسفر از این گاز ساخته شده است. هر مولکول نیتروژن از دو اتم نیتروژن تشکیل می شود و جرم مولکولی آن نزدیک به 28.02 گرم بر مول است، زیرا هر اتم نیتروژن جرمی در حدود 14.01 دارد.
وقتی این عدد با جرم مولکولی اسید هیدروکلریک مقایسه می شود، اختلاف مشخصی دیده می شود. جرم مولکولی HCl حدود 36.46 گرم بر مول است و به همین دلیل به طور محسوسی از نیتروژن سنگین تر به شمار می رود. این تفاوت به ترکیب اتمی آن ها مربوط است، زیرا اتم های نیتروژن نسبت به اتم کلر وزن کمتری دارند.
به دلیل جرم مولکولی پایین تر، گاز نیتروژن چگالی کمتری دارد و همین ویژگی باعث می شود میانگین جرم مولکولی هوا حدود 29 گرم بر مول باشد. در مقابل، اسید هیدروکلریک از این مقدار سنگین تر است و هنگام آزاد شدن در هوا تمایل دارد در لایه های پایین تر باقی بماند. این مقایسه کمک می کند تفاوت رفتار این دو گاز در شرایط واقعی بهتر درک شود.
مقایسه جرم مولکولی اسید هیدروکلریک با دی اکسید کربن
دی اکسید کربن با فرمول CO2 یک مولکول خطی است که از یک اتم کربن و دو اتم اکسیژن ساخته شده است. جرم مولکولی این گاز حدود 44.01 گرم بر مول برآورد می شود و دلیل آن حضور دو اتم اکسیژن با جرم نسبتا بالا در ساختار آن است. وقتی این مقدار با جرم مولکولی اسید هیدروکلریک مقایسه می شود، مشخص می گردد که CO2 سنگین تر است، زیرا HCl جرمی نزدیک به 36.46 گرم بر مول دارد.
این اختلاف به این معناست که هر مولکول دی اکسید کربن حدود 1.2 برابر یک مولکول اسید هیدروکلریک وزن دارد. وجود دو اتم اکسیژن باعث شده CO2 در میان گازهای ساده، مولکولی نسبتا سنگین محسوب شود. هر دو گاز CO2 و HCl از هوای معمولی سنگین تر هستند و در صورت رها شدن می توانند در لایه های پایین تر فضا جمع شوند.
با این حال، جرم مولکولی بالاتر دی اکسید کربن باعث می شود چگالی آن در شرایط یکسان بیشتر باشد. در یک محیط بسته، CO2 حتی می تواند زیر لایه گاز HCl قرار بگیرد. این مقایسه نشان می دهد افزایش تعداد یا وزن اتم ها چگونه جرم مولکولی را بالا برده و رفتار گاز را تغییر می دهد.
مقایسه جرم مولکولی اسید هیدروکلریک با گاز هیدروژن
گاز هیدروژن با فرمول H2 ساده ترین و سبک ترین مولکول شناخته شده است که تنها از دو اتم هیدروژن تشکیل می شود. جرم مولکولی آن حدود 2.016 گرم بر مول است و هر اتم هیدروژن جرمی نزدیک به 1.008 دارد. وقتی این عدد با جرم مولکولی اسید هیدروکلریک مقایسه می شود، اختلافی بسیار بزرگ دیده می شود، زیرا HCl جرمی در حدود 36.46 گرم بر مول دارد. به بیان ساده، یک مولکول اسید هیدروکلریک تقریبا 18 برابر سنگین تر از یک مولکول هیدروژن است.
این تفاوت چشمگیر باعث رفتار کاملا متفاوت این دو گاز می شود. هیدروژن به دلیل سبکی بسیار زیاد، چگالی پایینی دارد و پس از آزاد شدن به سرعت به سمت بالا حرکت کرده و حتی می تواند از لایه های بالایی جو خارج شود. در مقابل، گاز هیدروژن کلرید سنگین تر است و معمولا در نزدیکی سطح زمین باقی می ماند.
علاوه بر این، HCl در آب به خوبی حل می شود و در هوای مرطوب سریع جذب رطوبت می گردد، در حالی که هیدروژن چنین رفتاری ندارد. اختلاف زیاد جرم مولکولی همچنین نشان می دهد که در یک جرم مساوی، تعداد مولکول های هیدروژن بسیار بیشتر از مولکول های HCl خواهد بود. این مقایسه نمونه ای روشن از تفاوت های حدی میان مولکول های ساده است.
مقایسه جرم مولکولی اسید هیدروکلریک با گاز کلر
گاز کلر با فرمول Cl2 از دو اتم کلر تشکیل شده و جرم مولکولی آن حدود 70.90 گرم بر مول است. این عدد تقریبا دو برابر جرم مولکولی اسید هیدروکلریک محسوب می شود که حدود 36.46 گرم بر مول دارد. به همین دلیل، وقتی یک مولکول کلر با یک مولکول HCl مقایسه می شود، تفاوت وزن به وضوح دیده می شود و Cl2 به مراتب سنگین تر است.
علت این اختلاف به ترکیب سازنده این دو ماده برمی گردد. مولکول کلر شامل دو اتم کلر با جرم بالا است، در حالی که اسید هیدروکلریک تنها یک اتم کلر دارد و اتم دیگر آن هیدروژن بسیار سبک می باشد. همین جایگزینی باعث کاهش قابل توجه وزن مولکولی HCl نسبت به کلر می شود.
از نظر رفتار فیزیکی نیز این تفاوت کاملا محسوس است. گاز کلر چگالی بالایی دارد و به طور قابل توجهی از هوا سنگین تر است. در رویدادهای تاریخی نیز مشاهده شده که این گاز در نزدیکی سطح زمین باقی می مانده است. اسید هیدروکلریک هرچند از هوا سنگین تر است، اما به اندازه کلر وزن ندارد و رفتار آن در پخش شدن حالتی میانی دارد.
این مقایسه به خوبی نشان می دهد افزودن یک اتم کلر اضافی چگونه می تواند جرم مولکولی را افزایش داده و بر ویژگی های گاز تاثیر بگذارد.
مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن فلوئورید
هیدروژن فلوئورید با فرمول HF سبک ترین عضو خانواده هیدروژن هالیدها به شمار می رود و از یک اتم هیدروژن و یک اتم فلوئور ساخته شده است. جرم مولکولی این ترکیب حدود 20 گرم بر مول است که بخش عمده آن به اتم فلوئور اختصاص دارد. اگر این عدد با جرم مولکولی اسید هیدروکلریک مقایسه شود، اختلاف قابل توجهی دیده می شود، زیرا HCl جرمی نزدیک به 36.46 گرم بر مول دارد.
دلیل اصلی این تفاوت به نوع هالوژن موجود در ساختار مولکول برمی گردد. فلوئور نسبت به کلر جرم بسیار کمتری دارد و همین موضوع باعث می شود مولکول HF سبک تر باشد. در عمل، جرم یک مولکول HF تنها کمی بیش از نصف جرم یک مولکول HCl است.
این اختلاف وزنی در رفتار فیزیکی نیز اثر می گذارد. گاز HF چگالی پایین تری نسبت به گاز هیدروژن کلرید دارد و در حالت گازی اندکی سریع تر پخش می شود و راحت تر به سمت بالا حرکت می کند. با این حال، در حالت مایع، پیوندهای هیدروژنی قوی در HF باعث افزایش نقطه جوش آن می شوند. این مقایسه نشان می دهد هرچه هالوژن سنگین تر شود، جرم مولکولی و ویژگی های فیزیکی گاز نیز تغییر می کند.
مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن برومید
هیدروژن برومید با فرمول HBr یکی از اعضای خانواده هیدروژن هالیدها است که در آن به جای کلر، اتم برم قرار دارد. برم نسبت به کلر جرم بسیار بیشتری دارد و همین موضوع باعث می شود جرم مولکولی HBr به حدود 80.9 گرم بر مول برسد. این عدد در مقایسه با جرم مولکولی اسید هیدروکلریک که حدود 36.46 گرم بر مول است، اختلاف قابل توجهی را نشان می دهد.
این تفاوت به آن معناست که هر مولکول هیدروژن برومید بیش از دو برابر یک مولکول HCl وزن دارد. نتیجه این افزایش جرم در رفتار فیزیکی گاز نیز دیده می شود. گاز HBr چگال تر است و در شرایط مشابه، آهسته تر از گاز هیدروکلریک در هوا پخش می شود.
اگر هیدروژن هالیدها را به صورت یک روند بررسی کنیم، از HF سبک به سمت HCl و سپس HBr، افزایش تدریجی جرم مولکولی کاملا مشخص است. این تغییر نشان می دهد جایگزینی یک اتم با عنصری سنگین تر چگونه می تواند وزن مولکول و ویژگی های وابسته به آن را به شکل چشمگیری دگرگون کند.
مقایسه جرم مولکولی اسید هیدروکلریک با هیدروژن یدید
هیدروژن یدید با فرمول HI سنگین ترین عضو شناخته شده خانواده هیدروژن هالیدها است و از یک اتم هیدروژن و یک اتم ید تشکیل می شود. اتم ید جرم بالایی دارد و به همین دلیل جرم مولکولی HI به حدود 127.9 گرم بر مول می رسد. این مقدار در مقایسه با جرم مولکولی اسید هیدروکلریک که حدود 36.46 گرم بر مول است، اختلاف بسیار زیادی را نشان می دهد.
علت اصلی این تفاوت به حضور اتم ید بازمی گردد که نسبت به کلر بسیار سنگین تر است. همین موضوع باعث می شود هر مولکول HI تقریبا سه و نیم برابر یک مولکول HCl وزن داشته باشد. این افزایش جرم فقط یک عدد نیست و در رفتار فیزیکی ماده نیز اثر مستقیم دارد.
گاز هیدروژن یدید به دلیل جرم بالا، چگالی بیشتری دارد و در شرایط یکسان کندتر از HCl در هوا پخش می شود. همچنین نقطه جوش HI بالاتر است و راحت تر به حالت مایع تبدیل می شود. این مقایسه نشان می دهد جایگزینی یک هالوژن سبک با عنصری سنگین چگونه می تواند جرم مولکولی و ویژگی های حرکتی و فیزیکی گاز را به طور چشمگیری تغییر دهد.
اهمیت تفاوت های جرم مولکولی
این مقایسه ها به خوبی نشان می دهند که چرا جرم مولکولی یکی از ویژگی های کلیدی در شیمی به حساب می آید. حتی تفاوت های ظاهرا کوچک در این کمیت می توانند باعث تغییرات محسوس در رفتار مواد شوند. برای نمونه، مولکول های بسیار سبک مانند هیدروژن یا متان معمولا سریع تر حرکت می کنند، پخش بالاتری دارند و چگالی آن ها پایین است، در حالی که مولکول های سنگین تر مانند دی اکسید کربن یا هیدروژن یدید حرکت کندتری دارند و بیشتر در بخش های پایین فضا تجمع پیدا می کنند.
اسید هیدروکلریک از نظر جرم مولکولی در میانه این بازه قرار می گیرد. وزن آن از ترکیبات ساده ای که تنها از هیدروژن، کربن، نیتروژن یا اکسیژن تشکیل شده اند بیشتر است، اما همچنان از موادی که دارای هالوژن های سنگین یا چند اتم سنگین هستند سبک تر محسوب می شود. همین جایگاه میانی باعث می شود رفتار HCl نه کاملا شبیه گازهای بسیار سبک باشد و نه مانند گازهای بسیار سنگین.
شناخت این تفاوت ها صرفا جنبه تئوری ندارد و در عمل نیز کاربرد فراوانی دارد. از پیش بینی حرکت و تجمع گازها گرفته تا محاسبه دقیق مقدار مواد در واکنش ها و رعایت نکات ایمنی، همگی به درک جرم مولکولی وابسته اند. در نهایت، مقایسه HCl با ترکیبات ساده دیگر دید جامعی از اهمیت این ویژگی بنیادی ارائه می دهد و نشان می دهد چرا در شیمی و کاربردهای صنعتی نقش مهمی ایفا می کند.
| ترکیب | فرمول | جرم مولکولی (گرم/مول) | سبک تر یا سنگین تر نسبت به HCl | نسبت جرمی (HCl=1) |
|---|---|---|---|---|
| اسید هیدروکلریک | HCl | 36.46 | مرجع | 1.00 |
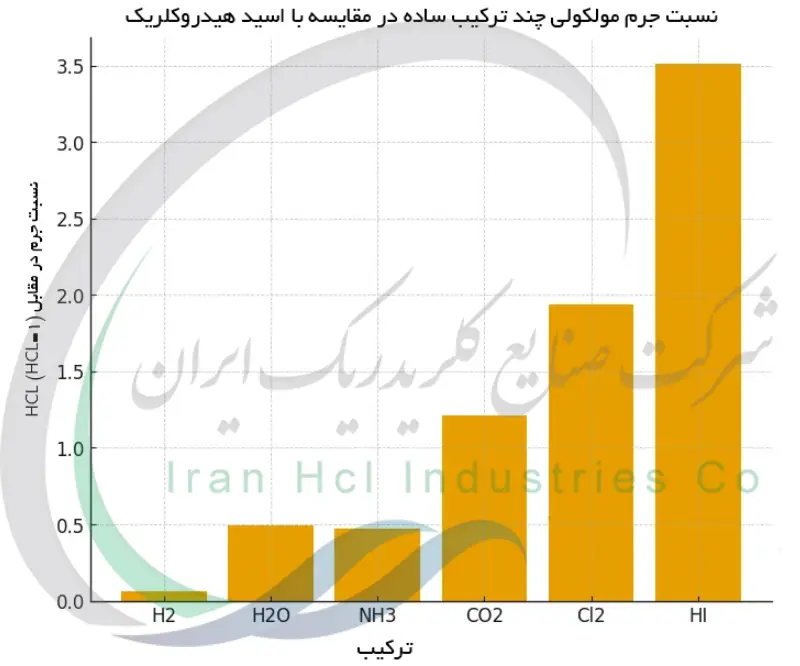
| گاز هیدروژن | H2 | 2.02 | سبک تر | 0.06 |
| آب | H2O | 18.02 | سبک تر | 0.49 |
| آمونیاک | NH3 | 17.03 | سبک تر | 0.47 |
| دی اکسید کربن | CO2 | 44.01 | سنگین تر | 1.21 |
| گاز کلر | Cl2 | 70.90 | سنگین تر | 1.94 |
| هیدروژن یدید | HI | 127.90 | سنگین تر | 3.51 |




