فهرست عناوین
- مقدمه
- ترکیب اسید هیدروکلریک (HCl)
- ساختار اتمی هیدروژن و کلر
- درک آرایش الکترونی در اتم ها
- لایه های الکترونی و تراز های انرژی
- هیدروژن: ساده ترین عنصر
- آرایش الکترونی اتم هیدروژن
- کلر: عنصری هالوژن و واکنش پذیر
- آرایش الکترونی اتم کلر
- الکترون های ظرفیت در هیدروژن و کلر
- شکل گیری پیوند کووالانسی در HCl از طریق به اشتراک گذاری الکترون ها
- قاعده هشت تایی و پایداری در HCl
- توزیع الکترون ها در لایه ها: هیدروژن در برابر کلر
- آرایش الکترونی و واکنش پذیری HCl
- آرایش الکترونی یون های HCl (H⁺ و Cl⁻)
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 12-09-1404
تاریخ بروزرسانی مقاله : 12-09-1404
تعداد کلمات : 3400
آدرس مقاله : لینک مقاله
پیکربندی الکترونی اتم های سازنده اسید کلریدریک

مقدمه
اسید هیدروکلریک (HCl) از یک اتم هیدروژن و یک اتم کلر تشکیل شده اند. خواص شیمیایی HCl به آرایش الکترون ها در اطراف اتم های تشکیل دهنده آن وابسته است. در شیمی به این ترتیب قرارگیری الکترون ها در اتم، اصطلاحاً آرایش الکترونی گفته می شود. دانستن آرایش الکترونی هیدروژن و کلر به درک علت پیوند خوردن این اتم ها و چگونگی رفتار HCl کمک می کند. این مقاله جامع به بررسی آرایش الکترونی اتم هایی که اسید هیدروکلریک را تشکیل می دهند می پردازد.
مباحث شامل ساختار پایه اتمی، چگونگی پر شدن تراز های انرژی توسط الکترون ها در اتم های هیدروژن و کلر، و نحوه تاثیر آرایش الکترونی آن ها بر تشکیل و ویژگی های HCl است. در بخش های کاربردی نیز اهمیت آرایش الکترونی به خوبی دیده می شود، به ویژه در صنایع که نیاز به مواد اولیه استاندارد و ایمن دارند؛ برای مثال در فرآیندهایی مرتبط با خرید اسید کلریدریک کلر پارس تبریز مخزن IBC که کیفیت شیمیایی ماده نقش تعیین کننده ای در عملکرد نهایی دارد.
ترکیب اسید هیدروکلریک (HCl)
HCl مولکولی ساده و دو اتمی است که از کنار هم قرار گرفتن یک اتم هیدروژن و یک اتم کلر به وجود آمده است. نسبت این دو عنصر در ساختار آن کاملا برابر و یک به یک است و همین سادگی، آن را به یکی از شناخته شده ترین ترکیبات شیمیایی تبدیل کرده است.
این ترکیب در حالت گازی با نام هیدروژن کلرید شناخته می شود، اما زمانی که وارد آب می گردد، به اسید هیدروکلریک تبدیل می شود؛ اسیدی که قدرت واکنش بالایی دارد و در کاربردهای مختلف مورد استفاده قرار می گیرد. با وجود ساختار ساده، رفتار شیمیایی HCl چندان ساده نیست و مستقیما به ویژگی های اتم های تشکیل دهنده آن مربوط می شود.
هیدروژن سبک ترین عنصر شناخته شده است و عدد اتمی آن یک می باشد. در مقابل، کلر عنصری سنگین تر از گروه هالوژن ها با عدد اتمی هفده است. تفاوت میان این دو عنصر از نظر جرم و آرایش الکترونی، نقش مهمی در نحوه پیوند آن ها دارد.
همین اختلاف در توانایی جذب الکترون باعث می شود پیوند میان هیدروژن و کلر حالت قطبی پیدا کند. این پیوند قطبی پایه رفتار اسیدی HCl را شکل می دهد. برای شناخت بهتر اسید هیدروکلریک، بررسی ویژگی های اتمی این دو عنصر و نحوه توزیع الکترون های آن ها نقطه شروع مناسبی به شمار می آید.
ساختار اتمی هیدروژن و کلر
هر اتم از یک هسته (شامل پروتون ها و نوترون ها) و الکترون هایی که به دور هسته در حال گردش هستند تشکیل شده است. عدد اتمی هر عنصر برابر با تعداد پروتون های موجود در هسته آن و همچنین تعداد الکترون های اتم خنثی آن عنصر است. هیدروژن عدد اتمی ۱ دارد، یعنی یک پروتون در هسته و یک الکترون در اطراف خود دارد. کلر دارای عدد اتمی ۱۷ است، به این معنا که هسته اش ۱۷ پروتون دارد و ۱۷ الکترون در پوسته های مختلف به دور آن حرکت می کنند.
این اختلاف چشمگیر بین تعداد ذرات زیر اتمی هیدروژن و کلر باعث می شوند که اتم های کلر بسیار بزرگ تر و از نظر ساختار الکترونی پیچیده تر از اتم های هیدروژن باشند. ساختار اتمی هیدروژن بسیار ساده و شامل تنها یک لایه الکترونی است، در حالی که الکترون های کلر در سه لایه الکترونی توزیع شده اند تا همه ۱۷ الکترون را در بر بگیرند. درک این تفاوت های پایه ای در ساختار هیدروژن و کلر پیش نیازی برای پرداختن به نحوه آرایش خاص الکترون های آن ها است.
در هر مورد، چیدمان الکترون ها (آرایش الکترونی) تعیین می کند که هر اتم چگونه با اتم های دیگر واکنش انجام داده و پیوند برقرار می کند. این مبانی همچنین پایه ای برای مباحث کاربردی تر هستند، از جمله بررسی جرم مولکولی اسید کلریدریک و محاسبه آن که درک دقیق آن وابسته به شناخت ساختار و تعداد ذرات زیراتمی تشکیلدهنده هر اتم است.
درک آرایش الکترونی در اتم ها
آرایش الکترونی روشی برای نشان دادن نحوه قرار گرفتن الکترون ها در لایه ها و مدارهای انرژی یک اتم است. هر عنصر با توجه به تعداد الکترون های خود، الگوی مشخص و ویژه ای دارد که ساختار درونی آن را توصیف می کند.
الکترون ها بر اساس قوانین مشخصی در اطراف هسته قرار می گیرند. طبق این اصول، ابتدا مدارهایی با انرژی کمتر پر می شوند و سپس الکترون ها به سطوح بالاتر منتقل می گردند. به همین دلیل، آرایش الکترونی معمولا به صورت مجموعه ای از مدارها و تعداد الکترون های هر کدام نوشته می شود و تصویر روشنی از وضعیت اتم ارائه می دهد.
دانستن آرایش الکترونی کمک می کند رفتار شیمیایی یک عنصر بهتر درک شود. این که یک اتم چگونه واکنش می دهد یا با چه عناصری پیوند برقرار می کند، تا حد زیادی به نحوه توزیع الکترون های آن بستگی دارد. به ویژه، الکترون هایی که در لایه بیرونی قرار دارند اهمیت بیشتری دارند، چون مستقیما در واکنش ها شرکت می کنند.
در واقع، آرایش الکترونی را می توان نقشه ای دانست که جایگاه الکترون ها را مشخص می کند. این نقشه پایه فهم بسیاری از الگوهای جدول تناوبی و تفاوت میان عناصر است.
پیش از بررسی ویژگی های هیدروژن و کلر، آشنایی با مفهوم آرایش الکترونی ضروری است، چون بدون آن درک پیوندها و رفتار شیمیایی این عناصر کامل نخواهد بود.
لایه های الکترونی و تراز های انرژی
الکترون های هر اتم در فاصله های متفاوتی از هسته قرار دارند و در لایه های انرژی جداگانه ساماندهی می شوند. این لایه ها از نزدیک ترین بخش به هسته با عدد یک شماره گذاری می شوند و هرچه عدد آن ها بزرگ تر باشد، انرژی بالاتری دارند و دورتر واقع شده اند.
هر لایه ظرفیت مشخصی برای نگهداری الکترون دارد. لایه اول فقط می تواند دو الکترون را در خود جای دهد، لایه دوم تا هشت الکترون را می پذیرد و لایه سوم توان نگهداری تعداد بیشتری را دارد. با افزایش شماره لایه، فضای بیشتری برای حضور الکترون ها فراهم می شود.
درون هر لایه، بخش های کوچک تری وجود دارد که زیرلایه نامیده می شوند. این زیرلایه ها با حروفی مانند s و p شناخته می شوند و هر کدام ظرفیت خاص خود را دارند. به زبان ساده، لایه اول تنها یک نوع زیرلایه دارد و لایه های بعدی ساختار پیچیده تری پیدا می کنند.
در اتم هیدروژن تنها یک الکترون در نزدیک ترین لایه قرار می گیرد، اما در اتم کلر که الکترون های بیشتری دارد، لایه های اول و دوم کامل می شوند و بخشی از لایه سوم نیز پر می گردد. شناخت این لایه ها پایه نوشتن آرایش الکترونی عناصر مختلف، از جمله ترکیباتی مانند HCl، به شمار می آید.
هیدروژن: ساده ترین عنصر
هیدروژن ساده ترین و سبک ترین عنصر شناخته شده در جدول تناوبی است. عدد اتمی آن یک است، یعنی در هسته خود تنها یک پروتون دارد و فقط یک الکترون پیرامون آن حرکت می کند. در شکل معمول هیدروژن، نوترونی وجود ندارد، هرچند گونه هایی مانند دوتریوم و تریتیم استثنا به شمار می آیند.
این عنصر تنها یک لایه الکترونی دارد و همان لایه نیز فقط با یک الکترون پر شده است. به همین دلیل، ساختار هیدروژن بسیار ساده و قابل فهم است و اغلب برای توضیح مفاهیم پایه شیمی از آن استفاده می شود.
در جدول تناوبی، هیدروژن در دوره اول قرار می گیرد و معمولا بالای گروه یک نمایش داده می شود، چون یک الکترون ظرفیت دارد. با این حال، رفتار شیمیایی آن همیشه کاملا شبیه فلزهای قلیایی نیست و در برخی واکنش ها شباهت هایی به هالوژن ها نشان می دهد.
نکته مهم این است که همین یک الکترون نقش تعیین کننده ای در واکنش پذیری هیدروژن دارد. از دست دادن، گرفتن یا به اشتراک گذاشتن این الکترون، پایه اصلی پیوندهای شیمیایی هیدروژن را تشکیل می دهد و اهمیت ویژه آن را در ترکیبات مختلف نشان می دهد.
آرایش الکترونی اتم هیدروژن
آرایش الکترونی هیدروژن به صورت 1s1 نوشته می شود و نشان می دهد این اتم تنها یک الکترون در نزدیک ترین مدار به هسته خود دارد. این مدار که با نام 1s شناخته می شود، در اولین تراز انرژی قرار گرفته و ساده ترین حالت توزیع الکترون را نشان می دهد.
لایه اول انرژی فقط یک اوربیتال از نوع s دارد و ظرفیت آن حداکثر دو الکترون است. در هیدروژن، تنها یک الکترون در این فضا قرار گرفته و به همین دلیل این اوربیتال به طور کامل پر نشده است. هیچ الکترونی در لایه های بالاتر وجود ندارد، چون کل اتم فقط همین یک الکترون را در اختیار دارد.
این وضعیت نیمه پر بودن لایه اول اهمیت زیادی دارد. از دید شیمیایی، اتم هیدروژن تمایل دارد به حالتی پایدارتر برسد. برای این کار یا الکترون خود را از دست می دهد یا یک الکترون دیگر به دست می آورد تا ظرفیت لایه اول تکمیل شود.
پر شدن این لایه با دو الکترون حالتی مشابه آرایش گاز نجیب هلیوم ایجاد می کند. همین میل به رسیدن به وضعیت پایدارتر، دلیل اصلی واکنش پذیری هیدروژن و توانایی آن در تشکیل پیوند با عناصر دیگر، مانند کلر در مولکول HCl، به شمار می آید.
کلر: عنصری هالوژن و واکنش پذیر
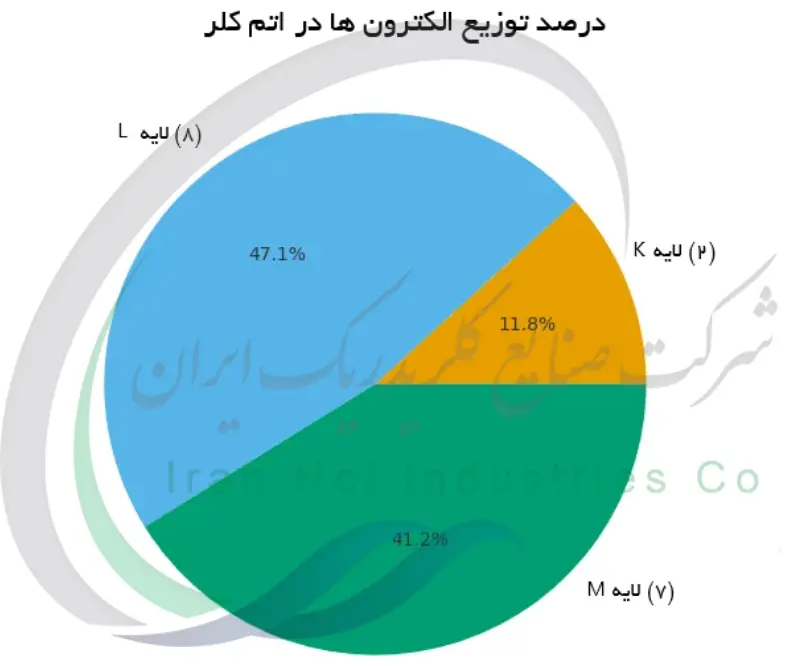
کلر یک عنصر شیمیایی با عدد اتمی ۱۷ است، بدین معنا که هر اتم کلر ۱۷ پروتون و ۱۷ الکترون دارد. کلر بخشی از خانواده هالوژن ها (گروه ۱۷ جدول تناوبی) است و به خاطر واکنش پذیری زیاد و رنگ سبز مایل به زرد گازش شناخته می شود. اتم های کلر به طور قابل توجهی بزرگ تر و پیچیده تر از اتم های هیدروژن هستند، زیرا پروتون ها، نوترون ها و الکترون های بسیار بیشتری دارند. کلر ۱۷ الکترون در سه پوسته اصلی دارند: ۲ الکترون در لایه اول، ۸ الکترون در لایه دوم و ۷ الکترون در لایه سوم.
این هفت الکترون در خارجی ترین لایه همان الکترون های ظرفیت هستند که رفتار شیمیایی کلر را تا حد زیادی تعیین می کنند. داشتن ۷ الکترون ظرفیت به این معنی است که کلر تنها یک الکترون با داشتن یک لایه بیرونی کامل (۸ الکترون در لایه آخر) فاصله دارد؛ بنابراین کلر عنصری بسیار واکنشگر است که تمایل دارد برای تکمیل لایه خود یک الکترون به دست آورد یا به اشتراک بگذارد. گرایش کلر به رسیدن به آرایش الکترونی پایدار، دلیل تشکیل ترکیباتی مثل اسید هیدروکلریک از پیوند آن با هیدروژن است.
آرایش الکترونی اتم کلر
آرایش الکترونی کلر نشان می دهد الکترون های این عنصر چگونه در لایه ها و مدارهای مختلف اطراف هسته پخش شده اند. کلر با عدد اتمی ۱۷، دارای هفده الکترون است که به ترتیب در ترازهای انرژی جای می گیرند.
در لایه اول، دو الکترون در مدار نزدیک به هسته قرار دارند و این لایه به طور کامل پر می شود. لایه دوم نیز هشت الکترون را در خود جای می دهد و به حالت پایدار می رسد. پس از آن نوبت به لایه سوم می رسد که هفت الکترون در آن قرار می گیرند و هنوز یک جای خالی باقی می ماند.
به همین دلیل، لایه بیرونی کلر کامل نیست و همین موضوع دلیل اصلی واکنش پذیری بالای این عنصر محسوب می شود. کلر تمایل دارد یک الکترون دیگر جذب کند تا آرایش لایه آخر آن کامل شود و به وضعیت پایدار برسد.
این ویژگی باعث می شود کلر به راحتی با عناصر دیگر وارد واکنش شود. بررسی آرایش الکترونی کلر کمک می کند دلیل رفتار شیمیایی آن و نقش فعالش در ترکیباتی مانند HCl بهتر درک شود.
الکترون های ظرفیت در هیدروژن و کلر
الکترون های ظرفیت به الکترون هایی گفته می شود که در بیرونی ترین لایه هر اتم قرار دارند. این الکترون ها نقش اصلی را در برقراری پیوندها و انجام واکنش های شیمیایی بازی می کنند و رفتار هر عنصر تا حد زیادی به تعداد و وضعیت آن ها بستگی دارد.
در ترکیب اسید هیدروکلریک، تعیین الکترون های ظرفیت بسیار ساده است. اتم هیدروژن تنها یک لایه دارد و همان لایه نیز فقط یک الکترون را در خود جای داده است، بنابراین هیدروژن یک الکترون ظرفیت دارد. در مقابل، کلر در لایه بیرونی خود هفت الکترون دارد که به آن ها الکترون های ظرفیت گفته می شود.
این مفهوم توضیح می دهد چرا اتم ها تمایل به واکنش نشان دادن دارند. هیدروژن با داشتن تنها یک الکترون در لایه اول، می تواند آن را از دست بدهد یا الکترون دیگری جذب کند تا به حالت پایدار برسد. از سوی دیگر، کلر فقط یک الکترون کم دارد تا لایه آخرش کامل شود و به همین دلیل به شدت به گرفتن یا شریک شدن یک الکترون تمایل دارد.
وقتی هیدروژن و کلر به هم نزدیک می شوند، الکترون های ظرفیت آن ها با هم جفت می شوند و پیوند میان این دو اتم شکل می گیرد. همین تعامل ساده میان الکترون های بیرونی است که تشکیل اسید هیدروکلریک و واکنش پذیری بالای آن را توضیح می دهد.
شکل گیری پیوند کووالانسی در HCl از طریق به اشتراک گذاری الکترون ها
وقتی اتم هیدروژن و اتم کلر به هم نزدیک می شوند، برای تشکیل مولکول HCl الکترون های خود را با هم شریک می کنند. این فرایند از طریق یک پیوند کووالانسی انجام می گیرد؛ یعنی هر کدام از این دو اتم، الکترون ظرفیت خود را در اختیار پیوند قرار می دهد تا یک جفت الکترون مشترک شکل بگیرد.
با ایجاد این پیوند، هر دو اتم به وضعیت مناسب تری از نظر الکترونی می رسند. هیدروژن که تنها یک الکترون دارد، با این اشتراک گذاری عملا لایه اول خود را کامل می کند و به حالتی شبیه گاز هلیوم می رسد. در همین زمان، کلر نیز با داشتن هشت الکترون در لایه بیرونی خود، به آرایشی پایدار شبیه آرگون دست پیدا می کند.
این نوع پیوند فقط یک اتصال ساده نیست. پیوند کووالانسی میان هیدروژن و کلر حالت قطبی دارد، چون کلر توان بیشتری در جذب الکترون ها دارد. به همین دلیل، جفت الکترون مشترک کمی به سمت کلر متمایل می شود و توزیع بار یکنواخت نیست.
با این حال، نکته اصلی این است که هر دو اتم از طریق به اشتراک گذاشتن الکترون ها به تعادل الکترونی می رسند. تشکیل مولکول HCl نتیجه مستقیم تمایل اتم ها به رسیدن به آرایش پایدار است. این سازوکار ساده اما مهم، پایه بسیاری از رفتارهای شیمیایی اسید هیدروکلریک را توضیح می دهد.
قاعده هشت تایی و پایداری در HCl
یکی از مفاهیم پایه در شیمی که دلیل شکل گیری بسیاری از پیوندها را توضیح می دهد، قانون هشت تایی است. بر اساس این قانون، بیشتر اتم ها تمایل دارند تعداد الکترون های لایه بیرونی خود را به عدد هشت برسانند تا به وضعیتی پایدار شبیه گازهای نجیب دست پیدا کنند. این هدف می تواند با گرفتن، از دست دادن یا شریک شدن الکترون ها محقق شود.
کلر نمونه روشنی از این رفتار است. این عنصر در لایه خارجی خود هفت الکترون دارد و تنها یک الکترون کم دارد تا لایه اش کامل شود. همین کمبود باعث می شود کلر میل زیادی به واکنش نشان دادن داشته باشد و به دنبال راهی برای تکمیل لایه بیرونی خود باشد.
هیدروژن اما شرایط متفاوتی دارد. از آنجا که فقط یک لایه الکترونی دارد، رسیدن به دو الکترون برایش کافی است. در واقع هیدروژن به جای قانون هشت تایی، از قانون دو تایی پیروی می کند و با داشتن دو الکترون به حالتی پایدار شبیه هلیوم می رسد.
زمانی که هیدروژن و کلر با هم پیوند برقرار می کنند، هر دو به خواسته الکترونی خود می رسند. کلر با شریک شدن الکترون هیدروژن، لایه بیرونی اش را کامل می کند و هیدروژن نیز با همین اشتراک گذاری، لایه اول خود را پر می سازد.
به همین دلیل، مولکول HCl پس از تشکیل ساختاری پایدار دارد. این مثال نشان می دهد که چگونه یک قانون ساده می تواند علت پیوند میان اتم ها و شکل گیری ترکیبات شیمیایی را به شکلی قابل فهم توضیح دهد.
توزیع الکترون ها در لایه ها: هیدروژن در برابر کلر
برای اینکه تفاوت میان آرایش الکترونی هیدروژن و کلر بهتر درک شود، می توان به نحوه پخش الکترون های آن ها در لایه های مختلف نگاه کرد. این مقایسه به شکل ساده نشان می دهد هر اتم چگونه ساختار الکترونی متفاوتی دارد.
هیدروژن تنها یک الکترون دارد و همین الکترون در نزدیک ترین لایه به هسته قرار می گیرد. این لایه که اولین لایه انرژی است، تنها فضای مورد استفاده هیدروژن محسوب می شود و هیچ الکترونی در لایه های بالاتر وجود ندارد. به بیان ساده، ساختار هیدروژن بسیار فشرده و محدود است.
در مقابل، کلر اتمی با الکترون های بیشتر است. این عنصر ۱۷ الکترون دارد که در چند لایه مختلف پخش شده اند. الکترون های کلر ابتدا لایه اول را پر می کنند، سپس به لایه دوم می روند و در نهایت بخشی از لایه سوم را اشغال می کنند. لایه های بعدی در این اتم خالی باقی می مانند.
هر لایه انرژی ظرفیت مشخصی دارد. لایه اول فقط دو الکترون را می پذیرد، لایه دوم تا هشت الکترون جا می دهد و لایه سوم می تواند تعداد بیشتری را در خود نگه دارد، هرچند کلر از تمام ظرفیت آن استفاده نمی کند.
این مقایسه به خوبی نشان می دهد چرا هیدروژن فقط یک الکترون فعال دارد، در حالی که کلر ساختار پیچیده تری با چند لایه الکترونی دارد.
| شماره لایه | نام لایه | حداکثر الکترون | الکترون های هیدروژن | الکترون های کلر |
|---|---|---|---|---|
| ۱ | K | ۲ | ۱ | ۲ |
| ۲ | L | ۸ | ۰ | ۸ |
| ۳ | M | ۱۸ | ۰ | ۷ |
| ۴ | N | ۳۲ | ۰ | ۰ |
| ۵ | O | ۵۰ | ۰ | ۰ |
| ۶ | P | ۷۲ | ۰ | ۰ |
| ۷ | Q | ۹۸ | ۰ | ۰ |
آرایش الکترونی و واکنش پذیری HCl
تفاوت میان آرایش الکترونی و میزان کشش الکترون ها در هیدروژن و کلر نقش مهمی در رفتار شیمیایی HCl دارد. کلر به دلیل ساختار الکترونی خود، تمایل زیادی به جذب الکترون نشان می دهد و همین ویژگی باعث می شود پیوند میان هیدروژن و کلر حالت نابرابر پیدا کند.
در این پیوند، الکترون های مشترک بیشتر به سمت کلر کشیده می شوند. نتیجه این موضوع، قطبی شدن مولکول HCl است؛ یعنی یک سر مولکول بار منفی نسبی و سر دیگر بار مثبت نسبی پیدا می کند. این تفاوت بار زمینه را برای واکنش پذیری بالای این ترکیب فراهم می سازد.
وقتی HCl وارد آب می شود، این نابرابری الکترونی اثر خود را به طور کامل نشان می دهد. کلر الکترون پیوندی را نزد خود نگه می دارد و به یون کلرید تبدیل می شود که از نظر الکترونی بسیار پایدار است. در مقابل، هیدروژن الکترون خود را از دست می دهد و به صورت یون H⁺ در محلول باقی می ماند.
همین فرایند باعث می شود اسید هیدروکلریک در آب به طور کامل تفکیک شود و به عنوان یک اسید قوی شناخته شود. آزاد شدن آسان پروتون ویژگی اصلی این اسید است که آن را از اسیدهای ضعیف متمایز می کند.
در واقع، تمایل کلر به تکمیل لایه بیرونی و توانایی هیدروژن برای از دست دادن تنها الکترونش، نیروی محرک این واکنش است. پایداری یون های حاصل نسبت به اتم های خنثی باعث می شود این تفکیک به سادگی انجام شود. به همین دلیل، قدرت اسیدی و واکنش پذیری بالای HCl مستقیماً به ویژگی های الکترونی سازندگان آن وابسته است.
آرایش الکترونی یون های HCl (H⁺ و Cl⁻)
وقتی اسید هیدروکلریک در آب حل می شود یا وارد یک واکنش اسید و باز می گردد، به ذرات بارداری تبدیل می شود که به آن ها یون گفته می شود. در این حالت، HCl به یون هیدروژن و یون کلرید تفکیک می گردد و رفتار شیمیایی محلول را شکل می دهد.
یون هیدروژن در واقع همان اتم هیدروژن است که الکترون خود را از دست داده است. با حذف این الکترون، چیزی جز یک پروتون باقی نمی ماند. به همین دلیل، یون H⁺ هیچ الکترونی ندارد و بسیار واکنش پذیر است. این یون معمولا به تنهایی در آب باقی نمی ماند و خیلی سریع به مولکول های آب متصل می شود.
در طرف مقابل، یون کلرید قرار دارد. این یون زمانی شکل می گیرد که اتم کلر یک الکترون اضافی دریافت کند. با این الکترون جدید، تعداد الکترون های کلر به ۱۸ می رسد و لایه های الکترونی آن کاملا پر می شوند. این وضعیت از نظر انرژی بسیار پایدار است و شبیه ساختار گازهای نجیب می باشد.
همین پایداری بالا باعث می شود یون کلرید تمایل چندانی به واکنش دوباره نداشته باشد. رسیدن کلر به این حالت پایدار یکی از دلایل اصلی است که اسید هیدروکلریک در آب به طور کامل یونیزه می شود.
پس از جدایی یون ها، یون هیدروژن اغلب به آب می چسبد و یون هیدرونیوم را می سازد، در حالی که یون کلرید به صورت آزاد در محلول باقی می ماند. در نهایت، هر دو ذره به وضعیتی پایدار رسیده اند و همین موضوع رفتار قوی و مشخص HCl در محلول های آبی را توضیح می دهد.




