فهرست عناوین
- مقدمه
- درک جرم مولکولی
- مروری بر اسید هیدروکلریک (HCl)
- فرمول شیمیایی و ترکیب HCl
- جرم اتمی هیدروژن در HCl
- جرم اتمی کلر در HCl
- محاسبه جرم مولکولی HCl
- درصد ترکیب HCl بر حسب جرم
- جرم مولکولی و جرم مولی HCl
- اهمیت جرم مولکولی در محاسبات شیمیایی
- استفاده از جرم مولکولی HCl در آزمایشگاه
- مقایسه جرم مولکولی HCl با ترکیبات دیگر
- تغییرات ایزوتوپی و جرم مولکولی HCl
- جرم مولکولی و خواص فیزیکی HCl
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 07-09-1404
تاریخ بروزرسانی مقاله : 07-09-1404
تعداد کلمات : 3000
آدرس مقاله : لینک مقاله
جرم مولکولی اسید کلریدریک و محاسبه آن

مقدمه
اسید هیدروکلریک (HCl) که با نام اسید کلریدریک نیز شناخته می شود، یک ترکیب شیمیایی شناخته شده است و درک جرم مولکولی آن در شیمی امری بنیادی است. جرم مولکولی یک ماده نشان دهنده جرم یک مولکول نسبت به مقیاس یکای جرم اتمی است. برای اسید هیدروکلریک که از اتم های هیدروژن و کلر تشکیل شده است، جرم مولکولی را می توان با جمع کردن جرم های اتمی این اجزای تشکیل دهنده تعیین کرد.
این مقدار در محاسبات گوناگون از آماده سازی های آزمایشگاهی گرفته تا کاربردهای صنعتی نقش مهمی دارد. در این بررسی جامع، به این می پردازیم که جرم مولکولی اسید هیدروکلریک چقدر است، چگونه محاسبه می شود و چرا اهمیت دارد. همچنین جرم مولکولی HCl را با ترکیبات دیگر مقایسه خواهیم کرد و مفاهیم مرتبط مانند جرم مولی، تغییرات ایزوتوپی و درصد ترکیب جرمی را بررسی می کنیم.
در همین راستا، برای کاربردهای صنعتی که نیازمند حجم های بالا و دقت در ترکیب هستند، انجام خرید اسید کلریدریک کلر پارس تبریز بشکه 220 لیتری به عنوان یکی از گزینه های مطمئن تأمین، اهمیت بیشتری پیدا می کند؛ زیرا درک درست جرم مولکولی این ماده نقش مهمی در کنترل کیفیت و کارایی آن دارد. در پایان درک روشنی از جرم مولکولی اسید هیدروکلریک و نحوه محاسبه آن خواهید داشت و خواهید دید که چگونه این عدد به ظاهر ساده نقش مهمی در زمینه های علمی و عملی ایفا می کند.
درک جرم مولکولی
جرم مولکولی نشان می دهد یک مولکول چه مقدار جرم دارد و در واقع مجموع جرم همه اتم هایی است که آن مولکول را ساخته اند. برای به دست آوردن این مقدار، جرم هر اتم موجود در مولکول با هم جمع می شود تا وزن کلی آن مشخص گردد.
در علم شیمی، برای بیان جرم مولکول ها از واحدی به نام جرم اتمی یا دالتون استفاده می شود. این واحد بر اساس جرم اتم کربن ۱۲ تعریف شده و برابر با یک دوازدهم جرم آن است. به همین دلیل، جرم مولکولی معمولا به صورت نسبی بیان می شود و از نظر علمی بدون واحد به حساب می آید، هرچند در عمل از همان واحد جرم اتمی استفاده می کنند.
به طور مثال، وقتی گفته می شود جرم مولکولی یک ماده ۱۸ است، یعنی جرم آن مولکول ۱۸ برابر یک دوازدهم جرم اتم کربن ۱۲ می باشد. این مفهوم کمک می کند بتوان جرم مولی را محاسبه کرد؛ یعنی بدانیم یک مول از یک ماده چه وزنی دارد.
درک جرم مولکولی اهمیت زیادی دارد، چون پایه بسیاری از محاسبات شیمیایی است. با استفاده از آن، شیمیدان ها می توانند از روی وزن مواد، تعداد مولکول ها را تخمین بزنند و واکنش های شیمیایی را به شکل دقیق بررسی کنند.
مروری بر اسید هیدروکلریک (HCl)
اسید هیدروکلریک با فرمول HCl از ساده ترین ترکیبات شیمیایی به شمار می رود و تنها از دو اتم هیدروژن و کلر ساخته شده است. این ماده در حالت خالص به صورت گاز هیدروژن کلرید وجود دارد، اما وقتی در آب حل می شود، به اسیدی قوی و خورنده تبدیل می گردد که کاربردهای فراوانی دارد.
این اسید یکی از پرمصرف ترین مواد شیمیایی در آزمایشگاه ها و صنایع مختلف است. از آن برای انجام واکنش های شیمیایی، تمیزکاری فلزات، تولید ترکیبات معدنی و بسیاری از فرآیندهای صنعتی استفاده می شود. جالب است بدانیم که اسید هیدروکلریک به طور طبیعی هم در بدن انسان حضور دارد و بخش مهمی از شیره معده را تشکیل می دهد و به هضم غذا کمک می کند.
از نظر ساختار مولکولی، HCl اهمیت ویژه ای دارد. پیوند بین هیدروژن و کلر از نوع کووالانسی قطبی است، چون کلر توانایی بیشتری در جذب الکترون دارد. همین ویژگی باعث می شود این ترکیب به راحتی در آب حل شود و رفتار اسیدی شدیدی از خود نشان دهد.
در محلول آبی، HCl تقریبا به طور کامل به یون های هیدروژن و کلرید جدا می شود. به همین دلیل، این اسید نمونه ای مناسب برای درک مفاهیم پایه شیمی مانند جرم مولکولی، ساختار مواد و ارتباط آن با واکنش پذیری محسوب می شود.
فرمول شیمیایی و ترکیب HCl
فرمول شیمیایی اسید هیدروکلریک HCl است که نشان می دهد هر مولکول از یک اتم هیدروژن (H) و یک اتم کلر (Cl) تشکیل شده است. این نسبت یک به یک اتمی باعث می شود HCl از نظر ترکیب یک مولکول بسیار ساده باشد. هیدروژن سبک ترین عنصر است، در حالی که کلر یک عنصر هالوژن سنگین تر است. ترکیب این دو یک مولکول با اندازه مولکولی متوسط ایجاد می کند. در فرمول HCl اندیس هر عنصر ۱ در نظر گرفته می شود که معمولاً نوشته نمی شود.
این فرمول ساده همچنین بدان معنا است که محاسبه هر کمیت وابسته به فرمول، مانند جرم مولکولی، نسبتاً آسان است زیرا تنها حاصل جمع جرم یک اتم هیدروژن و یک اتم کلر می باشد. ترکیب از نظر تعداد اتم ها یک اتم H و یک اتم Cl مستقیماً به ترکیب جرمی تبدیل می شود که شدیداً به سمت کلر متمایل است، زیرا اتم های کلر به مراتب سنگین تر از اتم های هیدروژن هستند. به همین دلیل در بسیاری از منابع علمی، بخش هایی مانند فرمول شیمیایی اسید کلریدریک (HCL) و اجزای آن به عنوان نقطه آغاز تحلیل مطرح می شود، زیرا درک همین ساختار ساده مقدمه ای برای تعیین دقیق جرم مولکولی و بررسی نقش هر اتم در جرم کلی مولکول است.
جرم اتمی هیدروژن در HCl
هیدروژن با نماد H اولین عنصر در جدول تناوبی است و عدد اتمی آن ۱ است. این عنصر سبک ترین عنصر می باشد و جرم اتمی آن تقریباً 1.008 واحد جرم اتمی (amu) است. این جرم اتمی در واقع یک میانگین وزنی است که فراوانی ایزوتوپ های طبیعی هیدروژن را لحاظ می کند. در محاسبه جرم مولکولی اسید هیدروکلریک، اتم هیدروژن حدود 1.008 واحد به جرم کل مولکول کمک می کند. از آنجا که جرم اتمی هیدروژن بسیار کم است، معمولاً در ترکیب هایی که هیدروژن به عناصر سنگین تر متصل است تنها تأثیر اندکی بر جرم کلی ترکیب دارد.
در HCl جرم اتم هیدروژن بخش بسیار کوچکی از جرم کل مولکول را تشکیل می دهد. با این حال حضور آن برای هویت و شیمی HCl حیاتی است بدون آن هیدروژن، عملاً با یک مولکول یا اتم کلر تنها روبرو بودیم. در محاسبات، از جرم اتمی هیدروژن (1.008) به عنوان یکی از اجزای مجموع استفاده می کنیم.
جرم اتمی کلر در HCl
کلر با نماد Cl یکی از عناصر گروه هالوژن ها است و عدد اتمی ۱۷ دارد. این عنصر در مقایسه با هیدروژن جرم بسیار بیشتری دارد و به همین دلیل سهم اصلی وزن ترکیباتی مانند HCl را به خود اختصاص می دهد.
جرم اتمی کلر عددی صحیح نیست و حدود ۳۵٫۴۵ واحد جرم اتمی در نظر گرفته می شود. دلیل این موضوع به ترکیب طبیعی کلر برمی گردد. کلر در طبیعت از دو ایزوتوپ پایدار تشکیل شده است؛ کلر ۳۵ که بخش عمده را شامل می شود و کلر ۳۷ که مقدار کمتری دارد. نسبت این دو ایزوتوپ باعث می شود عدد میانگین جرم اتمی کلر به صورت اعشاری بیان شود.
در محاسبات شیمیایی، از همین مقدار میانگین استفاده می شود، چون نمونه های واقعی کلر نیز همین ترکیب ایزوتوپی را دارند. در مولکول HCl، بخش اعظم جرم مربوط به اتم کلر است و سهم هیدروژن بسیار ناچیز محسوب می شود.
در واقع نزدیک به ۹۷ درصد جرم کل مولکول HCl از کلر ناشی می شود. به همین علت، انتخاب عدد دقیق برای جرم اتمی کلر اهمیت زیادی دارد. گاهی برای ساده سازی محاسبات آموزشی عدد ۳۵٫۵ به کار می رود، اما مقدار دقیق تر نتیجه واقع بینانه تری ارائه می دهد.
محاسبه جرم مولکولی HCl
محاسبه جرم مولکولی اسید هیدروکلریک به دلیل ساختار ساده آن کار پیچیده ای نیست. این ترکیب تنها از یک اتم هیدروژن و یک اتم کلر تشکیل شده و برای به دست آوردن جرم مولکولی کافی است جرم هر دو اتم با هم جمع شوند.
بر اساس مقادیر درج شده در جدول تناوبی، جرم اتمی هیدروژن حدود ۱٫۰۰۸ واحد و جرم اتمی کلر نزدیک به ۳۵٫۴۵ واحد جرم اتمی است. وقتی این دو عدد کنار هم قرار می گیرند، جرم یک مولکول HCl حدود ۳۶٫۴۶ واحد به دست می آید. این عدد همان جرم مولکولی نسبی اسید هیدروکلریک محسوب می شود.
اگر همین مقدار را در مقیاس مولی بیان کنیم، نتیجه به صورت ۳۶٫۴۶ گرم بر مول خواهد بود. به بیان ساده، یک مول از مولکول های HCl چنین جرمی دارد. این عدد در محاسبات شیمیایی بسیار کاربردی است و به تبدیل جرم به تعداد مول یا تعداد ذرات کمک می کند.
در برخی آموزش ها برای راحتی کار، از مقادیر گرد شده استفاده می شود. در این حالت جرم هیدروژن را ۱ و جرم کلر را ۳۵٫۵ در نظر می گیرند که حاصل آن حدود ۳۶٫۵ گرم بر مول است. این مقدار به عدد واقعی نزدیک است، اما برای محاسبات دقیق تر بهتر است از مقدار کامل استفاده شود.
این مثال به خوبی نشان می دهد که بخش اصلی جرم مولکول HCl مربوط به کلر است. دانستن جرم مولکولی به شیمیدان ها امکان می دهد واکنش ها را دقیق تر بررسی کرده و مقدار مواد مصرفی یا تولیدی را به درستی محاسبه کنند.
درصد ترکیب HCl بر حسب جرم
درصد ترکیب جرمی نشان می دهد هر عنصر چه سهمی از وزن کل یک ترکیب شیمیایی را به خود اختصاص داده است. این مفهوم کمک می کند بفهمیم در یک ماده مشخص، کدام عنصر سنگین تر است و کدام بخش کمتری از جرم را تشکیل می دهد.
در مورد اسید هیدروکلریک، محاسبه این درصدها بر پایه جرم مولکولی آن انجام می شود. جرم کل یک مولکول HCl حدود ۳۶٫۴۶ واحد است که از این مقدار، نزدیک به ۱٫۰۰۸ واحد مربوط به هیدروژن و حدود ۳۵٫۴۵ واحد متعلق به کلر است. با تقسیم جرم هر عنصر بر جرم کل و ضرب آن در صد، می توان سهم جرمی هر کدام را به دست آورد.
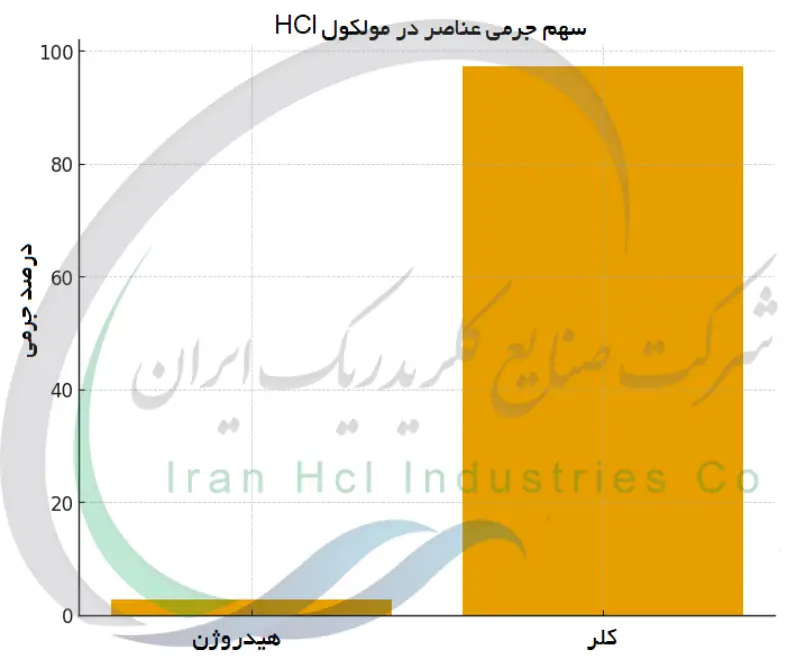
نتیجه این محاسبه نشان می دهد که هیدروژن تنها حدود ۲٫۷۶ درصد از جرم کل HCl را تشکیل می دهد. در مقابل، سهم کلر بسیار بیشتر است و چیزی در حدود ۹۷٫۲۴ درصد وزن این مولکول به آن اختصاص دارد. این اختلاف بزرگ به خوبی نشان می دهد که عنصر سنگین تر چگونه می تواند بر جرم نهایی یک ترکیب غلبه داشته باشد.
شناخت درصد ترکیب جرمی برای بررسی فرمول های شیمیایی و تحلیل مواد اهمیت زیادی دارد. نکته جالب اینجاست که با وجود سهم وزنی بسیار کم هیدروژن، همین عنصر نقش اصلی را در رفتار شیمیایی HCl ایفا می کند. آزاد شدن هیدروژن به شکل پروتون در محلول، دلیل اصلی خاصیت اسیدی این ترکیب است و اهمیت آن را فراتر از عدد جرمش نشان می دهد.
جرم مولکولی و جرم مولی HCl
تفاوت میان جرم مولکولی و جرم مولی موضوعی است که در نگاه اول ممکن است گیج کننده به نظر برسد، اما با کمی دقت می توان آن را ساده درک کرد. این دو مفهوم به هم مرتبط هستند، ولی هر کدام کاربرد و معنی خاص خود را دارند.
جرم مولکولی به وزن یک مولکول واحد از یک ماده اشاره دارد. این مقدار معمولاً با واحد جرم اتمی بیان می شود و نشان می دهد یک مولکول در مقیاس اتمی چه جرمی دارد. برای نمونه، جرم مولکولی HCl حدود ۳۶٫۴۶ واحد جرم اتمی است، یعنی یک مولکول از این ماده چنین وزنی دارد.
در مقابل، جرم مولی درباره مقدار بسیار بزرگی از همان مولکول ها صحبت می کند. جرم مولی برابر است با جرم یک مول از ماده که شامل عدد آووگادرو مولکول می شود و واحد آن گرم بر مول است. در مورد اسید هیدروکلریک، جرم مولی نیز ۳۶٫۴۶ گرم بر مول می باشد.
نکته جالب اینجاست که عدد جرم مولکولی و جرم مولی یکسان است، اما مفهوم آن ها فرق می کند. یکی مربوط به یک مولکول است و دیگری مربوط به یک مول از همان ماده. تفاوت اصلی در مقیاس و واحد اندازه گیری است، نه در مقدار عددی.
در عمل، جرم مولکولی بیشتر در توضیح ساختار و ویژگی های مولکولی به کار می رود، در حالی که جرم مولی ابزار اصلی محاسبات آزمایشگاهی و صنعتی محسوب می شود. شناخت این تفاوت به درک بهتر محاسبات شیمیایی کمک زیادی می کند.
اهمیت جرم مولکولی در محاسبات شیمیایی
دانستن جرم مولکولی ترکیبی مانند اسید هیدروکلریک برای انواع محاسبات شیمیایی ضروری است. یکی از رایج ترین کاربرد تبدیل بین جرم و مول یک ماده است. برای مثال، اگر شیمیدانی مقدار معینی HCl داشته باشد و بخواهد تعداد مول های آن را محاسبه کند، از جرم مولی HCl به عنوان عامل تبدیل استفاده می کند. از آنجا که 36.46 گرم HCl برابر با یک مول است، نمونه ای با نیمی از این جرم (مثلاً 18.23 گرم) 0.5 مول خواهد بود و به همین ترتیب. مثلاً برای خنثی کردن مقدار معینی باز توسط HCl، باید بدانیم چند گرم HCl (با توجه به جرم مولی آن) معادل مول های مورد نیاز است. علاوه بر این، برای تهیه محلول های اسیدی با مولاریته مشخص، دانستن جرم دقیق HCl مورد نیاز (بر اساس جرم مولکولی آن) ضروری است.
استفاده از جرم مولکولی HCl در آزمایشگاه
در کارهای آزمایشگاهی و همچنین در واحدهای صنعتی، برای اندازه گیری یا آماده سازی مقدار مشخصی از اسید هیدروکلریک، دانستن جرم مولی این ماده اهمیت زیادی دارد. هر زمان که صحبت از مقدار دقیق HCl می شود، محاسبات بر پایه جرم مولکولی یا جرم مولی انجام می گیرد.
برای نمونه، فرض کنید نیاز به تهیه یک لیتر محلول یک مولار اسید هیدروکلریک وجود دارد. در این حالت، دقیقا یک مول HCl لازم است. با توجه به اینکه جرم مولی این اسید حدود ۳۶٫۴۶ گرم بر مول است، می توان نتیجه گرفت که این مقدار HCl باید در حجم نهایی محلول وجود داشته باشد.
در عمل، اسید هیدروکلریک معمولا به صورت محلول غلیظ یا گاز در دسترس است و کمتر پیش می آید که گاز خالص آن وزن شود. به همین دلیل، محاسبات مربوط به جرم مولی کمک می کند مشخص شود چه مقدار از اسید غلیظ باید رقیق شود تا میزان مورد نظر HCl به دست آید.
همین منطق در روش هایی مانند تیتر کردن یا انجام واکنش های شیمیایی نیز کاربرد دارد. با دانستن جرم مولی، می توان به راحتی مقدار لازم اسید را برای شرکت در واکنش محاسبه کرد.
در مقیاس صنعتی نیز این اصول بدون تغییر باقی می مانند، فقط حجم و جرم ها بزرگ تر می شوند. در نهایت، جرم مولی اسید هیدروکلریک ابزاری اساسی برای کار دقیق، ایمن و قابل کنترل با این ماده محسوب می شود.
مقایسه جرم مولکولی HCl با ترکیبات دیگر
جرم مولکولی اسید هیدروکلریک را می توان با مقایسه آن با جرم مولکولی چند ترکیب ساده دیگر که حاوی هیدروژن هستند بهتر درک کرد. در زیر مقایسه ای میان HCl و چند ترکیب از این دست ارائه شده است؛ از مولکول سبکی مانند متان گرفته تا هیدروهالیدهای سنگین تر:
| ترکیب | فرمول | جرم مولی (گرم بر مول) | درصد جرم هیدروژن | درصد جرم عنصر دیگر |
|---|---|---|---|---|
| متان | CH₄ | 16.04 | 25.13% | 74.87% (کربن) |
| آمونیاک | NH₃ | 17.03 | 17.75% | 82.25% (نیتروژن) |
| آب | H₂O | 18.02 | 11.19% | 88.81% (اکسیژن) |
| اسید هیدروفلوئوریک | HF | 20.00 | 5.04% | 94.96% (فلوئور) |
| اسید هیدروکلریک | HCl | 36.46 | 2.76% | 97.24% (کلر) |
| اسید هیدروبرومیک | HBr | 80.91 | 1.25% | 98.75% (برم) |
| اسید هیدرویدیک | HI | 127.91 | 0.79% | 99.21% (ید) |
همان طور که در جدول مشاهده می شود، جرم مولی HCl (معادل 36.46 گرم بر مول) بیشتر از مولکول هایی مانند آب یا آمونیاک است اما بسیار کمتر از جرم مولی اسید هیدروبرومیک و اسید هیدرویدیک می باشد. داده ها به روشنی نشان می دهند که هرچه عنصر دیگر سنگین تر باشد، درصد جرمی هیدروژن کم تر است. در مورد HCl، هیدروژن تنها حدود 2.8% از جرم را تشکیل می دهد و این امر تأیید می کند که کلر بر جرم مولکول غلبه دارد.
تغییرات ایزوتوپی و جرم مولکولی HCl
جرم مولکولیای که برای اسید هیدروکلریک بیان می شود، یک مقدار میانگین است و به این معنا نیست که همه مولکول های HCl دقیقاً جرم یکسانی دارند. این عدد بر پایه جرم های اتمی متوسط عناصر تشکیل دهنده محاسبه شده و اختلاف های طبیعی را در نظر می گیرد.
در مورد هیدروژن، تقریباً تمام مولکول های HCl دارای هیدروژن معمولی هستند که به آن پروتیوم گفته می شود. به همین دلیل، از نظر هیدروژن تفاوت محسوسی بین مولکول ها وجود ندارد. فقط در شرایط خاص و آزمایشگاهی ممکن است هیدروژن سنگین تر، یعنی دوتریوم، جایگزین شود که در این صورت جرم مولکول کمی افزایش پیدا می کند.
داستان اصلی اختلاف جرم به عنصر کلر برمی گردد. کلر در طبیعت به صورت دو نوع پایدار وجود دارد که یکی سبک تر و دیگری سنگین تر است. اگر مولکول HCl دارای کلر سبک باشد، جرم آن کمتر خواهد بود و اگر کلر سنگین تر داشته باشد، وزن مولکول افزایش پیدا می کند.
در یک نمونه معمولی از اسید هیدروکلریک، بیشتر مولکول ها کلر سبک دارند و بخش کمتری شامل کلر سنگین هستند. عدد ۳۶٫۴۶ که به عنوان جرم مولکولی HCl شناخته می شود، در واقع میانگین این ترکیب طبیعی است.
این تفاوت های جزئی معمولاً تأثیر مهمی بر رفتار شیمیایی HCl ندارند و در محاسبات روزمره نادیده گرفته می شوند. بنابراین، جرم مولکولی اعلام شده یک عدد میانگین است که تنوع طبیعی مولکول ها را ساده سازی می کند.
جرم مولکولی و خواص فیزیکی HCl
جرم مولکولی یک ماده می تواند روی بعضی از ویژگی های فیزیکی آن اثر بگذارد، به ویژه زمانی که با گازها سر و کار داریم. اسید هیدروکلریک هم از این قاعده مستثنا نیست و وزن مولکولی آن نقش مهمی در نحوه رفتار این گاز ایفا می کند.
جرم مولی HCl حدود ۳۶٫۴۶ گرم بر مول است، در حالی که میانگین جرم مولی هوای اطراف ما نزدیک به ۲۹ گرم بر مول می باشد. به همین دلیل، گاز هیدروژن کلرید از هوا سنگین تر است. وقتی این گاز در محیط آزاد می شود، به جای بالا رفتن، تمایل دارد به سمت پایین حرکت کند و در بخش های پایین تر فضا جمع شود.
این ویژگی از نظر ایمنی اهمیت زیادی دارد. اگر تهویه مناسب وجود نداشته باشد، گاز HCl می تواند در محیط باقی بماند و خطر ایجاد کند. به همین دلیل هنگام کار با این گاز، توجه به جریان هوا و خروج مناسب گاز بسیار ضروری است.
جرم مولکولی همچنین بر سرعت پخش شدن گازها تأثیر می گذارد. مولکول های سبک تر معمولاً سریع تر حرکت می کنند و زودتر در فضا پخش می شوند. برای نمونه، گازی مانند آمونیاک که جرم مولی کمتری دارد، نسبت به HCl با سرعت بیشتری منتشر می شود.
از طرف دیگر، وزن مولکولی HCl همراه با نیروهای بین مولکولی آن باعث شده نقطه جوش بسیار پایینی داشته باشد. این مولکول قطبی است، اما بین مولکول های آن پیوند هیدروژنی قوی شکل نمی گیرد. در نتیجه، هیدروژن کلرید در دمای حدود منفی ۸۵ درجه سانتیگراد به جوش می آید.
در مجموع، جرم مولکولی بالاتر HCl نسبت به بسیاری از گازهای رایج، دلیل رفتارهایی مانند چگالی بیشتر، حرکت کندتر و نحوه خاص پخش شدن آن در هوا است.




