فهرست عناوین
- مقدمه
- درک گشتاور دوقطبی
- چه چیزی یک مولکول را قطبی می کند؟
- الکترونگاتیوی و قطبیت پیوند
- ساختار مولکول HCl
- چرا مولکول HCl قطبی است؟
- کمّی سازی گشتاور دوقطبی HCl
- محاسبه گشتاور دوقطبی در مولکول ها
- واحدهای گشتاور دوقطبی (دبی)
- چگونه گشتاورهای دوقطبی اندازه گیری می شوند؟
- شکل مولکولی و قطبیت
- مقایسه گشتاور دوقطبی HCl با مولکول های دیگر
- گشتاور دوقطبی و خواص فیزیکی
- قطبیت و نیروهای بین مولکولی
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 04-10-1404
تاریخ بروزرسانی مقاله : 04-10-1404
تعداد کلمات : 3200
آدرس مقاله : لینک مقاله
لحظه دوقطبی مولکول اسید کلریدریک (قطبیت مولکولی)
مقدمه
اسید هیدروکلریک (HCl) یک مولکول دو اتمی ساده است که در نشان دادن قطبیت مولکولی نقش مهمی دارد. وقتی شیمی دانان درباره ی گشتاور دوقطبی مولکولی مانند HCl صحبت می کنند، منظورشان جدایی بارهای مثبت و منفی درون آن مولکول است. مولکول HCl بین دو اتم خود اختلاف الکترونگاتیوی قابل توجهی دارد که باعث توزیع نایکنواخت چگالی الکترونی می شود. در نتیجه، یک سر مولکول تا حدی مثبت می شود و سر دیگر آن تا حدی منفی. قطبیت مولکولی بسیاری از ویژگی های فیزیکی و شیمیایی مواد را، از جمله نقطه جوش، حلالیت و نحوه ی برهم کنش مولکول ها با یکدیگر، تحت تأثیر قرار می دهند.
همین ویژگی های قطبی و رفتار شیمیایی مشخص اسید هیدروکلریک سبب شده است که در کاربردهای صنعتی گسترده، موضوع خرید اسید کلریدریک کلران سمنان تانکر برای مصارف حجیم و فرآیندهای حساس شیمیایی اهمیت ویژه ای پیدا کند. در این بررسی جامع خواهیم دید گشتاور دوقطبی چیست، چرا مولکول HCl قطبی است و این که قطبیت مولکولی چگونه بر ویژگی ها و رفتارهای مختلف مواد اثر می گذارد.
درک گشتاور دوقطبی
گشتاور دوقطبی مفهومی ساده اما مهم در شیمی است که توضیح میدهد چرا بعضی مولکولها رفتار قطبی دارند. وقتی الکترونها در یک پیوند شیمیایی بهطور مساوی بین اتمها پخش نشوند، تعادل بار الکتریکی به هم میخورد. در چنین حالتی، یک سمت مولکول کمی بار مثبت و سمت دیگر کمی بار منفی پیدا میکند و همین تفاوت، پایه شکلگیری گشتاور دوقطبی است.
برای درک بهتر، میتوان این وضعیت را شبیه یک فلش در نظر گرفت؛ فلشی که از بخش مثبت مولکول شروع میشود و به سمت بخش منفی آن جهت دارد. هرچه اختلاف بار الکتریکی بیشتر باشد یا فاصله این دو ناحیه افزایش پیدا کند، شدت این ویژگی هم بالاتر میرود. دانشمندان برای بیان مقدار آن از واحدی به نام دبی استفاده میکنند تا بتوانند مولکولهای مختلف را با هم مقایسه کنند.
در مولکولهایی که چند پیوند قطبی دارند، اثر هر پیوند بهتنهایی بررسی نمیشود. در عوض، همه این اثرها با هم ترکیب میشوند و نتیجه نهایی، رفتار کلی مولکول را مشخص میکند. اگر این ترکیب باعث نابرابری بیشتر توزیع بار شود، مولکول قطبیتر خواهد بود.
از آنجا که گشتاور دوقطبی هم اندازه دارد و هم جهت، به آن کمیت برداری گفته میشود. برای نمونه، در مولکولی مانند HCl که تنها یک پیوند قطبی دارد، جهت این بردار دقیقاً در راستای همان پیوند است و از هیدروژن به سمت کلر در نظر گرفته میشود.
چه چیزی یک مولکول را قطبی می کند؟
اینکه یک مولکول قطبی باشد یا نه، در اصل به نحوه پخش شدن الکترونها در کل ساختار آن برمیگردد. وقتی بار الکتریکی بهطور یکنواخت توزیع نشود، دو سوی مولکول رفتار متفاوتی پیدا میکنند و همین تفاوت، پایه قطبی بودن را شکل میدهد.
در این میان دو عامل نقش اصلی دارند. عامل اول به خود پیوندها مربوط میشود. اگر دو اتمی که به هم متصل هستند توانایی یکسانی در جذب الکترون نداشته باشند، الکترونهای مشترک بیشتر به سمت یکی از آنها کشیده میشوند و پیوند حالت نامتقارن پیدا میکند. چنین پیوندی ذاتاً قطبی است.
عامل دوم به شکل کلی مولکول مربوط میشود. حتی اگر چند پیوند قطبی در یک مولکول وجود داشته باشد، باز هم ممکن است کل مولکول قطبی نباشد. دلیلش این است که در ساختارهای متقارن، اثر پیوندها میتواند همدیگر را خنثی کند. نمونه شناختهشده آن دیاکسید کربن است که با وجود داشتن پیوندهای قطبی، به دلیل آرایش خطی، در مجموع رفتار غیرقطبی دارد.
در مقابل، وقتی شکل مولکول متقارن نباشد، شرایط فرق میکند. آب مثال سادهای از این حالت است؛ پیوندهای آن قطبیاند و به دلیل فرم خمیده، اثرشان با هم جمع میشود. در مولکولهای ساده دو اتمی مثل HCl هم اگر همان یک پیوند قطبی باشد، کل مولکول قطبی خواهد بود. به طور خلاصه، قطبی بودن زمانی رخ میدهد که هم پیوندها قطبی باشند و هم چیدمان آنها اجازه خنثی شدن اثرات را ندهد.
الکترونگاتیوی و قطبیت پیوند
الکترونگاتیوی معیاری است که نشان می دهد یک اتم با چه نیرویی الکترون های پیوندی را به سمت خود جذب می کند. وقتی دو اتم درگیر در یک پیوند مقادیر الکترونگاتیوی متفاوتی داشته باشند، الکترون های پیوندی به طور مساوی بین آن ها به اشتراک گذاشته نمی شوند. اتمی که الکترونگاتیوی بالاتری دارد ابر الکترونی پیوند را بیشتر به خود می کشد و بار منفی جزئی (δ−) می گیرد، در حالی که اتم دیگر تا حدی مثبت (δ+) می شود.
این جدایی بار در طول پیوند همان چیزی است که قطبیت پیوند نام دارد. هرچه اختلاف الکترونگاتیوی بیشتر باشد, پیوند قطبی تر خواهد بود. نمونه ی کلاسیک این پدیده، اختلاف الکترونگاتیوی بین اتم های هیدروژن و کلر در اسید کلریدریک است که باعث می شود الکترون ها به طور نامتقارن به سمت اتم کلر کشیده شوند. برای مثال، کلر به مراتب از هیدروژن الکترونگاتیوتر است؛ بنابراین در پیوند H–Cl الکترون ها زمان بیشتری را پیرامون اتم کلر می گذرانند.
به این ترتیب یک پیوند کووالانسی قطبی شکل می گیرد که در آن اتم Cl بار δ− (منفی جزئی) و اتم H بار δ+ (مثبت جزئی) دارد. در مقابل اگر دو اتم یکسان با هم پیوند تشکیل دهند (مانند H–H یا Cl–Cl ، چون الکترونگاتیوی یکسانی دارند هیچ جدایی باری رخ نمی دهد و پیوند حاصله یک پیوند اشتراکی غیرقطبی خواهد بود. پس تفاوت در الکترونگاتیوی اتم ها علت اصلی قطبیت یک پیوند است و در نهایت در صورتی که شکل هندسی مولکول این قطبیت ها را خنثی نکند دلیل قطبیت کل مولکول نیز به شمار می رود.
ساختار مولکول HCl
مولکول اسید هیدروکلریک یا همان HCl ساختاری بسیار ساده دارد و از دو اتم تشکیل شده است؛ یک اتم هیدروژن و یک اتم کلر. این دو اتم تنها با یک پیوند به هم متصل هستند و به همین دلیل HCl را در گروه مولکول های دو اتمی قرار می دهند. چون فقط دو اتم در این ساختار وجود دارد، شکل مولکول به صورت خطی است و حالت پیچیده تری برای آن قابل تصور نیست.
فاصله بین اتم هیدروژن و کلر در این مولکول بسیار کم است و همین نزدیکی باعث می شود پیوند میان آن ها پایدار باشد. HCl در دسته ای از ترکیبات به نام هیدروژن هالیدها قرار می گیرد که ویژگی مشترک آن ها اتصال هیدروژن به یکی از عناصر خانواده هالوژن هاست. این ساختار ساده نقش مهمی در رفتار شیمیایی این ماده دارد.
نکته مهم در مورد HCl تفاوت قدرت جذب الکترون بین دو اتم آن است. اتم کلر تمایل بیشتری به الکترون دارد و همین موضوع باعث می شود پیوند بین این دو اتم حالت قطبی پیدا کند. در نتیجه، مولکول HCl دارای یک سر با بار نسبی مثبت و یک سر با بار نسبی منفی است.
حتی زمانی که این ماده در دماهای بسیار پایین به صورت جامد در کنار مولکول های دیگر قرار می گیرد، هر واحد HCl همچنان ویژگی قطبی خود را حفظ می کند. در واقع، بسیاری از خواص اسید هیدروکلریک به همین ساختار ساده و همین پیوند قطبی وابسته است.
چرا مولکول HCl قطبی است؟
در مولکول HCl، اتم کلر توانایی بیشتری در جذب الکترون دارد و همین تفاوت باعث می شود پیوند میان کلر و هیدروژن حالت نامتقارن پیدا کند. الکترون هایی که بین این دو اتم مشترک هستند، بیشتر به سمت کلر کشیده می شوند و اطراف هیدروژن کمتر باقی می مانند. به همین دلیل، هیدروژن کمی بار مثبت و کلر اندکی بار منفی می گیرد.
این جابه جایی الکترون ها باعث می شود مولکول HCl دو سر متفاوت داشته باشد. یک سر آن رفتاری شبیه به بخش مثبت دارد و سر دیگر به صورت منفی عمل می کند. چون این مولکول فقط از همین یک پیوند تشکیل شده است، هیچ عامل دیگری وجود ندارد که این تفاوت بار را از بین ببرد یا متعادل کند.
برای نمایش این حالت، معمولاً HCl را به شکلی نشان می دهند که علامت مثبت کنار هیدروژن و علامت منفی کنار کلر قرار دارد. این موضوع نشان می دهد که بار الکتریکی در مولکول به طور یکنواخت پخش نشده است. چنین ساختاری باعث می شود HCl نسبت به بسیاری از مولکول های ساده، خاصیت قطبی قوی تری داشته باشد.
اگر این حالت را با گاز هیدروژن مقایسه کنیم، تفاوت به خوبی دیده می شود. در H2 هر دو اتم یکسان هستند و الکترون ها به طور مساوی تقسیم می شوند، بنابراین هیچ سر مثبت یا منفی مشخصی وجود ندارد. اما در HCl این جدایی بار کاملاً محسوس است و رفتار مولکول را تحت تاثیر قرار می دهد.
کمّی سازی گشتاور دوقطبی HCl
گشتاور دوقطبی مولکول HCl عددی در حدود ۱٫۰۳ دبی است که نشان می دهد این مولکول تا چه اندازه خاصیت قطبی دارد. این عدد در واقع بیان می کند که توزیع بار الکتریکی در HCl یکنواخت نیست و الکترون ها بیشتر به یک سمت مولکول متمایل شده اند. چنین مقداری برای یک مولکول دو اتمی نسبتاً قابل توجه محسوب می شود.
با دانستن طول پیوند میان هیدروژن و کلر که حدود ۱٫۲۷ آنگستروم است، می توان مقدار بار جزئی هر اتم را به صورت تقریبی محاسبه کرد. نتیجه این محاسبه نشان می دهد که بار مؤثر روی هر اتم چیزی نزدیک به ۰٫۱۸ بار الکترون است. یعنی هیدروژن کمی بار مثبت و کلر کمی بار منفی دارد، نه بار کامل یونی.
اگر پیوند H–Cl کاملاً یونی بود و بارها به طور کامل جدا می شدند، مقدار گشتاور دوقطبی باید چند برابر بزرگ تر می بود. اما عدد اندازه گیری شده نشان می دهد این پیوند فقط بخشی از ویژگی های یونی را دارد و بیشتر ماهیت کووالانسی خود را حفظ کرده است.
همین قطبیت نسبی باعث می شود HCl رفتار فیزیکی متفاوتی نسبت به مولکول های کاملاً غیرقطبی داشته باشد. برای مثال، با وجود جرم مولکولی کم، نقطه جوش آن بالاتر از انتظار است و به راحتی در آب حل می شود. این ویژگی ها مستقیماً به توزیع نابرابر بار در ساختار مولکول مربوط هستند.
محاسبه گشتاور دوقطبی در مولکول ها
برای به دست آوردن گشتاور دوقطبی یک مولکول، باید هم میزان جدایی بار الکتریکی را در نظر گرفت و هم فاصله ای که این بارها از یکدیگر دارند. در مولکول های ساده ای مثل HCl، این کار چندان پیچیده نیست و با یک محاسبه مستقیم انجام می شود. کافی است مقدار بار جزئی هر اتم در طول پیوند مشخص باشد.
در چنین حالتی، مقدار بار در فاصله بین دو اتم ضرب می شود تا عددی به دست آید که نشان دهنده شدت دوقطبی بودن مولکول است. این محاسبه ابتدا با واحدهای علمی استاندارد انجام می شود و در نهایت می توان نتیجه را به واحدی رایج تر به نام دبی تبدیل کرد. برای HCl، استفاده از مقادیر شناخته شده نشان می دهد که نتیجه با مقدار اندازه گیری شده تطابق خوبی دارد.
اما همه مولکول ها به این سادگی نیستند. در ترکیباتی که چند اتم و چند پیوند دارند، هر پیوند قطبی سهم جداگانه ای در رفتار کلی مولکول دارد. جهت قرار گرفتن این پیوندها نسبت به هم اهمیت زیادی پیدا می کند، زیرا ممکن است اثر یکدیگر را تقویت یا تضعیف کنند.
به همین دلیل، برای مولکول های بزرگ تر معمولاً از روش های آزمایشگاهی یا نرم افزارهای تخصصی استفاده می شود. این ابزارها کمک می کنند تا تاثیر شکل فضایی و زاویه پیوندها به شکل دقیق تری بررسی شود و نتیجه قابل اعتمادتری به دست آید.
واحدهای گشتاور دوقطبی (دبی)
برای بیان میزان گشتاور دوقطبی مولکول ها، معمولاً از واحدی به نام دبی استفاده می شود که با حرف D نشان داده می شود. این واحد به شکلی انتخاب شده که اندازه قطبیت مولکول ها را با عددهایی قابل فهم نشان دهد، به طوری که اغلب ترکیبات رایج در بازه چند دبی قرار می گیرند. همین موضوع باعث شده دبی در شیمی کاربرد زیادی داشته باشد.
در دستگاه بین المللی واحدها، گشتاور دوقطبی با کولن-متر بیان می شود، اما این واحد برای مقیاس مولکولی چندان مناسب نیست، چون عددهای بسیار کوچک و طولانی ایجاد می کند. هر دبی مقدار بسیار ناچیزی دارد و نشان دهنده جدا شدن بار الکتریکی در فاصله ای فوق العاده کوچک است؛ فاصله ای که تنها در ابعاد اتمی معنا پیدا می کند.
به عنوان نمونه، گشتاور دوقطبی HCl که کمی بیش از یک دبی است، در واحدهای علمی استاندارد به عددی در حد ۱۰ به توان منفی سی می رسد. استفاده از دبی کمک می کند تا این مقادیر بدون سردرگمی و به صورت ملموس تر بیان شوند.
نام این واحد از دانشمندی گرفته شده که نقش مهمی در شناخت رفتار الکتریکی مولکول ها داشته است. وقتی گفته می شود یک مولکول صفر دبی یا چند دبی گشتاور دارد، درک ساده تری از میزان قطبیت آن به دست می آید.
چگونه گشتاورهای دوقطبی اندازه گیری می شوند؟
برای اندازه گیری گشتاور دوقطبی مولکول هایی مثل HCl، روش های آزمایشگاهی مختلفی وجود دارد. یکی از ساده ترین راه ها بررسی واکنش مولکول ها در برابر یک میدان الکتریکی خارجی است. وقتی گاز HCl در چنین میدانی قرار می گیرد، مولکول های آن تمایل دارند طوری بچرخند که سر مثبت و منفی شان با جهت میدان هماهنگ شود. این رفتار نشانه قطبی بودن آن هاست.
این هم جهت شدن باعث ایجاد تغییراتی در ویژگی های الکتریکی محیط می شود که قابل اندازه گیری است. با بررسی این تغییرات، می توان مقدار گشتاور دوقطبی را به دست آورد. هرچه این اثر قوی تر باشد، نشان دهنده قطبیت بیشتر مولکول است.
روش دیگری که کاربرد زیادی دارد، اندازه گیری ثابت دی الکتریک مواد است. حضور مولکول های قطبی باعث می شود ماده بتواند بار الکتریکی بیشتری در خود نگه دارد. این افزایش ظرفیت مستقیماً با شدت دوقطبی بودن مولکول ها ارتباط دارد.
علاوه بر این، از روش های طیف سنجی نیز استفاده می شود. در طیف سنجی ریزموج، تنها مولکول هایی که دوقطبی دائمی دارند می توانند امواج خاصی را جذب کنند. بررسی این جذب اطلاعات دقیقی درباره مقدار گشتاور دوقطبی در اختیار پژوهشگران قرار می دهد.
شکل مولکولی و قطبیت
شکل کلی یک مولکول نقش مهمی در این دارد که قطبی باشد یا نه. حتی اگر پیوندهای داخل یک مولکول قطبی باشند، نحوه قرار گرفتن آن ها در فضا مشخص می کند که در نهایت بارهای مثبت و منفی همدیگر را خنثی می کنند یا یک اثر کلی باقی می ماند. به بیان ساده، فقط وجود پیوند قطبی کافی نیست و آرایش فضایی هم اهمیت دارد.
در مولکول هایی با ساختار کاملاً متقارن، معمولاً اثر پیوندهای قطبی از بین می رود. برای نمونه، دی اکسید کربن ساختاری خطی دارد و دو پیوند آن در جهت مخالف هم قرار گرفته اند. به همین دلیل، هرچند هر پیوند به تنهایی قطبی است، ولی کل مولکول رفتاری خنثی دارد و غیرقطبی محسوب می شود.
در مقابل، آب ساختاری خمیده دارد و پیوندهای آن در یک راستا نیستند. همین انحنا باعث می شود اثر پیوندها روی هم جمع شود و مولکول دارای قطبیت قابل توجهی باشد. این ویژگی بسیاری از رفتارهای خاص آب را توضیح می دهد.
مولکول متان هم مثال دیگری از نقش تقارن است. چهار پیوند یکسان آن به شکلی منظم قرار گرفته اند و اثر همدیگر را از بین می برند. اما با تغییر یکی از اتم ها، این نظم به هم می خورد و مولکول می تواند قطبی شود.
مقایسه گشتاور دوقطبی HCl با مولکول های دیگر
برای این که مقدار گشتاور دوقطبی HCl بهتر قابل درک باشد، مقایسه آن با چند مولکول شناخته شده کمک زیادی می کند. وقتی HCl را در کنار دیگر هیدروژن هالیدها قرار می دهیم، تفاوت ها به خوبی دیده می شود. برای مثال، هیدروژن فلوئورید قطبیت بیشتری دارد، اما هرچه به سمت هیدروژن برمید و هیدروژن یدید می رویم، این خاصیت ضعیف تر می شود.
دلیل این روند به دو عامل اصلی برمی گردد: اختلاف الکترونگاتیوی بین اتم ها و فاصله آن ها از یکدیگر. در مولکولی مثل HF، اتم فلوئور قدرت جذب الکترون بسیار بالایی دارد و همین موضوع باعث ایجاد گشتاور دوقطبی بزرگ می شود. در مقابل، در HI این اختلاف کمتر است و طول پیوند هم بیشتر می شود، بنابراین قطبیت کاهش پیدا می کند.
آب نیز نمونه جالبی برای مقایسه است. این مولکول به دلیل شکل خمیده و وجود دو پیوند قطبی، گشتاور دوقطبی قابل توجهی دارد و رفتار آن با بسیاری از مواد دیگر متفاوت است. همین ویژگی باعث شده آب نقش مهمی در حل شدن مواد مختلف داشته باشد.
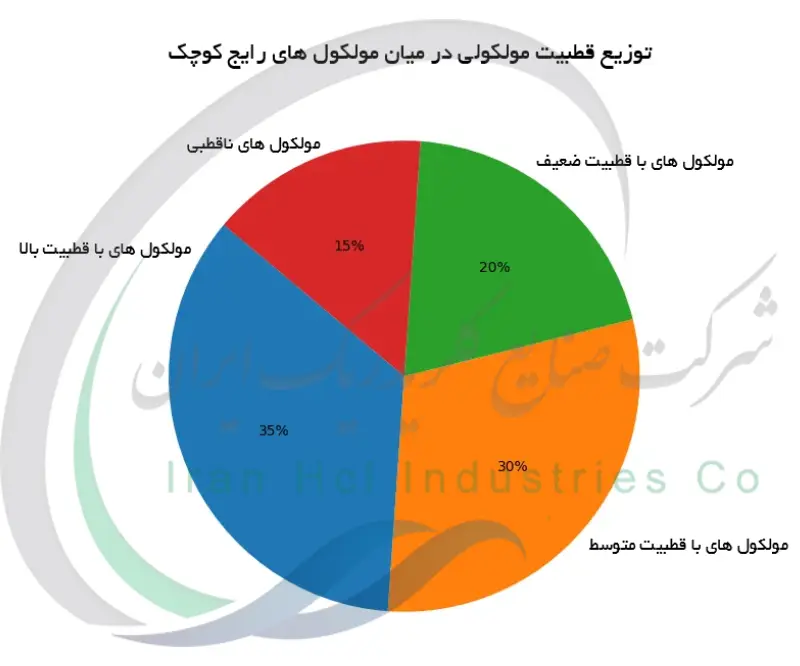
در سوی دیگر، مولکول هایی مثل هیدروژن، متان یا دی اکسید کربن ساختار متقارن دارند. در این ترکیبات، اگرچه ممکن است پیوندها قطبی باشند، اما اثر آن ها یکدیگر را خنثی می کند و در نهایت هیچ قطبیت کلی دیده نمی شود. این مقایسه ها نشان می دهد جایگاه HCl از نظر قطبیت در میان مولکول های رایج کجاست.
| مولکول | اختلاف الکترونگاتیوی | طول پیوند (آنگستروم) | گشتاور دوقطبی (D) | قطبیت |
|---|---|---|---|---|
| H2 | ۰٫۰ | ۰٫۷۴ | ۰٫۰ | ناقطبی |
| CO2 | ۰٫۹ | ۱٫۱۶ | ۰٫۰ | ناقطبی |
| HF | ۱٫۹ | ۰٫۹۲ | ۱٫۸۲ | قطبی |
| HCl | ۱٫۰ | ۱٫۲۷ | ۱٫۰۳ | قطبی |
| HBr | ۰٫۷ | ۱٫۴۱ | ۰٫۸ | قطبی |
| HI | ۰٫۴ | ۱٫۶۱ | ۰٫۴ | قطبی |
| H2O | ۱٫۲ | ۰٫۹۶ | ۱٫۸۵ | قطبی |
| CH4 | ۰٫۳ | ۱٫۰۹ | ۰٫۰ | ناقطبی |
گشتاور دوقطبی و خواص فیزیکی
میزان گشتاور دوقطبی هر مولکول تأثیر مستقیمی بر ویژگی های فیزیکی آن دارد. وقتی یک مولکول قطبی باشد، بخش مثبت و منفی آن می توانند یکدیگر را جذب کنند. این کشش میان مولکول ها باعث می شود جدا کردن آن ها از هم دشوارتر شود و برای تبدیل ماده به بخار یا ذوب شدن، انرژی بیشتری لازم باشد.
به همین دلیل، ترکیبات قطبی معمولاً نقطه جوش بالاتری نسبت به مواد غیرقطبی با جرم مشابه دارند. برای نمونه، HCl در دمایی بالاتر از گاز فلوئور به جوش می رسد، با اینکه جرم مولکولی آن ها نزدیک به هم است. علت این تفاوت، نیروی جاذبه قوی تری است که میان مولکول های HCl وجود دارد.
آب نمونه شناخته شده ای از یک مایع قطبی است که به دلیل وجود برهمکنش های قوی بین مولکول هایش، دمای جوش بالایی دارد. این نیروهای بین مولکولی باعث می شوند آب در شرایط معمول به صورت مایع باقی بماند.
قطبیت بر میزان حل شدن مواد نیز اثر می گذارد. HCl به خوبی در آب حل می شود، چون هر دو قطبی هستند و به هم جذب می شوند. در مقابل، گازهایی مثل اکسیژن یا نیتروژن که ساختار خنثی دارند، در آب به سختی حل می شوند. به طور کلی، مواد با ویژگی مشابه راحت تر با هم مخلوط می شوند.
قطبیت و نیروهای بین مولکولی
نیروهایی که بین مولکول ها عمل می کنند، ارتباط مستقیمی با قطبی بودن آن ها دارند. وقتی یک مولکول دارای بخش مثبت و منفی باشد، این قسمت ها می توانند با بخش های مخالف در مولکول های اطراف ارتباط برقرار کنند. همین کشش الکتریکی باعث می شود مولکول ها به یکدیگر نزدیک تر بمانند و راحت از هم جدا نشوند.
در مولکول های قطبی، این جذب به صورت منظم تری رخ می دهد. بخش مثبت یک مولکول به سمت بخش منفی مولکول کناری کشیده می شود و نوعی نظم موقتی ایجاد می کند. در HCl مایع، اتم هیدروژن یک مولکول معمولاً در نزدیکی اتم کلر مولکول دیگر قرار می گیرد. این آرایش باعث می شود دمای جوش و ذوب آن نسبت به گازهای خنثی هم جرم بالاتر باشد.
نوع قوی تری از این جاذبه ها با نام پیوند هیدروژنی شناخته می شود. این حالت زمانی رخ می دهد که هیدروژن به عناصری مثل اکسیژن یا فلوئور متصل باشد. آب نمونه بارز این پدیده است و به همین دلیل رفتار حرارتی خاصی دارد.
HCl با وجود قطبی بودن، چنین پیوند محکمی ایجاد نمی کند، اما همچنان از جاذبه های دوقطبی معمول بهره می برد. علاوه بر این، مولکول های قطبی می توانند به طور موقت در مولکول های خنثی هم اثر بگذارند و آن ها را جذب کنند. در مجموع، قطبیت باعث شکل گیری نیروهایی می شود که از جاذبه های ضعیف مواد غیرقطبی قوی تر هستند.




