فهرست عناوین
- مقدمه
- درک قطبیت پیوند
- الکترونگاتیویته و قطبیت پیوند
- پیوند کووالانسی قطبی و غیرقطبی
- گشتاور دوقطبی: سنجش کمی قطبیت پیوند
- اسید هیدروکلریک (HCl): پیوندی با قطبیت متوسط
- قطبیت HCl در مقایسه با HF اسید هیدروفلوئوریک
- مقایسه HCl با HBr اسید هیدروبرویک
- هیدریودیک اسید (HI) – کمترین قطبیت در هالیدها
- داده های مقایسه ای قطبیت پیوند برای HCl و مولکول های مشابه
- مقایسه HCl و H₂O : تفاوت در قطبیت
- قطبیت و نیروهای بین مولکولی در HCl و مولکول های مشابه
- قطبیت پیوند در برابر قدرت اسیدی: HF در مقابل HCl
نوشته شده توسط شرکت صنایع کلریدریک ایران
منتشر شده توسط شرکت صنایع کلریدریک ایران
تاریخ انتشار مقاله : 27-09-1404
تاریخ بروزرسانی مقاله : 27-09-1404
تعداد کلمات : 3300
آدرس مقاله : لینک مقاله
مقایسه قطبیت پیوند اسید کلریدریک با مولکول های مشابه

مقدمه
اسید هیدروکلریک (HCl) یک نمونه شناخته شده از یک مولکول کووالانسی قطبی است. پیوند بین هیدروژن و کلر در این ترکیب به دلیل تفاوت الکترونگاتیویته بین دو اتم، قطبی است. اما قطبیت پیوند HCl در مقایسه با مولکول های مشابه چگونه است؟ درک قطبیت پیوند برای توضیح بسیاری از ویژگی های شیمیایی و فیزیکی مواد ضروری است. در این بررسی جامع، ابتدا مفهوم قطبیت پیوند و اینکه تفاوت الکترونگاتیویته چگونه پیوندهای قطبی را ایجاد می کند بحث می شود، سپس قطبیت پیوند HCl با مولکول های مرتبط مانند هیدروفلوئوریک اسید (HF)، هیدروبرویک اسید (HBr)، هیدریودیک اسید (HI)، آب (H₂O) و موارد دیگر مقایسه خواهد شد.
با بررسی این مقایسه ها، روندهای قطبیت مشاهده و تأثیر آن ها بر ویژگی هایی مانند گشتاور دوقطبی، نقطه جوش، قدرت اسیدی و حلالیت مشخص می شود. همین ویژگی های شیمیایی و فیزیکی اسید هیدروکلریک موجب شده است که در کاربردهای صنعتی گسترده، به ویژه در صنایع فلزی، تصفیه آب و فرآیندهای شیمیایی در مقیاس بالا، موضوع خرید اسید کلریدریک کلران سمنان مخزن IBC به عنوان یک گزینه عملی و ایمن برای حمل و نگهداری این ماده مطرح باشد.
درک قطبیت پیوند
قطبیت پیوند یک مفهوم اساسی در شیمی است که به توزیع نابرابر الکترون ها بین دو اتم در یک پیوند کووالانسی اشاره دارد. زمانی که یکی از اتم ها به طور قابل توجهی الکترونگاتیوتر از دیگری باشد، الکترون های مشترک را بیشتر به سمت خود می کشد و در نتیجه آن اتم دارای بار جزئی منفی و اتم با الکترونگاتیویته کمتر دارای بار جزئی مثبت می شود. این جدایش بار درون پیوند یک دوقطبی الکتریکی ایجاد می کند.
برای مثال، در مولکول هیدروژن کلرید (HCl)، اتم کلر الکترونگاتیوتر از اتم هیدروژن است؛ بنابراین الکترون های پیوندی زمان بیشتری را نزدیک اتم کلر می گذرانند. در نتیجه پیوند H–Cl قطبی است؛ سر هیدروژن حامل بار جزئی مثبت δ+ و سر کلر حامل بار جزئی منفی δ–است. در چنین مولکولی، بررسی هم زمان قطبیت پیوند و طول پیوند در اسید کلریدریک و نحوه اندازه گیری آن نقش مهمی در درک دقیق ساختار مولکولی و رفتار ارتعاشی HCl دارد.
در مقابل پیوند بین اتم های یکسان مانند H–H در H₂ یا Cl–Cl در Cl₂ غیرقطبی است زیرا الکترون ها به طور مساوی به اشتراک گذاشته می شوند و هیچ بار جزئی تشکیل نمی شود. قطبیت پیوند یک طیف پیوسته است که از پیوندهای کاملاً غیرقطبی (مشارکت برابر الکترون ها) شروع شده و تا پیوندهای بسیار قطبی یا حتی یونی که در آن ها الکترون ها تقریباً به طور کامل منتقل می شوند ادامه دارد. پیوندهای قطبی زمینه ساز رفتار مولکول های قطبی هستند و بر نحوه برهم کنش آن ها با میدان های الکتریکی و سایر مولکول ها از طریق نیروهای بین مولکولی تأثیر می گذارند.
الکترونگاتیویته و قطبیت پیوند
الکترونگاتیویته به زبان ساده نشان می دهد هر اتم تا چه اندازه دوست دارد الکترون ها را به سمت خود بکشد. این ویژگی نقش اصلی را در قطبی یا غیرقطبی بودن پیوندها بازی می کند. وقتی دو اتم با تمایل های متفاوت به الکترون ها کنار هم قرار می گیرند، الکترون های پیوندی به طور مساوی تقسیم نمی شوند و همین نابرابری باعث ایجاد قطبیت می شود.
برای مقایسه این تمایل، به هر عنصر عددی نسبت داده شده که معمولاً بر پایه مقیاس پاولینگ بیان می شود. در این مقیاس، فلوئور بالاترین مقدار را دارد و بیش از همه الکترون ها را جذب می کند. هیدروژن عددی نزدیک به ۲.۲ دارد، در حالی که این مقدار برای کلر حدود ۳.۲ است. همین اختلاف تقریباً یک واحدی میان هیدروژن و کلر باعث می شود پیوند H–Cl حالت قطبی قابل توجهی داشته باشد.
به طور تجربی، اگر فاصله الکترونگاتیویته دو اتم بیشتر از حدود نیم واحد باشد، پیوند را کووالانسی قطبی در نظر می گیرند. برای نمونه، در HF این اختلاف بسیار زیاد است و پیوندی به شدت قطبی ایجاد می شود. در مقابل، HCl با اختلاف کمتر، قطبیتی متوسط دارد.
اما وقتی دو اتم الکترونگاتیویته یکسانی دارند، مثل H₂ یا Cl₂، الکترون ها به طور برابر تقسیم می شوند و پیوند غیرقطبی شکل می گیرد. بنابراین تنها با مقایسه این اعداد می توان تا حد زیادی نوع پیوند و نحوه توزیع الکترون ها را پیش بینی کرد.
پیوند کووالانسی قطبی و غیرقطبی
پیوندهای کووالانسی را می توان بر اساس نحوه تقسیم الکترون ها به دو گروه اصلی تقسیم کرد: قطبی و غیرقطبی. تفاوت این دو نوع پیوند به این برمی گردد که الکترون ها میان اتم ها به صورت برابر یا نابرابر پخش شوند. وقتی تقسیم الکترون ها نامساوی باشد، روی اتم ها بارهای جزئی شکل می گیرد و پیوند حالت قطبی پیدا می کند.
در پیوندهای غیرقطبی، شرایط متفاوت است. در این حالت، هر دو اتم قدرت تقریباً یکسانی در جذب الکترون دارند و الکترون ها بدون ترجیح خاصی میان آن ها قرار می گیرند. به همین دلیل بار جزئی قابل توجهی ایجاد نمی شود و پیوند خنثی باقی می ماند.
پیوند HCl نمونه روشنی از یک پیوند قطبی است. در این مولکول، کلر الکترون ها را قوی تر از هیدروژن جذب می کند و همین موضوع باعث نابرابری در توزیع الکترون می شود. در مقابل، مولکولی مثل H₂ غیرقطبی است، چون هر دو اتم کاملاً مشابه اند.
بسیاری از پیوندهای C–H نیز عملاً غیرقطبی به حساب می آیند، زیرا اختلاف تمایل الکترونی در آن ها بسیار کم است. مولکول های غیرقطبی مانند Cl₂ یا متان گشتاور دوقطبی ندارند، در حالی که مولکول های قطبی مثل HCl یا آب دارای دوقطبی مشخص هستند. البته مرز قطعی میان این دو وجود ندارد و بیشتر یک طیف تدریجی دیده می شود.
گشتاور دوقطبی: سنجش کمی قطبیت پیوند
اگرچه اختلاف الکترونگاتیویته به ما می گوید یک پیوند تا چه اندازه تمایل به قطبی شدن دارد، اما برای سنجش دقیق این موضوع از کمیتی به نام گشتاور دوقطبی استفاده می شود. گشتاور دوقطبی نشان می دهد بارهای مثبت و منفی در یک پیوند یا مولکول تا چه حد از هم جدا شده اند. هرچه این جدایی بیشتر باشد، قطبیت نیز بالاتر خواهد بود.
این کمیت از حاصل ضرب مقدار بارهای جزئی در فاصله میان آن ها به دست می آید و معمولاً با واحد دبی بیان می شود. عدد بزرگ تر در این مقیاس به معنای قطبیت قوی تر است. در مولکول های ساده دو اتمی، مانند HCl، گشتاور دوقطبی پیوند همان گشتاور دوقطبی کل مولکول محسوب می شود. مقدار این کمیت برای HCl حدود ۱.۰۸ دبی است که نشان دهنده یک قطبیت متوسط می باشد.
برای مقایسه، در مولکول HF که پیوند آن قطبی تر است، گشتاور دوقطبی به حدود ۱.۸ دبی می رسد. در مقابل، مولکول هایی مانند H₂ یا O₂ کاملاً غیرقطبی اند و گشتاور دوقطبی آن ها صفر است.
گشتاور دوقطبی تنها به اختلاف الکترونگاتیویته وابسته نیست، بلکه طول پیوند نیز در آن نقش دارد. در مولکول های بزرگ تر با چند پیوند، شکل فضایی مولکول اهمیت پیدا می کند، زیرا دوقطبی های پیوندی می توانند همدیگر را تقویت یا خنثی کنند. به همین دلیل، گشتاور دوقطبی یک شاخص عملی و قابل اندازه گیری برای تشخیص قطبیت پیوند و مولکول به شمار می رود.
اسید هیدروکلریک (HCl): پیوندی با قطبیت متوسط
در مولکول اسید هیدروکلریک، اتم های هیدروژن و کلر با یک پیوند کووالانسی به هم متصل شده اند که از نظر قطبیت در حد میانه قرار دارد. تفاوت تمایل این دو اتم به جذب الکترون ها قابل توجه است؛ هیدروژن عددی نزدیک به ۲.۲ و کلر عددی حدود ۳.۲ در مقیاس پاولینگ دارد. همین اختلاف باعث می شود الکترون های پیوندی بیشتر به سمت کلر کشیده شوند.
در نتیجه این توزیع نابرابر، هیدروژن دارای بار جزئی مثبت و کلر دارای بار جزئی منفی می شود. این جدایی بارها به صورت عددی با گشتاور دوقطبی توصیف می گردد که برای HCl حدود ۱.۰۸ دبی اندازه گیری شده است. چنین مقداری نشان می دهد پیوند H–Cl قطبی است، اما شدت آن به اندازه پیوندی مانند H–F نیست که قطبیت بسیار بالاتری دارد.
در فاز گازی، هر مولکول HCl این دوقطبی دائمی را حفظ می کند و به همین دلیل میان مولکول ها نیروهای جاذبه دوقطبی–دوقطبی شکل می گیرد، هرچند این نیروها آن قدر قوی نیستند که پیوند هیدروژنی ایجاد کنند.
وقتی HCl وارد آب می شود، همین قطبیت باعث می گردد پیوند به راحتی شکسته شود و یون های H⁺ و Cl⁻ تشکیل شوند. این ویژگی توضیح می دهد چرا اسید هیدروکلریک در آب به خوبی حل می شود و در محلول رفتاری شبیه یک اسید قوی از خود نشان می دهد. در مجموع، پیوند H–Cl نمونه روشنی از یک پیوند کووالانسی قطبی با بارهای جزئی مشخص است، بدون آن که ماهیت کاملاً یونی داشته باشد.
قطبیت HCl در مقایسه با HF اسید هیدروفلوئوریک
اسید هیدروفلوئوریک یا HF معمولاً به عنوان یکی از نمونه های شاخص پیوند کووالانسی بسیار قطبی معرفی می شود و مقایسه آن با HCl دید خوبی از تفاوت ها به دست می دهد. در مولکول HF، اتم فلوئور تمایل بسیار زیادی به جذب الکترون دارد و عدد الکترونگاتیویته آن نزدیک به ۴ است، در حالی که این مقدار برای هیدروژن حدود ۲.۲ می باشد. همین اختلاف بزرگ باعث می شود پیوند H–F به شدت نامتعادل و قطبی شود.
شدت این نابرابری در گشتاور دوقطبی HF به خوبی دیده می شود. مقدار این کمیت برای HF حدود ۱.۸۲ دبی است که به شکل محسوسی از مقدار ثبت شده برای HCl بیشتر است. این موضوع نشان می دهد بارهای مثبت و منفی در HF فاصله و تمرکز بیشتری دارند و دوقطبی قوی تری شکل می گیرد.
یکی از پیامدهای مهم این قطبیت بالا، توانایی HF در ایجاد پیوند هیدروژنی بین مولکول هاست. این نوع جاذبه بین مولکولی بسیار قوی تر از نیروهای معمول دوقطبی است و باعث می شود HF با وجود جرم کم، نقطه جوش بالاتری داشته باشد.
در مقابل، HCl فاقد چنین برهم کنشی است و تنها نیروهای ضعیف تری میان مولکول های آن وجود دارد، به همین دلیل نقطه جوش بسیار پایینی دارد. نکته جالب اینجاست که با وجود قطبی تر بودن پیوند HF، در آب این HCl است که رفتار یک اسید قوی تر را نشان می دهد. این مقایسه نشان می دهد قطبیت پیوند تنها یکی از عوامل تعیین کننده رفتار شیمیایی مواد است.
مقایسه HCl با HBr اسید هیدروبرویک
اسید هیدروبرویک یا HBr نمونه ای است که در آن شدت قطبیت پیوند از HCl کمتر است. دلیل اصلی این تفاوت به ویژگی اتم برم برمی گردد. برم نسبت به کلر تمایل ضعیف تری برای جذب الکترون دارد و به همین خاطر اختلاف الکترونگاتیویته میان هیدروژن و برم کوچکتر می شود. این اختلاف کمتر باعث می گردد الکترون های پیوندی به اندازه HCl جابه جا نشوند.
در نتیجه، پیوند H–Br همچنان قطبی است، اما شدت این قطبیت پایین تر از پیوند H–Cl می باشد. این موضوع به صورت عددی نیز دیده می شود، زیرا گشتاور دوقطبی HBr حدود ۰.۸۲ دبی است که مقدار کمتری نسبت به HCl دارد. بنابراین بارهای جزئی مثبت و منفی در این مولکول ضعیف تر و پخش تر هستند.
به علت همین قطبیت کمتر، نیروهای جاذبه بین مولکول های HBr نیز کمی ضعیف تر عمل می کنند. با این حال، هیدروژن برومید در دمای معمولی به شکل گاز است و به راحتی در آب حل می شود. در محیط آبی، این ترکیب مانند HCl رفتار اسیدی قوی از خود نشان می دهد.
نکته مهم این است که پیوند H–Br هم طولانی تر و هم قطبی تر از حد متوسط نیست، به همین دلیل نسبتاً آسان شکسته می شود. این روند نشان می دهد با کاهش اختلاف الکترونگاتیویته، قطبیت پیوند نیز کاهش پیدا می کند.
هیدریودیک اسید (HI) – کمترین قطبیت در هالیدها
اسید هیدریودیک یا HI در میان هیدروژن هالیدهای شناخته شده، کمترین میزان قطبیت پیوند را دارد. علت اصلی این موضوع به شباهت زیاد تمایل الکترونی ید و هیدروژن برمی گردد. عدد الکترونگاتیویته ید حدود ۲.۶ است و فاصله کمی با مقدار ۲.۲ هیدروژن دارد، به همین دلیل اختلاف میان آن ها چندان چشمگیر نیست و پیوند H–I تنها اندکی حالت قطبی پیدا می کند.
این قطبیت ضعیف را می توان در مقدار گشتاور دوقطبی HI مشاهده کرد که حدود ۰.۴۴ دبی است. این عدد در مقایسه با HCl و حتی HBr بسیار پایین تر بوده و نشان می دهد جدایی بار در این مولکول محدود است. در نتیجه، بارهای جزئی مثبت و منفی روی اتم ها چندان برجسته نیستند و الکترون ها تقریباً به طور یکنواخت میان دو اتم تقسیم شده اند.
از سوی دیگر، پیوند H–I طولانی ترین پیوند در این خانواده به شمار می رود، زیرا اتم ید اندازه بزرگی دارد. هرچند پیوند بلندتر می تواند در شرایطی به افزایش دوقطبی کمک کند، اما در HI کم بودن اختلاف بار اثر غالب را دارد.
با وجود این قطبیت اندک، هیدروژن یدید در آب رفتاری کاملاً اسیدی از خود نشان می دهد. پیوند ضعیف H–I به آسانی شکسته می شود و همین ویژگی باعث می شود HI در محیط آبی قوی ترین اسید هیدروهالیک باشد. این روند به خوبی نشان می دهد کاهش اختلاف الکترونگاتیویته به کاهش تدریجی قطبیت پیوند منجر می شود.
داده های مقایسه ای قطبیت پیوند برای HCl و مولکول های مشابه
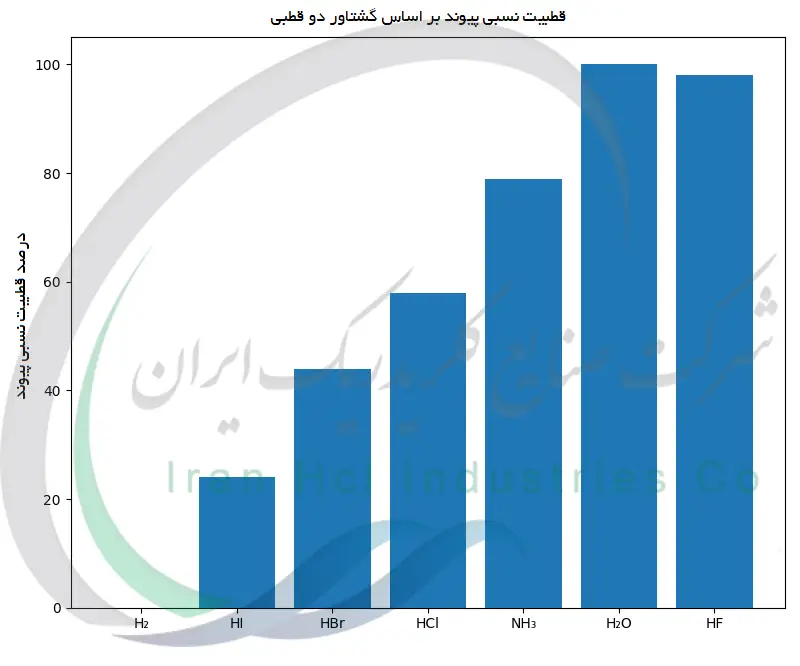
برای درک بهتر تفاوت قطبیت پیوندها، جدول زیر مجموعه ای از اطلاعات مهم را کنار هم قرار می دهد تا مقایسه ها به شکل روشن تری دیده شوند. در این جدول، هیدروژن هالیدهایی مانند HF، HCl، HBr و HI به همراه چند مولکول ساده دیگر آورده شده اند تا روند تغییر قطبیت به خوبی مشخص شود.
در هر ردیف، طول پیوند، اختلاف الکترونگاتیویته میان اتم های درگیر و مقدار گشتاور دوقطبی ذکر شده است. این داده ها کمک می کنند بفهمیم چرا برخی پیوندها بسیار قطبی هستند و برخی دیگر تقریباً خنثی به نظر می رسند. برای نمونه، HF بیشترین اختلاف الکترونگاتیویته و بالاترین گشتاور دوقطبی را دارد که نشان دهنده یک پیوند به شدت قطبی است.
با حرکت از فلوئور به سمت ید، یعنی از HF تا HI، کاهش تدریجی اختلاف الکترونگاتیویته دیده می شود و همزمان مقدار دوقطبی نیز کمتر می گردد. در این میان، H₂ به عنوان نمونه ای از یک پیوند کاملاً غیرقطبی معرفی شده، چون دو اتم یکسان دارد و هیچ جدایی باری شکل نمی گیرد.
همچنین مولکول هایی مثل آب و آمونیاک در جدول قرار داده شده اند تا نشان داده شود چگونه پیوندهای قطبی متعدد و شکل فضایی مولکول می توانند یک دوقطبی کلی قابل توجه ایجاد کنند. این مقایسه ها به خوبی نقش الکترونگاتیویته را در شکل گیری قطبیت پیوند نشان می دهند.
| مولکول | طول پیوند (Å) | اختلاف الکترونگاتیویته | گشتاور دوقطبی (D) | قطبیت پیوند |
|---|---|---|---|---|
| H₂ | ۰.۷۴ | ۰.۰ | ۰.۰۰ | کووالانسی غیرقطبی |
| HF | ۰.۹۲ | ۱.۹ | ۱.۸۲ | کووالانسی بسیار قطبی |
| HCl | ۱.۲۷ | ۰.۹ | ۱.۰۸ | کووالانسی قطبی |
| HBr | ۱.۴۱ | ۰.۷ | ۰.۸۲ | کووالانسی قطبی (کمتر) |
| HI | ۱.۶۱ | ۰.۴ | ۰.۴۴ | کووالانسی با قطبیت ضعیف |
| H₂O | ۰.۹۶ | ۱.۲ | ۱.۸۵ | قطبی (مولکول خمیده) |
| NH₃ | ۱.۰۱ | ۰.۸ | ۱.۴۷ | قطبی (مولکول هرمی) |
مقایسه HCl و H₂O : تفاوت در قطبیت
مولکول آب نیز نمونه روشنی از ترکیبات دارای پیوند قطبی است و مقایسه آن با HCl دید بهتری از شدت قطبیت به دست می دهد. در هر پیوند O–H، اکسیژن تمایل بسیار بیشتری به جذب الکترون دارد و همین موضوع باعث می شود الکترون ها به شکل نامتقارن توزیع شوند. اختلاف تمایل الکترونی میان اکسیژن و هیدروژن از اختلاف موجود در پیوند H–Cl بیشتر است و همین عامل، قطبیت بالاتر پیوندهای آب را توضیح می دهد.
علاوه بر این، آب تنها یک پیوند ندارد، بلکه شامل دو پیوند O–H است که در یک ساختار خمیده کنار هم قرار گرفته اند. این آرایش باعث می شود اثر قطبیت هر پیوند خنثی نشود و در نهایت یک دوقطبی قوی برای کل مولکول ایجاد گردد. مقدار این دوقطبی به طور محسوسی از HCl بیشتر است که تنها یک پیوند ساده دارد.
قطبیت بالای آب پیامدهای مهمی به همراه دارد. مولکول های آب به شدت یکدیگر را جذب می کنند و پیوندهای هیدروژنی قدرتمندی می سازند. به همین دلیل، آب در دمای معمولی مایع است و نقطه جوش بالایی دارد.
در مقابل، HCl با قطبیت کمتر و نبود پیوند هیدروژنی، تنها از جاذبه های ضعیف تری بهره می برد و به صورت گاز دیده می شود. این تفاوت ها نشان می دهد شدت قطبیت چگونه رفتار فیزیکی مواد را تغییر می دهد.
قطبیت و نیروهای بین مولکولی در HCl و مولکول های مشابه
میزان قطبیت پیوند در هر مولکول نقش مهمی در نوع و قدرت جاذبه هایی دارد که میان مولکول ها شکل می گیرد. در ترکیبات قطبی مانند HCl، وجود بارهای جزئی مثبت و منفی باعث می شود مولکول ها یکدیگر را از راه نیروهای دوقطبی–دوقطبی جذب کنند. این برهم کنش ها نسبت به نیروهای بسیار ضعیف موجود در مواد غیرقطبی، اثرگذارتر هستند و می توانند رفتار فیزیکی ماده را تغییر دهند.
برای نمونه، HCl با وجود جرم مولکولی نسبتاً کم، نقطه جوشی بالاتر از گازهای غیرقطبی با جرم مشابه دارد. این تفاوت به دلیل همان جاذبه های دوقطبی میان مولکول های HCl است که مانع جدا شدن آسان آن ها از یکدیگر می شود. در مقابل، موادی که فاقد قطبیت هستند، تنها به نیروهای پراکندگی ساده متکی اند و به همین دلیل زودتر به حالت گاز می روند.
اگر قطبیت پیوند بسیار زیاد باشد و هیدروژن به اتمی با تمایل الکترونی بالا متصل شود، امکان ایجاد پیوند هیدروژنی فراهم می گردد. این نوع جاذبه در موادی مانند آب یا HF دیده می شود و قدرت زیادی دارد. به همین علت این ترکیبات، برخلاف انتظار، نقطه جوش بالایی دارند.
در HCl چنین پیوندی شکل نمی گیرد و تنها نیروهای دوقطبی و پراکندگی نقش دارند. با کاهش قطبیت در موادی مثل HBr و HI، این جاذبه ها ضعیف تر می شوند، هرچند بزرگی اتم ها تا حدی اثر را جبران می کند. در مجموع، هرچه قطبیت پیوند بیشتر باشد، نیروهای بین مولکولی نیز قوی تر خواهند بود.
قطبیت پیوند در برابر قدرت اسیدی: HF در مقابل HCl
مقایسه اسید هیدروکلریک و اسید هیدروفلوئوریک نکته مهمی را روشن می کند: میزان قطبیت پیوند به تنهایی معیار قدرت اسیدی نیست. در آب، HCl رفتاری شبیه یک اسید قوی دارد و تقریباً به طور کامل به یون های هیدروژن و کلرید تبدیل می شود. در مقابل، HF با وجود قطبیت بالاتر، تنها بخشی از مولکول هایش در آب یونیزه می شوند.
دلیل اصلی این تفاوت به استحکام پیوند برمی گردد. پیوند H–F اگرچه بسیار قطبی است، اما به شدت محکم می باشد. اندازه کوچک اتم فلوئور و جاذبه قوی میان هیدروژن و فلوئور باعث می شود این اتصال به آسانی شکسته نشود. به همین خاطر، مولکول های آب نمی توانند به راحتی هیدروژن را از HF جدا کنند.
در سوی دیگر، پیوند H–Cl کمی ضعیف تر و بلندتر است. همین ویژگی اجازه می دهد آب ساده تر وارد عمل شود و یون H⁺ را از مولکول جدا کند. در نتیجه، HCl بدون مقاومت زیاد تفکیک می شود و خاصیت اسیدی شدیدی از خود نشان می دهد.
این مقایسه نشان می دهد قطبیت بالا همیشه به معنای اسید قوی تر نیست. برای اسیدی قوی، پیوند باید علاوه بر داشتن بارهای جزئی، به اندازه کافی سست باشد. در مورد HCl و HF، انرژی کمتر پیوند در HCl عامل تعیین کننده قدرت اسیدی بیشتر آن است.




